
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
26ЃЎФГД§ВтвКжаПЩФмКЌгаAg+ЁЂFe3+ЁЂK+ЁЂBa2+ЁЂNH4+ЕШРызгЃЌНјааШчЯТЪЕбщЃК
(1)МгШыЙ§СПЕФЯЁбЮЫсЃЌгаАзЩЋГСЕэЩњГЩЁЃ
(2)Й§ТЫЃЌдкТЫвКжаМгШыЙ§СПЕФЯЁСђЫсЃЌгжгаАзЩЋГСЕэЩњГЩЁЃ
(3)Й§ТЫЃЌШЁЩйСПТЫвКЃЌЕЮШы2ЕЮKSCNШмвКЃЌУЛгаУїЯдЕФЯжЯѓГіЯжЁЃ
(4)СэШЁЩйСПВНжш(3)жаЕФТЫвКЃЌМгШыNaOHШмвКжСЪЙШмвКГЪМюадЃЌМгШШЃЌПЩВњЩњЪЙЪЊ
ШѓЕФКьЩЋЪЏШяЪджНБфРЖЩЋЕФЦјЬхЁЃ
ИљОнЪЕбщЯжЯѓЛиД№ЃКД§ВтвКжавЛЖЈКЌгаЁЁЁЁЁЁЁЁ РызгЃЌвЛЖЈВЛКЌгаЁЁ ЁЁЁЁРызгЃЌЛЙгавЛжжРызгВЛФмШЗЖЈЪЧЗёДцдкЃЌвЊМьбщетжжРызгЕФЪЕбщЗНЗЈЪЧ(ЬюаДЪЕбщУћГЦКЭЙлВьЕНЕФЯжЯѓЃЌВЛвЊЧѓаДЪЕбщВйзїЙ§ГЬ)ЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
0.1molЁЄLЃ1ЃЌЙЄзївЛЖЮЪБМфКѓЃЌВтЕУЕМЯпЩЯЭЈЙ§0.02 molЕчзгЃЌШєВЛПМТЧбЮ
ЫЎНтКЭШмвКЬхЛ§ЕФБфЛЏЃЌдђЯТСаа№Ъіе§ШЗЕФЪЧ
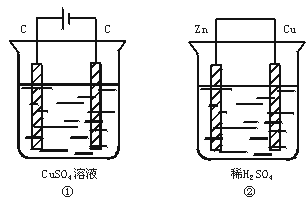
AЃЎВњЩњЦјЬхЕФЬхЛ§ЃКЂйЃОЂк
BЃЎЕчМЋЩЯЮіГіЙЬЬхЕФжЪСПЃКЂйЃОЂк
CЃЎШмвКЕФpHБфЛЏЃКЂйдіДѓЃЌЂкМѕаЁ
DЃЎЕчМЋЗДгІЪНЃКЂйбєМЋЃК4OHЃЃ4eЃ===2H2O+O2Ёќ
ЂквѕМЋЃК2H++2eЃ===H2ЁќЁЁ
25ЃЎШчЯТЭМЫљЪОСНИізАжУжаЃЌШмвКЬхЛ§ОљЮЊ200 mLЃЌПЊЪМЪБЕчНтжЪШмвКЕФХЈЖШОљЮЊ
24ЃЎ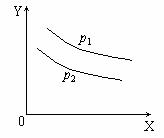 ЗДгІL(ЙЬ)+aG(Цј)
ЗДгІL(ЙЬ)+aG(Цј) bR(Цј)ДяЕНЦНКт
bR(Цј)ДяЕНЦНКт
ЪБЃЌЮТЖШКЭбЙЧПЖдИУЗДгІЕФгАЯьШчЯТЭМЫљЪОЃЌ
ЭМжаЃКбЙЧПp1>p2ЃЌXжсБэЪОЮТЖШЃЌYжсБэЪОЦН
КтЛьКЯЦјжаGЕФЬхЛ§ЗжЪ§ЁЃОнДЫПЩХаЖЯ
(1)ЩЯЪіЗДгІЪЧЗХШШЗДгІ
(2)ЩЯЪіЗДгІЪЧЮќШШЗДгІ
(3)a>b
(4)a<b
AЃЎ(1)(2)ЁЁЁЁ ЁЁBЃЎ(3)(4)ЁЁЁЁЁЁ CЃЎ(1)(3)ЁЁЁЁ ЁЁDЃЎ(2)(4)
23ЃЎЕчЦПГЕЫљгУЕчГивЛАуЮЊЧІаюЕчГиЃЌетЪЧвЛжжЕфаЭЕФПЩГфЕчЕчГиЃЌЕчГизмЗДгІЪНЮЊ
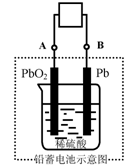 Pb+PbO2+4H++2SO42Ѓ
Pb+PbO2+4H++2SO42Ѓ 2PbSO4+2H2OЃЌ
2PbSO4+2H2OЃЌ
дђЯТСаЫЕЗЈе§ШЗЕФЪЧ
AЃЎЗХЕчЪБЃКЕчзгСїЖЏЗНЯђгЩAЕНB
BЃЎЗХЕчЪБЃКе§МЋЗДгІЪЧPb-2eЃ+SO42Ѓ PbSO4
PbSO4
CЃЎГфЕчЪБЃКЧІаюЕчГиЕФИКМЋгІгыГфЕчЦїЕчдД
ЕФе§МЋЯрСЌ
DЃЎГфЕчЪБЃКбєМЋЗДгІЪЧPbSO4Ѓ2eЃ+2H2O
PbO2+SO42Ѓ+4H+
22ЃЎФГЮТЖШЯТЃЌЗДгІN2O4(Цј)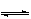 2NO2(Цј)ЁїH>0ЃЌдкУмБеШнЦїжаДяЕНЦНКтЃЌЯТСаЫЕЗЈ
2NO2(Цј)ЁїH>0ЃЌдкУмБеШнЦїжаДяЕНЦНКтЃЌЯТСаЫЕЗЈ
ВЛе§ШЗЕФЪЧ
AЃЎМгбЙЪБ(ЬхЛ§БфаЁ),НЋЪЙе§ЗДгІЫйЖШдіДѓ
BЃЎБЃГжЬхЛ§ВЛБф,МгШыЩйаэNO2,НЋЪЙе§ЗДгІЫйЖШМѕаЁ
CЃЎБЃГжЬхЛ§ВЛБф,МгШыЩйаэN2O4,дйДяЕНЦНКтЪБ,беЩЋБфЩю
DЃЎБЃГжЬхЛ§ВЛБф,Щ§ИпЮТЖШ,дйДяЦНКтЪБбеЩЋБфЩю
21ЃЎЗЈЙњРяАКЕФПЦбЇМвзюНќЗЂЯжвЛжжжЛгЩЫФИіжазгзщГЩЕФЮЂСЃЃЌетжжЮЂСЃГЦЮЊЁАЫФжазгЁБЃЌ
вВгаШЫГЦжЎЮЊЁАСуКХдЊЫиЁБЁЃЫќгыЬьЬхжаЕФжазгаЧЙЙГЩРрЫЦЁЃгаЙиЃКЁАЫФжазгЁБЮЂСЃЕФЫЕ
ЗЈе§ШЗЕФ
AЃЎИУЮЂСЃВЛЯдЕчадЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁBЃЎИУЮЂСЃЕФжЪСПЪ§ЮЊ2
CЃЎдкдЊЫижмЦкБэжагыЧтдЊЫиеМЭЌвЛЮЛЁЁ ЁЁЁЁЁЁЁЁDЃЎЫќгыЦеЭЈжазгЛЅГЦЮЊЭЌЮЛЫи
20ЃЎЯТСаЙигкдЊЫиЕФа№Ъіе§ШЗЕФЪЧ
AЃЎЗЧН№ЪєдЊЫиМфвВПЩвдаЮГЩРызгЛЏКЯЮя
BЃЎжЛгадкдзгжаЃЌжЪзгЪ§ВХгыКЫЭтЕчзгЪ§ЯрЕШ
CЃЎФПЧАЪЙгУЕФдЊЫижмЦкБэжаЃЌзюГЄЕФжмЦкКЌга36жждЊЫи
DЃЎЗЧН№ЪєдЊЫиаЮГЩЕФЙВМлЛЏКЯЮяжаЃЌдзгЕФзюЭтВуЕчзгЪ§жЛФмЪЧ2Лђ8
19ЃЎдк100mLКЌЕШЮяжЪЕФСПЕФHBrКЭH2SO3ЕФШмвКРяЭЈШы0.01mol Cl2ЃЌгавЛАыBr-БфЮЊBr2
(вбжЊBr2ФмбѕЛЏH2SO3)ЁЃдШмвКжаHBrКЭH2SO3ЕФХЈЖШЖМЕШгк
AЃЎ0.0075mol/LЁЁ ЁЁЁЁBЃЎ0.008mol/L ЁЁЁЁЁЁCЃЎ0.075mol/LЁЁ ЁЁЁЁDЃЎ0.08mol/L
18ЃЎЯТСаЯжЯѓЕФЗЂЩњЃЌгыЛЏбЇБфЛЏЮожБНгЙиЯЕЕФЪЧ
AЃЎЦЄЗєВЛЩїеДгаХЈЯѕЫсГЪЛЦЩЋЁЁЁЁЁЁЁЁ BЃЎгУТШЛЏФЦзібцЩЋЗДгІЪЕбщЃЌЛ№бцГЪЛЦЩЋ
CЃЎОУжУдкПеЦјжаЕФKIШмвКГЪЛЦЩЋЁЁЁЁЁЁ DЃЎЪЂдкЮоЩЋЪдМСЦПжаЕФХЈЯѕЫсГЪЛЦЩЋ
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com