
题目列表(包括答案和解析)
26.(12分)已知A、B、C、D、X、Y六种物质均由短周期元素组成,其中X为常见离子化合物,它们之间的转换关系如下图所示
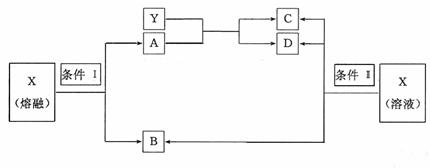
(1)已知条件I和条件II相同,则该反应条件为
(2)物质X的电子式为
(3)写出B与Ca(OH)2反应的化学方程式
(4)写出X在条件II下反应生成B、C、D的离子方程式
(5)写出实验室制B的化学方程式,并标出电子转移方向、数目
(6)请简述鉴定物质X的实验方法: .
25.(6分)某无色溶液,由Na+、Ag+、Ba2+、Al3+、、、、中的若干种组成。取该溶液进行如下实验:
(A)取适量试液,加入过量盐酸,有气体生成,并得到溶液;
(B)在(A)所得溶液中再加入过量碳酸氢铵溶液,有气体生成,同时析出白色沉淀甲;
(C)在(B)所得溶液中加入过量Ba(OH)2溶液,也有气体生成,并有白色沉淀乙析出。
根据上述实验回答下列问题:
⑴ 溶液中一定不存在的离子是 。
⑵ 一定存在的离子是 。
⑶ 判断沉淀乙成份的方法是 。
24.(12分)A、B、C、D、E都是短周期元素,原子序数依次增大,B、C同周期,A、D同主族。A、B能形成两种液态化合物甲和乙,原子个数比分别为2∶1和1∶1。C单质的氧化性最强。E的单质既能与强酸反应,也能与强碱反应。根据以上信息回答下列问题:
(1)甲、乙两分子中含有非极性键的物质是________分子(填“极性”或“非极性”)请用电子式表示其形成过程___________________________________________。
(2)C元素在周期表中的位置是__________________。
(3)C和D的离子中,半径较小的是__________(填离子符号)。
(4)将D的单质投入甲中,待D消失后再向上述溶液中加入E的单质,此时发生反应的化学方程式是____________________________________________________。
 (5)C、D、E可组成离子化合物DxEC6,其晶胞结构如右图所示,阳离子D+位于正方体的棱的中点和正方体内部;阴离子EC6x-位于该正方体的顶点和面心。该化合物的化学式是____________。
(5)C、D、E可组成离子化合物DxEC6,其晶胞结构如右图所示,阳离子D+位于正方体的棱的中点和正方体内部;阴离子EC6x-位于该正方体的顶点和面心。该化合物的化学式是____________。
23.(12分)下图是元素周期表的一部分,表中所列字母分别代表某一化学元素:
|
|
|
|
|
|
||||||||||||||
|
a |
|
|
b |
c |
d |
e |
|
|||||||||||
|
f |
|
g |
|
|
h |
|
i |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
j |
|
|
(1)g的单质能与f元素的最高价氧化物对应的水化物的溶液反应,请写出该反应的离子方程式 。
(2)将等物质的量的f、g的单质投入足量水中,反应后逐滴加入1mol/L的盐酸溶液,到100mL时能产生最大沉淀。则在该过程中一共放出 L气体(标况)

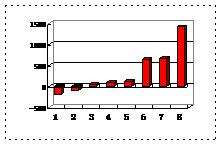
(3)第三周期8种元素按单质熔点(℃)大小顺序的柱形图(上左图),其中序列“2”代表 ,“8”代表 。
(4)a、b、c、d、e的氢化物的沸点直角坐标图(上右图),序列“5”氢化物的化学式为 ,序列“1”的氢化物的电子式: 。
22.铜和镁的合金4.7克完全溶于浓硝酸中,若反应中硝酸被还原只产生4480mL的NO2气体和336mL的N2O4气体(都已经折算成标准状况)。在反应后的溶液中加入足量的NaOH溶液,生成沉淀的质量为( )
A.9.02g B.8.26g C.8.61g D.7.04g
第II卷 非选择题部分(共56分)
21.Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1:16,则x的值是( )
A.2 B.3 C.4 D.5
20.郑老师做了一个如图所示的实验,发现烧杯中酸性KMnO4溶液褪色。若将烧杯中的溶液换成有少量KSCN和FeCl2溶液,溶液显红色。判断下列说法中正确的是( )
A.该条件下生成的水分子化学性质比较活泼
B.该条件下H2被冷却为液态氢,液氢的水溶液具有还原性
C.该条件下H2燃烧生成了只具有还原性的物质
D.该条件下H2燃烧的产物中可能含有一定量的H2O2
18.A、B、C、D为四种短周期元素,已知A、C同主族,B、D同周期;A的气态氢化物比C的气态氢化物稳定;B的阳离子比D的阳离子氧化性强;B的阳离子比C的阴离子少一个电子层。下列叙述正确的是( )
A.原子序数:A>B>C>D B.单质熔点:D>B,A>C
C.原子半径:D>B>C>A D.简单离子半径:D>B>C>A
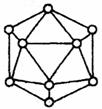 19.晶体硼的基本结构单元都是由硼原子组成的二十面体的原子晶体(如下图)。其中含20个等边三角形和一定数量的顶角,每个顶角上各有一个
19.晶体硼的基本结构单元都是由硼原子组成的二十面体的原子晶体(如下图)。其中含20个等边三角形和一定数量的顶角,每个顶角上各有一个
原子。试观察推断这个基本结构单元所含B原子数,
B-B键个数及键角正确的一组是( )
A.20个,60个,360° B.12个,30个,60°
C.9个,18个,45° D.18个,54个,90°
17.氯化碘(ICl)跟 水发生反应:ICl+H2O=HIO+HCl,这个过程可以称为ICl的水解。预计PCl3水解的产物是 ( )
A.PH3和HClO B.HCl和H3PO4 C.HCl和H3PO3 D.HCl和HPO3
16.下列性质的比较中,正确的是( )
A.熔点:Li>Na>K>Rb B.沸点:NH3<PH3<AsH3<SbH3
C.热稳定性:SiH4>PH3>H2O>HF D.酸性:HClO>H2SO4>H3PO4>H2CO3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com