
题目列表(包括答案和解析)
1、下列分子中所有原子都满足最外层8电子结构的是( )
A.HF B.CO2 C.BF3 D.PCl5
20.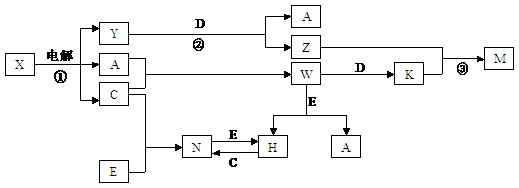 (12分)中学化学中几种常见物质的转化关系如图所示(图中部分反应物或生成物及反应条件未列出)。
(12分)中学化学中几种常见物质的转化关系如图所示(图中部分反应物或生成物及反应条件未列出)。
已知:常温下,A、C为气态单质,B、D、E是固态单质,组成它们的元素的原子序数依次为a、b、c、d、e;且3(a + b) = 2(a + c) = 3(d -a),X、Y、Z、M、N、W、H、K是化合物,其中X是B和C的化合产物的水溶液。请回答下列问题:
(1)用电子式表示X中溶质的形成过程:_______________,组成D的元素的原子结构示意图是_____ 。
(2)写出B在氧气中燃烧生成的产物与H2O反应的化学方程式:
_______________________________________________________________。
(3)组成单质B、C、D的三种元素简单离子的离子半径由大到小的顺序是 _____ > ______ > ______(用离子符号表示)。
(4)常温下,N溶液的PH<7,原因是 (写出相应离子方程式);
写出M在水溶液中电离的方程式 。
19.(12分)现有浓度各为1 mol/L的FeCl3、FeCl2、CuCl2的混合溶液100mL,加入一定量的铁粉,按下列情况填空:
①充分反应后铁粉有剩余,则溶液中一定没有__________阳离子。有关反应的离子方程式是____________________________________________________________________________。
②充分反应后铁粉无剩余,有铜生成。则反应后的溶液中可能含有的阳离子是_________,该阳离子在溶液中物质的量的可能存在范围是: ______________________。
③充分反应后,无固体沉淀物存在,检验反应后的溶液中是否含有Fe3+的方法是 。
18.(10分) 中学常见反应的化学方程式是A+B→X+Y+H2O(未配平,反应条件略去),其中A、B的物质的量之比为1:4。请回答:
中学常见反应的化学方程式是A+B→X+Y+H2O(未配平,反应条件略去),其中A、B的物质的量之比为1:4。请回答:
(1)若Y是黄绿色气体,B为常见强酸,则Y的电子式是 ,Y在工业或日常生活中的重要用途是 (举一例)。
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为某浓酸,则反应中氧化剂与还原剂的物质的量之比是 。
(3)若A为金属单质,常温下A在B的浓溶液中“钝化”,且A可溶于X溶液中。
①A元素在周期表中的位置是 (填所在周期和族)。
②含a mol X的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量恰好相等,则被还原的X是 mol。
17.(18分)10月12日,浏阳一中进行了学业水平考试实验操作,试题分别为:Ⅰ.配制一定物质的量浓度的盐酸。Ⅱ.几种重要金属化合物的性质。
⑴、实验Ⅰ中合理的实验操作顺序是 定容和摇匀。(填序号)
①稀释,②计算和量取,③转移和洗涤,④查漏。
⑵、实验Ⅰ中两次使用玻璃棒,其作用分别为 、 ;配制1.19mol/l盐酸200ml,需36.5%(ρ=1.19g/ml)的浓盐酸多少 ml。
⑶、实验Ⅱ中的仪器为:试管、钥匙、胶头滴管。试剂有:①铁粉②氨水③氢氧化钠溶液④硫酸铝溶液⑤KSCN溶液(滴瓶盛装)⑥氯化铁溶液(滴瓶盛装)⑦稀盐酸。
填空:上述不同的试剂应该存放相关的试剂瓶,广口瓶存放 (填试剂序号,下同),带橡皮塞的细口玻璃瓶存放 。个别小组实验结束后,发现硫酸铝试剂瓶中有白色沉淀,可能原因是 。(填序号)
A、铝离子水解引起,B、空气中大量氨气溶解于试剂瓶中,C、生成了硫酸钡,D、滴加氢氧化钠溶液的滴管插入该试剂瓶中,E、滴加盐酸的滴管插入该试剂瓶中,F、滴加氨水的滴管插入该试剂瓶中。
请根据实际情况分析、推测沉淀的成分并设计实验、运用实验Ⅱ中的仪器和试剂检验该沉淀的成分,完成下列实验步骤:①将被污染试剂过滤并洗涤沉淀,②转移固体至试管中(两支以上),③ 。④ 。⑤ 。(可以不填满)写出相关反应的离子反应方程式 。
16、将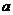 mol钠和
mol钠和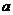 mol铝一同投入
mol铝一同投入 g足量水中,所得溶液密度为
g足量水中,所得溶液密度为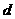 g·mL-1,该溶液中溶质质量分数为 (
)
g·mL-1,该溶液中溶质质量分数为 (
)
A.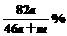 B.
B.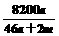 % C.
% C.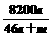 % D.
% D.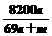 %
%
15、某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、CO32-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化的图象如下所示,下列说法正确的是
A.原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+[
B.原溶液中一定含有SO42-和Na+
C.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
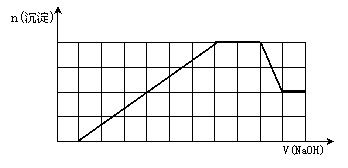 D.反应最后形成的溶液中含有的溶质为Na2SO4
D.反应最后形成的溶液中含有的溶质为Na2SO4
14、下列关于硅单质及其化合物的说法正确的是( )
①硅是构成一些岩石和矿物的基本元素 ②水泥、玻璃、水晶饰物都是硅酸盐制品 ③高纯度的硅单质广泛用于制作光导纤维 ④陶瓷是人类应用很早的硅酸盐材料 ⑤硅胶是硅酸凝胶经干燥脱水后得到的多孔固体
A.①②⑤ B.②③⑤ C.①④⑤ D.③④
13、某溶液含有①NO3-、②HCO3-、③SO32-、④CO32-、⑤SO42-等五种阴离子。向其中加入少量的Na2O2固体后,溶液中离子浓度基本保持不变的是(设溶液体积无变化)( )
A.① B.①②④ C.①③⑤ D.①③④⑤
12、有A、B两个完全相同的装置,某学生分别在它们的侧管中装入1.06 g Na2CO3和0.84 g NaHCO3,A、B中分别有10 mL相同浓度的盐酸,将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是 ( )
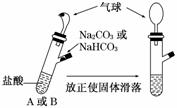
A.A装置的气球膨胀速率大
B.若最终两气球体积相同,则盐酸的浓度一定大于或等于1 mol/L
C.若最终两气球体积不同,则盐酸的浓度一定小于或等于2mol/L
D.最终两试管中Na+、Cl-的物质的量不一定相同
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com