
题目列表(包括答案和解析)
21、在ag浓度为18mol/L,密度为Ρg/cm3的浓硫酸中加入一定量的水,稀释成9mol/L的硫酸,则加入水的体积( )
A.小于amL B.等于amL
C.大于amL D.等于a/ΡmL
河北正定中学2010-2011学年第一学期第二次考试

 高三年级化学试卷
高三年级化学试卷
卷Ⅱ(非选择题 共52分)
20、一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g)
 3C(g),若反应开始时充入2
mol A和2
mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是( )
3C(g),若反应开始时充入2
mol A和2
mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是( )
A.2 mol C
B.1 mol B和1 molC
C.2 mol A,1 mol B和1 mol Ar(不参加反应)
D.2 mol A,3 mol B和3 mol C
19、下列条件下,可能大量共存的离子组是( )
A.常温下水电离的c(OH-)为1×10-10 mol/L的溶液中:AlO2-、CO32-、K+、Na+
B.常温下水电离的c(OH-)为1×10-5 mol/L的溶液中:S2-、SO42-、S2O32-、K+
C.在含有Fe3+、Cl-的溶液中:HCO3-、I-、NH4+、Mg2+
D.在含有KNO3和NaHSO4的溶液中:Fe2+、Ca2+、Al3+、Cl-、Br-
18、①pH=2的CH3COOH; ②pH=2的HCl; ③pH=12的氨水;④pH=12的NaOH溶液。相同条件下,有关上述溶液的比较中,不正确的是( )
A.水电离的c(H+):①=②=③=④
B.将②③两溶液等体积混合所得的溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.等体积的①②④溶液分别与足量铝粉反应,生成H2的量②最大
D.向溶液中加入100mL水后,溶液的pH:③>④>②>①
17.99℃时KW=1x10-12,该温度下在某物质的溶液中,由水电离出的H+浓度为1×10-a mol/L,下列说法不正确的是 ( )
A.a<6时,水的电离受到促进
B.a>6时,水的电离受到抑制
C.a<6时,溶液的pH可能为a
D.a>6时,溶液的pH一定为12-a
16、设NA为阿佛加德罗常数,下列叙述中正确的是( )
A.124g白磷中含有P-P键的个数为4NA
B.12g石墨中含有C-C键的个数为1.5NA
C.1mol金刚石中含有C-C键的个数为2NA
D.60gSiO2中含有Si-O键的个数为2NA
15、有下列离子晶体空间结构示意图:●为阳离子,○为阴离子。以M代表阳离子,N代表阴离子,化学式为MN2的晶体结构为( )
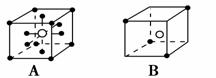
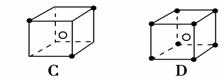
14、下列物质性质的变化规律,与共价键的键能大小无关的是( )
①F2、Cl2、Br2、I2的熔点、沸点逐渐升高
②HF、HCl、HBr、HI的热稳定性依次减弱
③金刚石、碳化硅、晶体硅熔点逐渐降低
④NaF、NaCl、NaBr、NaI的熔点依次降低
A. 仅② B. ①④ C. ②③ D. ①②③
13、在盛有足量 A 的体积可变的密闭容器中,加入B ,发生反应:
A (s)+2B(g) 4C(g) + D ( g );△H < 0 。
4C(g) + D ( g );△H < 0 。
在t℃、p KPa下达到平衡。平衡时 C 的物质的量与加入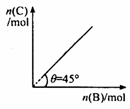 的
B 的物质的量的变化关系如右图。下列说法正确的是( )
的
B 的物质的量的变化关系如右图。下列说法正确的是( )
A.平衡时B的转化率为33.3 %
B.若再加入B,则再次达到平衡时正、逆反应速率均增大,但仍然相等
C.若再加人4molC和1molD ,则再次达到平衡时体系气体密度减小,平均摩尔质量不变
D.若温度变为(t+10)℃,则θ<45°
12、常温下甲为pH=2的醋酸溶液,乙为pH=2的醋酸和盐酸的混合溶液,下列说法正确的是( )
A.甲溶液中c(CH3COO-)一定大于乙溶液中c(CH3COO-)
B.甲、乙等体积混合后pH大于2
C.乙溶液离子浓度大小关系为:c(Cl-) >c(CH3COO-) > c(H+) >c(OH-)
D.加入相同浓度的NaOH溶液至中性,甲乙两溶液消耗NaOH溶液的体积相同
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com