
题目列表(包括答案和解析)
29.(12分)某同学用如图一所示的装置来探究CO2、
SO2与澄清石灰水的反应,结果通入CO2可以看
到先浑浊后澄清的现象,但通入SO2没有能看到
浑浊现象。经过思考分析后,该同学改用图二的
装置,将气体收集在注射器,缓慢地将气体一个
气泡一个气泡地通入澄清石灰水中,都能看到石
灰水先变浑浊再澄清的现象,且通入SO2产生
现象明显比通入CO2快。
(1)对比分析两组实验,你认为用图一装置实验
时,通入SO2不能出现浑浊的原因可能是:
_________________。
(2)用图二装置实验时,以相同速率通入CO2或
SO2,SO2产生浑浊、澄清的现象比CO2
快的原因是______________________________________。
(3)用图一进行SO2与石灰水反应的实验时,从安全角度
考虑装置应做何改进?
_____________________________________________。
(4)有人提出上述实验现象“石灰水先变浑浊再澄清”可能与澄清石灰水的浓度有关。为了探究CO2通入澄清石灰水中的实验现象,查得下列数据:
Ⅰ 20℃时,Ca(OH)2 的溶解度为:0.165g/100g水。
Ⅱ 不同浓度石灰水生成CaCO3的最大量
|
饱和石灰水与水的体积比 |
1:0 |
1:1 |
1:2 |
1:3 |
1:5 |
1:7 |
|
能生成CaCO3的最大量(g/100水) |
A |
0.110 |
0.073 |
0.055 |
0.037 |
0.028 |
① 上表中A= g/100g水
Ⅲ 在1.01×105Pa CO2压力下,CaCO3的溶解度
|
热力学温度/K |
282 |
298 |
308 |
|
CaCO3溶解度(g/100水) |
0.130 |
0.094 |
0.076 5 |
Ⅳ 在不同压强(CO2)下,CaCO3溶解度(18℃)
|
P(CO2)/Pa |
0 |
1.40×104 |
9.95×104 |
|
CaCO3溶解度(g/100水) |
0.001 3 |
0.023 3 |
0.108 6 |
认真分析以上数据回答下列问题:
②由表Ⅲ和表Ⅳ可知CaCO3溶解度的变化规律是:
③由以上数据可以得出结论:欲观察到“石灰水先变浑浊再澄清的现象”,所需要的实验条件是:
28.(9分)A、B、C、D、E五种短周期元素,已知:它们的原子序数依次增大,A、B两种元素的核电荷数之差等于它们的原子最外层电子数之和;B原子最外层电子数比其次外层电子数多2;在元素周期表中,C是E的不同周期邻族元素;D和E的原子序数之和为30。它们两两形成的化合物为甲、乙、丙、丁四种。这四种化合物中原子个数比如下表:(用元素符号作答)
|
|
甲 |
乙 |
丙 |
丁 |
|
化合物中各元素原子个数比 |
A:C=1:1 |
B:A=1:2 |
D:E=1:3 |
B:E=1:4 |
(1)写出A~E的元素符号
A: B: C: D: E:
(2)向甲的水溶液中加入MnO2,氧化产物是 。
(3)已知有机物乙的分子为平面结构,碳氢键键角为120°,实验室制取乙的化学方程式为:
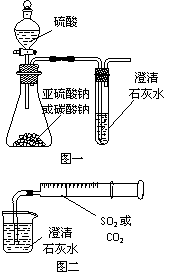 (4)丙的水溶液呈酸性,与饱和NaHCO3溶液反应会产生大量气体和难溶物,有关离子方程式是:
(4)丙的水溶液呈酸性,与饱和NaHCO3溶液反应会产生大量气体和难溶物,有关离子方程式是:
27.(8分)现有①CaBr2 ②金刚石 ③ 铜 ④干冰 ⑤Na2SO4 ⑥碘片 ⑦NH4Cl ⑧晶体硅八种物质,按下列要求回答(填序号):
(1)晶体熔化时需要破坏共价键的是 ,熔点最低的是 。
(2)属于离子晶体的是 。
(3)晶体中只存在一种微粒间作用力是 。
26.(4分)一种有机化合物的结构简式如下:
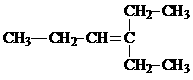
(1)该分子中有 个sp2杂化碳原子; 个sp3杂化碳原子。
(2)该分子中有 个sp2-sp3的σ键; 个sp3-sp3的σ键型。
24.分子式为C9H6O3(只有苯环而不含其它的环)的有机物在苯环上的一氯取代物只有一种的结构种类为 ( )
A.2种 B.3种 C.4种 D.5种
25.A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X。它们有如下的转化关系:A在碱性条件下反应生成B、C,B、C在酸性条件下生成A。(部分产物及反应条件已略去):下列判断正确的是 ( )
A.反应①和②一定为氧化还原反应 B.X元素不一定为非金属元素
C.反应①和②互为可逆反应 D.X元素可能为Al
第Ⅱ卷(非选择题 共45分)
23.现有200mL MgCl2和AlCl3的混合溶液,其中c(Mg2+)=0.2mol/L,c(Cl-)=1.3mol/L,要使Mg2+转化成Mg(OH)2,并使Mg2+、Al3+分离开来,4mol/L NaOH溶液的最少用量为 ( )
A.140mL B.120mL C.11mL D.80mL
22.下列说法中正确的是 ( )
A.天然气、液化气和氢气分别属于化石能源、可再生能源和新能源
B.蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质
C.光导纤维、集成电路晶体管,分别属于硅和二氧化硅的用途之一
D.碳酸钠、氢氧化钠、碳酸氢钠的俗名分别为苏打、纯碱、小苏打
21.根据已学知识推断下列数据可信的是 ................. ( )
A.某元素的原子半径是0.160nm B.某常见气体的密度为1.8g/cm3
C.某硫酸钙溶液的浓度是2.0mol/L D.某溶液中溶质的质量分数超过100%
20.X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如下转化关系(其它产物已略去):下列说法不正确的是( )
 A.若W是单质铁,则Z溶液可能是
A.若W是单质铁,则Z溶液可能是 FeCl2溶液
FeCl2溶液
B.若W是氢氧化钠,则X与Z可反应生成Y
C.若X是金属镁,则W可能是强氧化性的单质
D.若X为甲醇,则X、Z的相对分子质量可能相差14
19.下面是两种兴奋剂的结构简式:
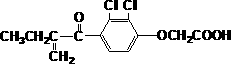
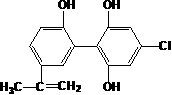
兴奋剂X 兴奋剂Y
关于它们的说法中正确的是 ( )
A.1mol X与足量的NaOH溶液在常温常压下反应,最多消耗3mol NaOH
B.1mol X与足量的氢气反应,最多消耗2mol H2
C.Y与足量的浓溴水反应,能产生白色沉淀
D.Y遇到FeCl3溶液时显紫色,但不能使溴的四氯化碳溶液褪色
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com