
题目列表(包括答案和解析)
21、元素X的离子和其含氧酸根离子,在pH=0的溶液中产生X的单质沉淀,且氧化产物与还原产物质量之比为2:1,X可能是
A.氯 B.硫 C.硅 D.铝
20、利用核聚变发电,3He是最安全、最清洁的能源。地球上3He仅有15吨左右,月球上的3He最保守估计可供全世界开采500年。地球上的氦元素主要以4He形式存在,而月球土壤中吸附着数百万吨3He。下列说法正确的是
①3He、4He的化学性质基本相同;②3He、4He具有相同的中子数;③3He核聚变是化学变化;④3He液化是物理变化;⑤3He和4He形成的晶体类型相同,所含化学键不同;⑥3He和4He组成的气体单质,在相同条件下密度之比为3︰4。
A.①②⑤ B.①④⑥ C.②③⑤ D.③④⑥
19、在水玻璃中通入少量的CO2气体,充分反应后加热蒸干,再高温充分灼烧,冷却后所得的固体物质为
A.Na2SiO3 B.Na2SiO3与Na2CO3
C.SiO2与Na2CO3 D.SiO2、Na2SiO3及Na2CO3
18、向硫酸氢钠溶液中滴加氢氧化钡溶液,溶液的pH与生成的沉淀关系如图所示,正确的是A

16、 已知:2CO(g) + O2(g) == 2CO2(g) ΔH=-566 kJ·mol-1
N2(g) + O2(g)
== 2NO(g) ΔH=+180
kJ·mol-1
则2CO(g) +2NO(g) == N2(g)+2CO2(g)的ΔH是
A.-386kJ·mol-1
B.+386kJ·mol-1
C.-746kJ·mol-1 D.+746kJ·mol-1
17、将足量CO2通入NaOH和Ba(OH)2的混合稀溶液中,生成沉淀的物质的量(n)和通入CO2体积(V)的关系如图,图中AB段表示的先后离子方程式是 ( )
已知:2CO(g) + O2(g) == 2CO2(g) ΔH=-566 kJ·mol-1
N2(g) + O2(g)
== 2NO(g) ΔH=+180
kJ·mol-1
则2CO(g) +2NO(g) == N2(g)+2CO2(g)的ΔH是
A.-386kJ·mol-1
B.+386kJ·mol-1
C.-746kJ·mol-1 D.+746kJ·mol-1
17、将足量CO2通入NaOH和Ba(OH)2的混合稀溶液中,生成沉淀的物质的量(n)和通入CO2体积(V)的关系如图,图中AB段表示的先后离子方程式是 ( )
①CO2+OH-=HCO3- ②CO2+2OH- =CO32-+ H2O ③CO32-+Ba2+=BaCO3↓
④ BaCO3+CO2+H2O=Ba2++2HCO3- ⑤CO32-+CO2+H2O=2HCO3-
A.②⑤ B.⑤④ C.④② D.④①
13、设NA是阿伏加德罗常数的值,下列说法正确的是 A.标准状况下,22.4L乙醇中含有的氧原子数为NA B.标准状况下,22.4L37Cl2中所含中子数为4NA C.将0.1mol氯化铁溶于1L水中,所得溶液含有0.1NA个Fe3+ D.25℃时,pH=13的1.0L Ba(OH)2溶液中含有OH-数目为0.2NA 14、化学与生活、社会密切相关。下列说法正确的是 A.用NaOH溶液雕刻工艺玻璃上的纹饰 B.Na2O可用于呼吸面具中作为氧气的来源 C.工业上硝酸可用于制化肥、农药、炸药和染料等 D.向煤中加入适量CaSO4,可大大减少燃烧产物中SO2的量 15、将足量稀盐酸加到下列固体混合物中,只能发生一种反应的是
A、Mg、AlCl3、NaAlO2 B、KNO3、NaCl、CH3COONa
C、NaClO、Na2SO3、BaCl2 D、Ba(NO3)2、FeSO4、NH4HCO3
11、针对节能减排课题。某研究性学习小组提出如下方案,你认为不符合课题要求的是 A.利用太阳能制氢燃料 B.利用潮汐能发电 C.大力建设火电厂 D.用节能灯代替白炽灯 12、类比推理是化学学习中的一种重要方法。下列类推结论正确的是
|
|
类比对象 |
结论 |
|
A |
Cl2+H2O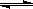 HCl+HClO HCl+HClO |
I2+H2O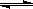 HI+HIO HI+HIO |
|
B |
C+2CuO 2Cu+CO2↑ 2Cu+CO2↑ |
C+SiO2 Si+
CO2↑ Si+
CO2↑ |
|
C |
Na2O+H2O==2NaOH |
CuO+H2O==Cu(OH)2 |
|
D |
Ca(ClO)2+CO2+H2O==CaCO3↓+2HClO |
Ca(ClO)2+SO2+H2O==CaSO3↓+2HClO |
4、2004年7月德俄两国化学家共同宣布,在高压下氮气会聚合生成高聚氮,这种高聚氮的 晶体中每个氮原子都通过三个单键与其它氮原子结合并向空间发展构成立体网状结构。已知晶体中N-N键的键能为160 kJ·mol-1,而N≡N的键能为942 kJ·mol-1(键能表示形成化学键释放的能量或者破坏化学键消耗的能量)。则下列有关说法不正确的是 A.键能越大说明化学键越牢固,所构成物质越稳定 B.高聚氮晶体属于原子晶体 C.高聚氮晶体中n(N)∶n(N-N)=1∶3 D.用作炸药或高能材料可能是高聚氮潜在的应用 5、下列各组离子能在指定环境中大量共存的是 A.在c(HCO3-)=0.1mol/L的溶液中:NH4+、Al3+、Cl-、NO3- B.在由水电离出的c(H+)=1×10-12mol/L的溶液中:Fe2+、ClO-、Na+、SO42- C.pH=1的溶液中:Mg2+、Fe3+、NO3-、[Ag(NH3)2]+ D.在使红色石蕊试纸变蓝的溶液中:SO32-、CO32-、Na+、K+ 6、某一胶体进行电泳实验时,胶体微粒向阴极移动,对胶体进行下列操作时,能使胶体发生凝聚的是①加入酒精;②加入MgSO4溶液;③加入Fe(OH)3溶胶;④加入H2SiO3溶胶;⑤降低温度 A、②③ B、②④ C、①③ D、①⑤ 7、高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强,无二次污染的绿色处理剂。工业是先制得高铁酸钠,然后在低温下,在高铁酸钠溶液中加入KOH至饱和就可析出高铁酸钾(K2FeO4)。湿法制备的主要反应方程为: 2Fe(OH)3+3ClO-+4OH--→2FeO42-+3Cl-+5H2O 干法制备的主要反应为:2FeSO4+6Na2O2-→2Na2FeO4+2Na2O+2Na2SO4+O2↑ 下列有关说法不正确的是 A.高铁酸钾中铁显+6价 B.湿法中每生成1 mol Na2FeO4转移3 mol电子 C.干法中每生成1 mol Na2FeO4转移4 mol电子 D.K2FeO4处理水时,不仅能消毒杀菌,还能除去水体中的H2S、NH3等,生成的Fe(OH)3还能吸附水中的悬浮杂质 8、从下列事实所列出的相应结论正确的是
|
|
实 验 事 实 |
结 论 |
|
① |
Cl2的水溶液可以导电 |
Cl2是电解质 |
|
② |
将燃烧的镁条放入CO2中能继续燃烧 |
还原性:Mg>C |
|
③ |
NaHCO3溶液与Na[Al(OH)4]溶液混合产生白色沉淀 |
酸性:HCO3->Al(OH)3 |
|
④ |
常温下白磷可自燃而氮气须在放电时才与氧气反应 |
非金属性:P>N |
|
⑤ |
某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 |
该溶液一定有NH4+ |
A.③④⑤ B.②③⑤ C.①②③
D.全部
9、下列离子方程式正确的是
A、溴化亚铁溶液中通入过量氯气:2Fe2++4Br-+3Cl2-→2Fe3++2Br2+6Cl-
B、实验室用MnO2和浓盐酸制取Cl2:MnO2+4HCl(浓) Mn2++Cl2↑+2Cl-+2H2O
C、用FeS除去工业废水中含有的Cu2+:S2-(aq)+Cu2+(aq) -→ CuS(s)↓
D、1L0.5mol·L-1稀硫酸与1L1mol·L-1氢氧化钠溶液反应放出57.3kJ的热量:
H2SO4(aq)+2NaOH(aq)-→Na2SO4(aq)+2H2O(1)+57.3 kJ·mol-1
10、A和B两元素分别得到两个电子后,都变成零族元素的电子层结构,其中A放出的能量比B大,因此
A、A比B容易被还原
B、A2-的还原性比B2-的强
C、A的氧化性比B弱
D、A2-比B2-的半径大
Mn2++Cl2↑+2Cl-+2H2O
C、用FeS除去工业废水中含有的Cu2+:S2-(aq)+Cu2+(aq) -→ CuS(s)↓
D、1L0.5mol·L-1稀硫酸与1L1mol·L-1氢氧化钠溶液反应放出57.3kJ的热量:
H2SO4(aq)+2NaOH(aq)-→Na2SO4(aq)+2H2O(1)+57.3 kJ·mol-1
10、A和B两元素分别得到两个电子后,都变成零族元素的电子层结构,其中A放出的能量比B大,因此
A、A比B容易被还原
B、A2-的还原性比B2-的强
C、A的氧化性比B弱
D、A2-比B2-的半径大
3、下列过程中属于化学变化的是
①白色的硫酸铜粉末久置于空气中变成蓝色 ②同素异形体之间的互变
③福尔马林用来浸制标本 ④同分异构体之间的互变
⑤乳酸聚合成的纤维降解 ⑥氯化钠溶液通电后导电
A.只有①②④⑤ B.①②③④⑤⑥ C.只有③④⑤ D.只有①④⑤
2、简单原子的原子结构可用下图形象地表示:
 其中“●”表示质子或电子,“○”表示中子,则下列有关①②③的叙述正确的是
A.①②③互为同素异形体 B.①②③互为同位素
C.①②③是三种化学性质不同的粒子
D.①②③具有相同的质量数
其中“●”表示质子或电子,“○”表示中子,则下列有关①②③的叙述正确的是
A.①②③互为同素异形体 B.①②③互为同位素
C.①②③是三种化学性质不同的粒子
D.①②③具有相同的质量数
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com