
题目列表(包括答案和解析)
24.(1) ____ _____ (2) _______ _____;
(3) __ ____ ; ;
(4)
23.(1)___________ ;____________ ___________
(2)① _______ _________② ________
22. (1) , ;
(2) ;
。
21.(1) ① ② ______________ ____ _____ ____________;
③ ;④________________;
(2) ;
(3)____ _______;
20. (1) _____________________________________;(2)
(3) ________ _______ ______________; ; ;
(4)
19.(1) (2)① ;
② ; ;
③ ④
26.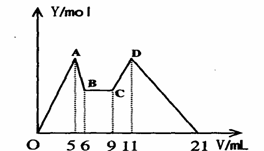 (7分)某溶液含 Mg2+、Al3+,向其中滴加a mLC1mol·L-1NaOH之后,改成滴加C2mol·L-1H2SO4溶液,所得沉淀Y(mol)与所加试剂总体积V(mL)间的关系如右图所示。据此,回答下列问题:
(7分)某溶液含 Mg2+、Al3+,向其中滴加a mLC1mol·L-1NaOH之后,改成滴加C2mol·L-1H2SO4溶液,所得沉淀Y(mol)与所加试剂总体积V(mL)间的关系如右图所示。据此,回答下列问题:
(1)C-D过程中的离子方程式 ;
(2)n(Mg2+)/ n(Al3+) = ;
(3)C1/C2= ;
(4)所加入NaOH溶液的体积a= mL。
可能用到的原子量:H-1 C-12 N-14 O-16 Na-23 S-32 P-31 Mg-24 Al-27 Cl-35.5 K-39 Fe-56
25.(7分)科学家对H2O2结构的认识经历了较为漫长的过程,最初,科学家提出了两种观点: ①H-O-O-H、② 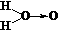 。式中O→O表示配位键,即共用电子对由某原子单方面提供(已知在化学反应中氧氧键遇到还原剂时易断裂)。
。式中O→O表示配位键,即共用电子对由某原子单方面提供(已知在化学反应中氧氧键遇到还原剂时易断裂)。
化学家Baeyer和Villiyer为研究H2O2的结构,设计并完成了下列实验:
a.将C2H5OH与浓H2SO4反应,生成(C2H5)2SO4和水;
b.将制得的(C2H5)2SO4与H2O2反应,只生成A和H2SO4;
c.将生成的A与H2反应(已知该反应中H2作还原剂)。
(1)用电子式表示①、②两种结构:①_________________、②________________。
(2)如果H2O2的结构如①所示,实验c中化学反应方程式为(A写结构简式,下同)___________________________________________________________________;假如H2O2的结构如②所示,实验c中化学反应方程式为
___________________________________________________________________。
(3)为了进一步确定H2O2的结构,还需要在实验c后添加一步实验d,请设计d的实验方案:___________________________________________________________。
24.(7分)某无色溶液X,由Na+、Ag+、Ba2+、Al3+、AlO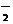 、MnO
、MnO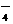 、CO
、CO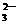 、SO
、SO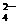 中的若干种离子组成,取溶液进行如下连续实验:
中的若干种离子组成,取溶液进行如下连续实验:
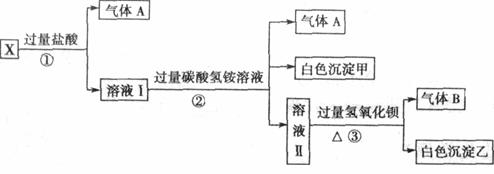
(1)白色沉淀甲是 _________。
(2)X溶液中一定存在的离子是_____________。
(3)白色沉淀乙中一定有:______ ,可能有 证明其是否存在的方法是 。
(4)若将过量的气体A与适量的气体B通入水中,写出反应的离子方程式
23.(6分)化学反应中的能量变化,是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同所致。下图为N2(g)和O2(g)生成NO(g)过程中的能量变化
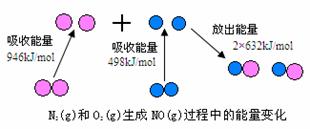
(1)人们通常把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,则N≡N的键能为___________ kJ/mol,由上图写出N2(g)和O2(g)生成NO(g)的热化学反应方程式_______________________
(2)1840年,俄国化学家盖斯在分析了许多化学反应热效应的基础上,总结出一条规律:“一个化学反应,不论是一步完成,还是分几步完成,其总的热效应是完全相同的。”这个规律被称为盖斯定律。有些反应的反应热虽然无法直接测得,但可以利用盖斯定律间接计算求得。
①根据下列反应的热化学反应式,计算由C(石墨)和H2(g)反应生成1mol C2H2(g)的△H。
C(石墨) + O2(g) = CO2(g);△H1 = - 393.5 kJ/mol
2H2(g) + O2(g) = 2H2O(l);△H2 = - 571.6 kJ/mol
2C2H2(g) + 5 O2(g) = 4CO2(g) + 2H2O(l);△H3 = - 2599.2 kJ/mol,则由C(石墨)和H2(g)反应生成1mol C2H2(g)的△H _______________________ kJ/mol。
②已知3.6 g碳在6.4 g的氧气中燃烧,至反应物耗尽,并放出X kJ热量。已知单质碳的燃烧热为Y kJ/mol,则1mol C与O2反应生成CO的反应热△H为_________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com