
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
11.ТШЦјИњЕтдкМгШШЬѕМўЯТЃЌвдЕШЮяжЪЕФСПНјааЗДгІЃЌПЩЕУЕНвЛжжКьзиЩЋвКЬхIClЁЃIClгаКмЧПЕФбѕЛЏадЃЌIClИњZnЁЂH2OЗДгІЕФЛЏбЇЗНГЬЪНЮЊЃК2ICl+2Zn===ZnCl2+ZnI2 ЁЁЁЁЁЁICl+H2O===HCl+HIO
ЯТСаа№Ъіжае§ШЗЕФЪЧ
A.ZnCl2МШЪЧбѕЛЏВњЮяЃЌгжЪЧЛЙдВњЮяЁЁ B.IClИњH2OЕФЗДгІЪЧздЩэбѕЛЏЛЙдЗДгІЁЁ
C.ZnI2МШЪЧбѕЛЏВњЮяЃЌгжЪЧЛЙдВњЮяЁЁ D.дкIClИњH2OЕФЗДгІжаЃЌIClЪЧбѕЛЏМСЃЌH2OЪЧЛЙдМС
10ЃЎвбжЊЃКNaAЕФЫЎШмвКГЪМюадЁЃГЃЮТЯТНЋЕШЬхЛ§ЕФ0.10mol/L NaAШмвК гы0.05mol/L HClШмвКЛьКЯЃЌЫљЕУШмвКpH < 7ЁЃОнДЫХаЖЯвдЯТЙиЯЕЪНВЛГЩСЂЕФЪЧ
AЃЎc(Cl‾ ) + c(OH‾ ) + c(A‾) > c(Na+ )ЁЁЁЁ
BЃЎc(Na+ ) > c(A‾ ) > c(H+ ) > c(OH‾ )
CЃЎc(A‾ ) + c(HA) = c(Na+ )ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
DЃЎc(A‾ ) > c(Na+ ) >c(H+ ) > c(OH‾ )
9ЃЎЯТСаЪЕбщВйзїЃЌе§ШЗЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁAЃЎжаКЭЕЮЖЈЪБЃЌгУБъзМвКШѓЯДЕЮЖЈЙмЃЌгУД§ВтвКШѓЯДзЖаЮЦПЃЌВЂЕЮШыl mLжИЪОМС
BЃЎХфжЦЮяжЪЕФСПХЈЖШШмвКЪБЃЌНЋГЦСПКУЕФШмжЪШмгкЪЂгаЪЪСПЫЎЕФЩеБжаЃЌШмНтКѓСЂМДЧуШыШнСПЦПжаЃЌМЬајНјааЯДЕгКЭЖЈШн
CЃЎжЦШЁFe(OH)2ЪБЃЌЮќШЁNaOHШмвКЕФНКЭЗЕЮЙмЕФФЉЖЫгІВхШыFeSO4ШмвКжаЃЌдйЛКЛКНЋNaOHШмвКМЗГі
DЃЎфхввЭщКЭЩеМюШмвКЙВШШКѓЃЌНЋЯѕЫсвјШмвКЕЮШыЫЎНтвКжаЃЌМДПЩМћЕНЕЛЦЩЋГСЕэ
8.ЁЁ ЯжгаДјЛюШћЕФУмБеШнЦїAКЭBЃЌвЛЖЈЮТЖШЪБШнЦїAзАШыЕтЛЏЧтЦјЬхЁЂШнЦїBзАШыЖўбѕЛЏЕЊЦјЬхЃЌЪЙЦфЬхЛ§ЯрЕШЁЃЕБЮТЖШВЛБфЪБЃЌЛКЛКбЙЫѕСНШнЦїЃЌЪЙСНШнЦїЕФбЙЧПОљЮЊдРДЕФ4БЖЃЌДЫЪБСНШнЦїФкЦјЬхЕФЬхЛ§ЙиЯЕе§ШЗЕФЪЧ(ЫљгаЮяжЪЪМжеЮЊЦјЬЌ)
AЃЎA=BЁЁЁЁЁЁЁЁЁЁ BЃЎA<BЁЁЁЁЁЁЁЁ CЃЎЮоЗЈХаЖЯЁЁЁЁЁЁЁЁ DЃЎA>B
7. ЩшNAБэЪОАЂЗќМгЕТТоГЃЪ§ЃЌЯТСаа№Ъіжае§ШЗЕФЪЧЁЁ
AЃЎГЃЮТГЃбЙЯТЃЌ11.2LбѕЦјЫљКЌЕФдзгЪ§ЮЊNAЁЁ BЃЎ1.7gЕФNH+4РызгжаКЌгаЕФЕчзгЪ§ЮЊNA
CЃЎГЃЮТГЃбЙЯТЃЌ48gO3КЌгаЕФбѕдзгЪ§ЮЊ3NAЁЁ DЃЎ2.4gН№ЪєУОБфЮЊУОРызгЪБЪЇШЅЕФЕчзгЪ§ЮЊ0.1NA
6ЃЎЛЏбЇгУгяЪЧбЇЯАЛЏбЇЕФживЊЙЄОпЁЃЯТСагУРДБэЪОЮяжЪБфЛЏЕФЛЏбЇгУгяжаЃЌДэЮѓЕФЪЧЁЁ
AЃЎИжЬњИЏЪДЪБПЩФмЗЂЩњЕФе§МЋЗДгІЃК2H2O + O2 + 4e- = 4OH-
BЃЎБэЪОH2ШМЩеШШЕФШШЛЏбЇЗНГЬЪНЃК2H2(g)+O2(g)=2H2O(g)ЃЛЁїH=-483.6kJ/mol
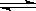 CЃЎДПМюЫЎНтЕФРызгЗНГЬЪНЃКCO32- + H2OЁЁЁЁЁЁЁЁ HCO3-
+ OH-
CЃЎДПМюЫЎНтЕФРызгЗНГЬЪНЃКCO32- + H2OЁЁЁЁЁЁЁЁ HCO3-
+ OH-
DЃЎCa(HCO3)2ШмвКжаМгШыЙ§СПГЮЧхЪЏЛвЫЎЃКCa2++HCO3Ѓ+OHЃ=CaCO3Ё§+H2O
5ЃЎФГЮоЩЋЭИУїШмвКФмгыТСЗлЗДгІЗХГіH2ЃЌдђДЫШмвКжавЛЖЈФмДѓСПЙВДцЕФРызгзщЮЊЁЁ
AЃЎOH-ЁЂNa+ЁЂK+ЁЂMnO4-ЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁBЃЎH+ЁЂCl-ЁЂBa2+ЁЂNO3-
CЃЎK+ЁЂCl-ЁЂNa+ЁЂSO42-ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎNH4+ЁЂMg2+ЁЂCl-ЁЂHCO3-
4.ЯТСаЗжЩЂЯЕжаЪЧНКЬхЕФЮЊ
AЁЁ дкЕтЛЏМиШмвКжаМгШыЙ§СПЕФЯѕЫсвјШмвКЃЌБпЕЮШыБпеёЕД
BЁЁ дкЕтЛЏМиЯЁШмвКжаМгШыЩйСПЕФЯѕЫсвјШмвКЃЌБпЕЮШыБпеёЕДЁЁЁЁ
CЁЁ НЋесЬЧЗХШыЫЎжаВЂеёЕДЁЁЁЁЁЁЁЁ DЁЁ НЋЛЈЩњгЭЗХШыЫЎжаВЂеёЕД
3. ЯТСаЫЕЗЈе§ШЗЕФЪЧ
AЃЎгЩгкH2OЗжзгМфДцдкЧтМќЃЌЫљвдH2OБШH2SЮШЖЈЁЃ
BЃЎ11.2 L O2КЭCO2ЕФЛьКЯЦјЬхжаКЌга6.02ЁС1023ИібѕдзгЁЃ
CЃЎЙЬЬЌNaClВЛЕМЕчЃЌЪЧгЩгкNaClОЇЬхжаВЛДцдквѕЁЂбєРызгЁЃ
DЃЎПЩФцЗДгІДяЦНКтзДЬЌКѓЃЌЛЏбЇЗДгІЫйТЪЗЂЩњБфЛЏЃЌЦНКтВЛвЛЖЈвЦЖЏЁЃ
2. ЫЎЕФзДЬЌГ§СЫЦјЁЂвККЭЙЬЬЌЭтЃЌЛЙгаВЃСЇЬЌЁЃЫќЪЧгЩвКЬЌЫЎМБЫйРфШДЕН165 KЪБаЮГЩЕФЃЌВЃСЇЬЌЕФЫЎЮоЙЬЖЈаЮзДЃЌВЛДцдкОЇЬхНсЙЙЃЌЧвУмЖШгыЦеЭЈвКЬЌЫЎЕФУмЖШЯрЭЌЃЌгаЙиВЃСЇЬЌЫЎЕФа№Ъіе§ШЗЕФЪЧ
A.ЫЎгЩвКЬЌБфЮЊВЃСЇЬЌЃЌЬхЛ§ЫѕаЁЁЁЁЁ B.ЫЎгЩвКЬЌБфЮЊВЃСЇЬЌЃЌЬхЛ§ХђеЭЁЁ
C.ВЃСЇЬЌЪЧЫЎЕФвЛжжЬиЪтзДЬЌЁЁЁЁЁЁЁЁ D.ВЃСЇЬЌЫЎЪЧЗжзгОЇЬх
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com