
题目列表(包括答案和解析)
21.(7分)常温下将0.01 mol NH4Cl和0.002 mol NaOH溶于水配成1L溶液,
(1)该溶液中存在的___________个平衡体系;
(2)溶液中共有___________种不同的粒子;
(3)这些粒子中浓度为0.01 mol·L-1的是____________ ,浓度为0.002 mol·L-1的是______________;
(4)物质的量之和为0.01 mol 的两种粒子是____________________;
(5)_________和__________两种粒子数量之和比OH-多0.008 mol。
20. (7分)已知FeSO4·7H2O晶体在加热条件下发生如下反应:
2FeSO4·7H2O Fe2O3 + SO2↑+SO3↑+14H2O↑;下图的装置可用来检验上述反应中所有的气体产物,请回答下列问题:
Fe2O3 + SO2↑+SO3↑+14H2O↑;下图的装置可用来检验上述反应中所有的气体产物,请回答下列问题:

(1)用于检验SO2气体的装置是 (填装置的字母),确认水蒸气存在的现象是 ;
(2)利用装置B可以确认的产物是 ,装置B中的甲溶液可选(填序号) ,
①足量澄清石灰水 ②足量氯化钡溶液 ③足量硝酸钡溶液
该装置中冷水的作用是 ;
(3)为探究Fe2O3的性质和用途,取试管中少许固体溶于适量盐酸中制备饱和铁盐溶液,将此饱和溶液逐滴加入沸水中加热片刻,观察液体的颜色变为 ,检验该分散系的最简方法为 。
19.(4分)化合物BrFx与水按物质的量之比为3∶5发生反应,其产物为溴酸、氢氟酸、单质溴和氧气。
(1)BrFx中,x= 。
(2)该反应的化学方程式是 。
(3)此反应中的氧化剂是_________和还原剂是_________。
18. (2分)周期表前20号元素中,某两种元素的原子序数相差3,周期数相差1,它们形成化合物时原子数之比为1:2。写出这些化合物的化学式 。
17. (2分)现有某种不溶于水的金属氧化物,如要判别它是酸性氧化物、碱性氧化物还是两性氧化物,其方法是 。
16.(2分)分别设计实验,用最佳方法证明明矾溶于水时发生的下列变化:
供选用的药品和仪器:明矾溶液、甲基橙试液、石蕊试液、酚酞试液、pH试纸、氢氧化钠溶液、酒精灯、半透膜、电泳仪、聚光束仪
(1)证明明矾溶于水发生了水解反应_______________;
(2)证明明矾的水解反应是一个吸热反应_______________;
15. 气体X可能含有Cl2、HBr、CO2中的一种或几种,已知X通入AgNO3溶液时产生淡黄色沉淀,且沉淀不溶于稀硝酸;若将X通入澄清的石灰水中,却不见沉淀产生.对于气体X的成分,下列说法正确的是
A.一定含有HBr,可能含有CO2 B.一定不含CO2
C.一定不含Cl2和CO2 D.可能含有CO2和Cl2
第II卷(非选择题,共55分)
14.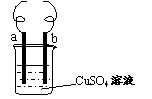 用铁丝(电极a)、铜丝(电极b)和CuSO4溶液可以构成原电池或电解池,如右图所示。则下列说法正确的是
用铁丝(电极a)、铜丝(电极b)和CuSO4溶液可以构成原电池或电解池,如右图所示。则下列说法正确的是
A.构成原电池时b极反应为: Cu﹣2e-=Cu2+
B.构成电解池时a极质量一定减少
C.构成电解池时b 极质量可能减少也可能增加
D.构成的原电池或电解池工作后就可能产生大量气体
13.HPE是合成除草剂的重要中间体,其结构简式如下图所示。下列有关HPE的说法正确的是
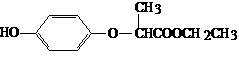 A.HPE不能跟浓溴水反应
A.HPE不能跟浓溴水反应
B.1molHPE最多可以和2mol NaOH反应
C.HPE在核磁共振氢谱中有6个峰
D.HPE分子中有2个手性碳原子
12.短周期元素X、Y、Z,其中X、Y位于同一主族,Y、Z位于同一周期。X原子的最外层电子数是其电子层数的3倍,Z原子的核外电子数比Y原子少1。下列比较正确的是
A. 气态氢化物的稳定性:Z < Y < X B.最高价氧化物水化物酸性:Z > Y
C. 原子半径:Z < Y < X D. 元素非金属性:Z> Y > X
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com