
题目列表(包括答案和解析)
8.设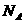 表示阿伏加德罗常数,下列叙述中正确的是
表示阿伏加德罗常数,下列叙述中正确的是
①.31g白磷含有的P-P键数为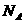 ②. 1mol
②. 1mol (碳正离子)中含有电子数为10
(碳正离子)中含有电子数为10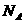 ③. 1mol铜与足量硫蒸气反应,转移电子数为2
③. 1mol铜与足量硫蒸气反应,转移电子数为2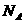 ④.1mol Mg与足量O2或N2反应生成MgO或Mg3N2,均失去2
④.1mol Mg与足量O2或N2反应生成MgO或Mg3N2,均失去2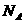 个电子 ⑤.用惰性电极电解CuCl2溶液,阴极析出16g铜时,线路中通过的电子数为NA
⑥.0.84 g
个电子 ⑤.用惰性电极电解CuCl2溶液,阴极析出16g铜时,线路中通过的电子数为NA
⑥.0.84 g 晶体中阳离子和阴离子总数为0.03
晶体中阳离子和阴离子总数为0.03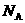 ⑦.3.9gNa2O2吸收足量的CO2时转移的电子数是0.05NA
⑧.标准状况下,3.2g铜与足量的浓硝酸反应生成的气体含有的分子数是0.1NA ⑨.28 g C16O与28 g C18O中含有的质子数均为14×6.02×1023
⑩.标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为2×6.02×1023
⑦.3.9gNa2O2吸收足量的CO2时转移的电子数是0.05NA
⑧.标准状况下,3.2g铜与足量的浓硝酸反应生成的气体含有的分子数是0.1NA ⑨.28 g C16O与28 g C18O中含有的质子数均为14×6.02×1023
⑩.标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为2×6.02×1023
A ②④⑦⑧ B ③④⑥⑦⑧ C ④⑦ D④⑥⑨⑩
7.下列各溶液中,各粒子的物质的量浓度关系正确的是
A.0.1mol/LNa2CO3溶液中:c(Na+) + c(H+) = c(CO32-) + c(HCO3-) + c(OH-)
B.0.1mol/L(NH4)2SO4溶液中:c(SO42-) > c(NH4+) > c(H+) > c(OH-)
C.0.1mol/LNaHCO3溶液中:c(OH-) = 2c(H2CO3) + c(HCO3-) + c(H+)
D.0.1mol/LNa2S溶液中:c(Na+) = 2c(S2-) +2c(HS-) + 2c(H2S)
6、三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:
3 NF3 + 5 H2O = 2 NO + HNO3 + 9 HF。下列有关该反应的说法正确的是
A.NF3是氧化剂,H2O是还原剂 B.还原剂与氧化剂的物质的量之比为2:1
C.若生成0.2 mol HNO3,则转移0.2 mol电子 D.NF3在潮湿的空气中泄漏会产生红棕色气体
5、已知常温下可用Co2O3制备Cl2,反应前后存在六种微粒:Co2O3﹑H2O﹑Cl2、H+ 、Cl-和Co2+ 。下列叙述不正确的是
A.氧化产物为Cl2 B.氧化剂与还原剂的物质的量之比为1∶2
C.若有3mol H2O生成,则反应中有2mol电子转移
D.当该反应生成2.24L Cl2时,则反应中有0.1mol电子转移
4、设某元素某原子核内的质子数为m,中子数为n,则下述论断正确的是
(A)不能由此确定该元素的原子量 (B)这种元素的原子量为m+n
(C)若碳原子质量为W克,此原子的质量为(m+n)W克 (D)核内中子和质子共同决定元素种类
3、Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1:16,则x值是
A.2 B.3 C.4 D.5
2、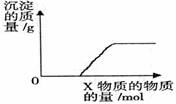 将溶液(或气体)X逐渐加入(或通入)到一定量Y溶液中,产生沉淀的质量与加入X的物质的量关系如右图,符合图中情况的一组物质是
将溶液(或气体)X逐渐加入(或通入)到一定量Y溶液中,产生沉淀的质量与加入X的物质的量关系如右图,符合图中情况的一组物质是
|
|
(A) |
(B) |
(C) |
(D) |
|
X |
Ba(HCO3)2 溶液 |
Na2CO3 溶液 |
KOH 溶液 |
CO2 气体 |
|
Y |
NaOH 溶液 |
CaCl2 溶液 |
Mg(HSO4)2 溶液 |
石灰水 |
1、下列有关物质分类或归类正确的是
①混合物:石炭酸、福尔马林、水玻璃、水银 ②化合物:CaCl2、烧碱、聚苯乙烯、HD
③电解质:明矾、胆矾、冰醋酸、硫酸钡 ④同系物: CH2O2、C2H4O2、C3H6O2、C4H8O2
⑤有机物:酒精、 油脂、蔗糖、蛋白质
A.①③④ B.②④ C.②③④ D.③⑤
25.(11分)有一混合气体,可能由H2、O2、NH3、N2、CO2、HCl和He中的两种或多种组成。常温下,取此气体200mL进行实验,实验的过程和结果如下:
(1)观察此混合气体为无色。
(2)将此气体通过浓H2SO4,气体体积减少了40mL。
(3)将(2)中剩余的气体,通过Na2O2固体,气体体积变为120mL。
(4)将(3)中剩余的气体引燃充分反应后,冷却至常温,气体体积又减少了105mL。
(5)又将(4)中剩余的气体通过炽热的铜网,气体的体积又减少了三分之一(上述气体的体积都是相同条件下测定的)。
根据上述实验,试推断:
(1)混合气体中肯定存在的气体是 ,它们的体积分别为
。
(2)混合气体中肯定不存在的气体是 。
(3)混合气体中可能含有的气体是 ,其体积共为
。
24.(11分)海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
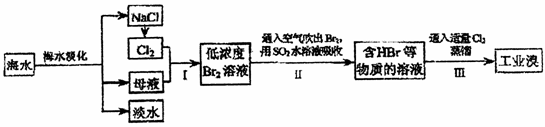
(1)从海水中可以得到食盐。为了除去粗盐中的Ca2+、Mg2+、SO2-4及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤,②加过量NaOH溶液,③加适量盐酸,④加过量NaCO3溶液,⑤加过量BaCl2溶液。正确的操作顺序是 。
A.①④②⑤③ B.④①②⑤③ C.②⑤④①③ D.②④⑤①③
(2)电解 NaCl溶液是氯碱工业的核心反应,请写出其化学方程式
。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为 。
(4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为
,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是 。
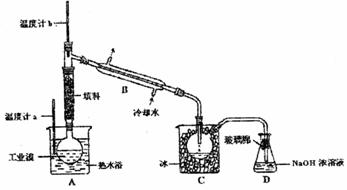 (5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,绘制了如右装置简图,请你参与分析讨论:
(5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,绘制了如右装置简图,请你参与分析讨论:
①整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是
。
②实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件:
。
③C中液体产生颜色为 。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com