
题目列表(包括答案和解析)
18、常温下,对下列四种溶液的叙述正确的是
|
|
① |
② |
③ |
④ |
|
pH |
10 |
10 |
4 |
4 |
|
溶液 |
氨水 |
氢氧化钠溶液 |
醋酸溶液 |
盐酸 |
A.四种溶液分别加水稀释10倍,pH变化最大的是①和④
B.②、④两溶液相比,两者的kw相同
C.①、②、③中分别加入少量的醋酸铵固体后,三种溶液的pH均减小
D.①、④ 两溶液按一定体积比混合,所得溶液中离子浓度顺序一定为:
c(NH4+)>c(Cl-)>c(H+)> c(OH-)
17、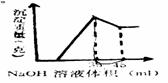 准确称取6克铝土矿样品(含Al2O3、Fe2O3、SiO2)加入100mL硫酸溶液,充分反应后,向滤液中加入10mol/L NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,求所用硫酸溶液的物质的量浓度
准确称取6克铝土矿样品(含Al2O3、Fe2O3、SiO2)加入100mL硫酸溶液,充分反应后,向滤液中加入10mol/L NaOH溶液,产生沉淀的质量与加入NaOH溶液的体积关系如图所示,求所用硫酸溶液的物质的量浓度
A 1.75 mol/L B 3.5 mol/L
C 2.25 mol/L D无法计算
16、 往一体积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g) 2HI(g);△H<0,当达到平衡后,t0时改变反应的某一条件,平衡图像如下,则下列说法正确的是
往一体积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g) 2HI(g);△H<0,当达到平衡后,t0时改变反应的某一条件,平衡图像如下,则下列说法正确的是
A.容器内气体颜色变深,平均相对分子质量不变 B.平衡不移动,混合气体密度增大
C.H2转化率增大,HI平衡浓度变小 D.t0时改变的条件是增压
15、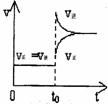 用pH大小表示溶液的酸碱性相对强弱有许多不足之处。因此,荷兰科学家Henk Van Lubeck引入了酸度(AG)的概念,即把电解质溶液中的酸度定义为c(H+)与c(OH一)比值的对数,用公式表示为AG=lg [c(H+)/c(OH一)] 。常温下,在AG=10的溶液中能大量共存的离子是:
用pH大小表示溶液的酸碱性相对强弱有许多不足之处。因此,荷兰科学家Henk Van Lubeck引入了酸度(AG)的概念,即把电解质溶液中的酸度定义为c(H+)与c(OH一)比值的对数,用公式表示为AG=lg [c(H+)/c(OH一)] 。常温下,在AG=10的溶液中能大量共存的离子是:
A.Ca2+、K+、Cl-、SO32- B.NH4+、Fe2+、 I一、SO42-
C.Na+ 、K+、ClO-、S2- D.Na+、S2O32-、AlO2-、K+
14、对于某酸性溶液(可能含有Br –、SO42 –、H2SO3、NH4+),分别进行如下实验: ①加热时放出的气体可使品红溶液褪色;②加入碱溶液使溶液呈碱性,再加热时放出的气体可使湿润的红色石蕊试纸变蓝;③加入氯水时,溶液略呈橙红色,再加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀。对于下列物质不能确定其在原溶液中是否存在的是
A.Br – B.SO42– C.H2SO3 D.NH4+
13、 一定条件下,可逆反应X(g) + 3Y(g) 2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0,单位mol/L),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判断不合理的是
一定条件下,可逆反应X(g) + 3Y(g) 2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0,单位mol/L),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判断不合理的是
A.c1:c2 = 1:3 B.平衡时,Y和Z的生成速率之比为3:2
C.X、Y的转化率不相等 D.c1的取值范围为0 < c1 < 0.14mol/L
12、下列离子方程式书写正确的是
①.等体积等物质的量浓度的氢氧化钡稀溶液与碳酸氢铵稀溶液混合
Ba2+ + 2OH – + NH4+ + HCO3 – = BaCO3↓+ NH3·H2O + H2O
②.氯化铝溶液中加入过量的氨水 Al3+ + 4NH3·H2O = 4NH4+ + AlO2 – + 2H2O
③.向次氯酸钙溶液中通入过量的二氧化硫 Ca2+ + 2ClO – + SO2 + H2O = CaSO3↓+ 2HClO
④.已知等浓度的碳酸钠、次氯酸钠、碳酸氢钠PH逐渐减小,向次氯酸钠溶液通少量二氧化碳 ClO- +CO2 +H2O = HClO + CO32-
⑤.过氧化钠固体与水反应:2O22‾+2H2O=4OH‾+O2↑
⑥.氨水中通入过量二氧化硫:2NH3•H2O + SO2 = 2NH4+ +SO32‾ +H2O
⑦.澄清的石灰水中加人过量的NaHCO3溶液:Ca2++OH‾+HCO3‾=CaCO3↓+H2O
⑧.将2mol/LAlCl3溶液和7mol/LNaOH溶液等体积混合:
2Al3++7OH‾=Al(OH)3↓+AlO2‾+2H2O
⑨、向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:Ba2+ + 2OH- + 2H+ + SO42- = BaSO4↓+ 2H2O
A ①③⑥⑨ B②④⑤⑨ C③④⑦⑧ D①⑧⑨
11、某无色透明溶液能与铝粉反应放出H2,则此溶液中一定能大量共存的离子组为
A.OH-、Na+、K+、MnO4- B.H+、Cl-、Ba2+、NO3-
C.K+、Cl-、Na+、SO42- D.NH4+、Mg2+、Cl-、HCO3-
10、实验室将NaClO3和Na2SO3按物质的量为2:1放入烧杯中,同时滴入适量H2SO4,并用水浴加热,产生棕黄色的气体X,反应后测得NaClO3和Na2SO3恰好完全反应,则X的化学式为
A.Cl2 B.Cl2O C.ClO2 D.Cl2O3
9、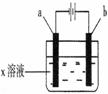 如右图所示,下列实验现象的描述正确的是
如右图所示,下列实验现象的描述正确的是
|
|
a电极 |
b电极 |
x溶液 |
实 验 现 象 |
|
A |
石墨 |
石墨 |
CuCl2 |
a极质量增加,b极放出无色气体 |
|
B |
Fe |
石墨 |
KNO3 |
a极质量增加,b极放出无色气体 |
|
C |
Fe |
Cu |
CuSO4 |
a极质量增加,b极质量减少 |
|
D |
石墨 |
石墨 |
HCl |
a极放出无色气体,b极放出无色气体 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com