
题目列表(包括答案和解析)
8.用1 L 1.0 mol / L NaOH溶液吸收0.8 mol CO2,所得溶液中的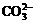 和
和 的浓度之比约是 (
)
的浓度之比约是 (
)
A. 1∶3 B.1∶2 C.2∶3 D.3∶2
7.等物质的量的过氧化钠与碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是( )
A.Na2CO3 B.NaOH Na2CO3
C.Na2O2 Na2CO3 D.Na2O2 NaOH Na2CO3
6.下列离子方程式书写正确的是 ( )
A.碳酸氢铵和足量的氢氧化钠溶液反应:NH4++OH- NH3↑+H2O
B.向氯化亚铁溶液中滴加新制氯水:Fe2++Cl2 Fe3++2Cl-
C.向次氯酸钠溶液中通人少量SO2:2ClO-+SO2+H2O 2HClO+SO32-
D.向FeCl 3溶液中滴加过量NaOH溶液:Fe3++3OH-=Fe(OH)3↓
5.下列实验设计及其对应的离子方程式均正确的是 ( )
A.用FeCl3溶液腐蚀铜线路板:Cu + 2Fe3+ = Cu2+ + 2Fe2+
B.Na2O2与H2O反应制备O2 :Na2O2 + H2O = 2Na+ + 2OH- + O2↑
C.将氯气溶于水制备次氯酸:Cl2 + H2O = 2H+ + Cl- + ClO-
D.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:
2MnO + 6H+ +
5H2O2 = 2Mn2+ + 5O2↑ + 8H2O
+ 6H+ +
5H2O2 = 2Mn2+ + 5O2↑ + 8H2O
4.下列各组离子在指定溶液中能大量共存的是 ( )
①无色溶液中: K+、Cu2+、Na+、SO42-
②pH=11的溶液中:CO32-、Na+、AlO2-、NO3-
③加入Al能放出H2的溶液中:Cl-、HCO3-、NO3-、NH4+
④在由水电离出的c(OH-)=10-13mol·L-1的溶液中:Na+、Ba2+、Cl-、I-
⑤能使pH试纸变为蓝色的溶液:Na+、C1-、S2-、ClO-
⑥酸性溶液中:Fe2+、Al3+、NO3-、Cl-
A.①②⑤ B.③⑤⑥ C.②④ D.②④⑥
3.下列说法都正确的是( )
①江河入海口三角洲的形成通常与胶体的性质有关
②蔗糖、硫酸钡和纯碱分别属于非电解质、弱电解质和强电解质
③用玻璃棒搅拌漏斗中的液体以加快过滤速度
④在容量瓶中加入一体积的水,再加入浓硫酸配制准确浓度的稀硫酸
⑤常用的自来水消毒剂有氯气和二氧化氯,氯气的消毒效率低于二氧化氯。
A.②③⑤ B.②④ C.①⑤ D.①④
2.下列关于胶体的叙述正确的是( )
A.胶体粒子不能透过滤纸
B.胶体和溶液的本质区别是胶体能发生丁达尔现象
C.胶体带电,故在电场作用下会产生电泳现象
D.用渗析的方法净化胶体时,使用半透膜只能让小分子和离子通过
1.若NA表示阿伏加德罗常数的值,下列叙述正确的是( )
①标准状况下,2.24L四氯化碳含碳原子数为0.1NA
②标准状况下,a L的氧气和氮气的混合物含有的分子数为a/22.4 NA
③电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量减少64g
④7g CnH2n中含有的氢原子数为2NA
⑤常温下,7.1g氯气与足量的氢氧化钠溶液反应转移的电子数为0.1NA
⑥标况下22.4LNO和11.2LO2混合后所得气体分子数为NA
⑦ 2L1mol/L的盐酸中所含氯化氢分子数为2 NA
A.①④⑦ B.②⑤⑥ C.③④⑤ D.②⑤
35. (8分).C70分子是形如椭球状的多面体,该结构的建立基于以下考虑:
(8分).C70分子是形如椭球状的多面体,该结构的建立基于以下考虑:
(1)C70分子中每个碳原子只跟相邻的3个碳原子形成化学键;
(2)C70分子中只含有五边形和六边形;
(3)多面体的顶点数、面数和棱边数的关系遵循欧拉定理:顶点数+面数-棱边数=2。
根据以上所述确定:
(1)C70分子中所含的单键数和双键数;(2)C70分子中的五边形和六边形各有多少?
34.(5分)如图所示为高温超导领域里的一种化合物--钙钛矿 晶体结构,该结构是具有代表性的最小重复单位。

(1)在该物质的晶体结构中,每个钛离子周围与它最接近且距离相等的钛离子、钙离子各有 、 个。
(2)该晶体结构中,元素氧、钛、钙的离子个数比是 。该物质的化学式可表示为 。
(3)若钙、钛、氧三元素的相对质量分别为a,b,c,晶体结构图中正方体边长(钛原子之间的距离)为dnm(1nm=10-9m),则该晶体的密度为 g/cm3。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com