
题目列表(包括答案和解析)
16.(18分)某课外小组利用H2还原黄色的WO3粉末测定W的相对原子质量,下图是测定装置的示意图,A中的试剂是盐酸。

(1)仪器中装入的试剂:B______ ___ 、C_ _______、D_______ ____;
(2)连接好装置后应首先_________________________,
其方法是____________ ____
(3)“加热反应管E”和“从A瓶逐滴滴加液体”这两步操作应该先进行的是 ____________。在这两步之间还应进行的操作是____________________________;
(4)装置F的作用是____________ ,装置G的作用是___ __
15.(15分)实验室可由软锰矿(主要成分为MnO2)制备KMnO4,方法如下:软锰矿与过量固体KOH和KClO3在高温下反应,生成锰酸钾(K2MnO4)和KCl:用水溶解,滤去残渣,滤液酸化后,K2MnO4转变为MnO2和KMnO4;滤去MnO2沉淀,浓缩滤液,结晶得到深紫色的针状KMnO4。请回答:
(1)软锰矿制备K2MnO4的化学方程式是 ;
(2)KMnO4能与热的经硫酸酸化的Na2C2O4反应生成Mn2+和CO2该反应的离子方程式是 。
(3)若用2.5 g软锰矿(含MnO2 80%)进行上述实验,计算KMnO4的理论产量;
14.在a L Al2(SO4)3和(NH4)2SO4的混合溶液中加入b mol BaCl2,恰好使溶液中的SO 离子完全沉淀;如加入足量强碱并加热可得到c mol NH3气,则原溶液中的Al3+离子浓度(mol/L)为
离子完全沉淀;如加入足量强碱并加热可得到c mol NH3气,则原溶液中的Al3+离子浓度(mol/L)为
A.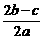 B.
B. C.
C.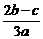 D.
D.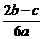
醴陵二中、醴陵四中2011届高三上学期期中考试联考
化学试卷答卷
第一卷:选择题(共42分)
第二卷:非选择题(共58分)
13.下列实验中能证明某气体为SO2的是
①使澄清石灰水变浑浊 ②使湿润的蓝色石蕊试纸变红 ③使品红溶液褪色 ④通入足量NaOH溶液中,再滴加BaC12溶液,有白色沉淀生成,该沉淀溶液于稀盐酸 ⑤通入溴水中,能使溴水退色,再滴加Ba(NO3)2溶液有白色沉淀产生
A.都能证明 B.都不能证明 C.③④⑤均能证明 D.只有⑤能证明
12.下列离子方程式表示正确的是
A.AgNO3 溶液中加入Cu :Cu+Ag+=Cu2++Ag
B.NaHCO3溶液中加入CH3COOH:CO32-+2CH3COOH=CO2↑+2CH3COO-+H2O
C.0.1mol FeBr2 溶液中通入足量Cl2 :2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
D.等体积等物质的量浓度的NaHCO3和Ba(OH)2两溶液混合:
HCO3-+Ba2++OH-=BaCO3↓+H2O
11.下列反应的离子方程式正确的是
A 次氯酸钠的溶液中通入少量的SO2气体 2ClO-+ SO2+ H2O= SO32-+ 2HClO
B 硫化氢气体通入CuSO4溶液 H2S +Cu2+=CuS↓+2H+
C Na2O2固体溶于水 Na2O2 + 2H2O = 2Na++ 2OH-+ O2 ↑
D Ba(OH)2溶液中加入过量的碳酸氢钠溶液 Ba2+ + OH-+ HCO3- = BaCO3↓+ H2O
10.下列有关化学实验的叙述正确的是 ( )
A.用待测液润洗滴定用的锥形瓶
B.配制FeCl3溶液时,向溶液中加入少量Fe和稀盐酸
C.用稀盐酸洗涤盛放过石灰水的试剂瓶
D.Na2CO3溶液保存在带玻璃塞的试剂瓶中
9.下列各组在溶液中反应,无论反应物的量怎么改变,其化学方程式都不变的是
A.FeBr2与Cl2 B.Ba(OH)2与H2SO4 C.CO2与NaOH D.Ca(HCO3)2与NaOH
8.将过量的气体通入到一种溶液中,一定能产生沉淀的是
①二氧化硫通入到硝酸钡溶液中 ②二氧化碳通入偏铝酸钠溶液中 ③二氧化碳通入到氯化钙溶液中 ④氨气通入到AgNO3溶液中
A.只有①② B.只有①②③ C.只有①②④ D.只有②③
7.下列各组溶液,不加任何试剂,也不做焰色反应实验,不能将其一一区别出来的是A.(NH4)2SO4、BaCl2、NaOH、NaCl B.NaCl、AgNO3、Na2CO3、CaCl2
C.CuSO4、BaCl2、NaOH、NaCl D.Al2(SO4)3、Na2CO3、Ba(NO3)2、H2SO4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com