
题目列表(包括答案和解析)
17、 在一定温度下,容器内某一反应中M、N的物质的量n随反应时间t变化的曲线如
 图所示,下列表述中正确的是( )
图所示,下列表述中正确的是( )
A. 反应的化学方程式为2M N
N
B. t2时V正=V逆,达到平衡
C. t3时V正 > V逆
D. t1时浓度c(N)=2c(M)
16、 在某温度下,可逆反应mA + nB 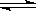 pC + qD的平衡常数为K,下列说法正确的是( )
pC + qD的平衡常数为K,下列说法正确的是( )
A.K越大,达到平衡时,反应进行的程度越大
B.K越小,达到平衡时,反应物的转化率越大
C.K随反应物浓度的改变而改变
D.K随温度和压强的改变而改变
15、可逆反应∶2NO2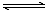 2NO+O2在密闭容器中反应,达到平衡状态的标志是:
2NO+O2在密闭容器中反应,达到平衡状态的标志是:
①单位时间内生成n molO2的同时生成2n molNO2 ②单位时间内生成n molO2 的同时,生成2n molNO ③用NO2、NO、O2 的物质的量浓度变化表示的反应速率的比为2 : 2 : 1的状态 ④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态 ⑥ 混合气体的平均相对分子质量不再改变的状态
A.①④⑥ B.②③⑤ C.①③④ D.①②③④⑤⑥
14、高氯酸铵(NH4ClO4)加热至483 K时,可完全分解成N2、Cl2、O2和H2O,则反应中氧化产物与还原产物的物质的量之比是( )
A.1∶1 B.1∶3 C.2∶1 D .3∶1
13、若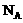 代表阿伏加德罗常数,下列说法正确的是 (
)
代表阿伏加德罗常数,下列说法正确的是 (
)
A.1 molCl2参加反应转移电子数一定为2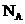
B.将31g的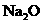 溶解于1L水中,所得溶液中
溶解于1L水中,所得溶液中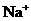 的物质的量浓度为1 mol/L
的物质的量浓度为1 mol/L
C.常温常压下,22.4L的NH3 和16g CH4中所含有的电子数都是10NA
D.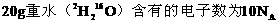
12、在下述条件下,一定能大量共存的离子组是( )
A.强酸性溶液中:Al3+、K+、Mg2+、Cl-、SO42-
B.PH=13的溶液中:Cl-,HCO3-,NO3-,NH4+
C.c(Fe3+)=0.1 mol·L-1的溶液中:Na+、SCN-、Cl-、Br-
D.强碱性溶液中:ClO-、SO42-、SO32-、Na+
11、下列离子方程式书写可能正确的是( )
A.钠与水的反应:Na + H2O === Na+ +OH-+ H2↑
B.用浓盐酸与MnO2
反应制取少量氯气:MnO2+2H++2Cl- Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
C.在氢氧化钠溶液中通入少量的CO2:2OH-+CO2=CO32-+H2O
D.在硫酸铝溶液中加入过量氨水:Al3+ + 4OH- = AlO2-+2H2O
10、下图 为直流电源,
为直流电源, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽。
为电镀槽。
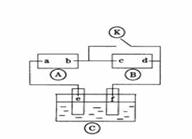 接通电路后发现
接通电路后发现 上的c点显红色。为实现铁上镀锌,接通
上的c点显红色。为实现铁上镀锌,接通 后,使c、d两点短路。
后,使c、d两点短路。
下列叙述正确的是( )
A.a为直流电源的负极 B.c极发生的反应为2H++2e-=H2↑
C.f电极为锌板 D.e极发生还原反应
9、用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一物质中(括号内),溶液能与原来溶液完全一样的是( )
A.CuCl2 [CuSO4] B.NaOH [NaOH] C.NaCl [HCl] D.CuSO4 [Cu(OH)2]
8、金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+)( )
A. 阳极发生还原反应,其电极反应式:Ni2++2e- =Ni
B. 电解过程中,阳极质量的减少与阴极质量的增加相等
C. 电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D. 电解后,电解槽底部的阳极泥中只有Cu和Pt
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com