
题目列表(包括答案和解析)
8.某同学为检验溶液中是否含有常见的几种无机离子,进行了如下图所示的实验操作。其中检验过程中产生的气体能使湿润的红色石蕊试纸变蓝。由该实验能得到的正确结论是
( )
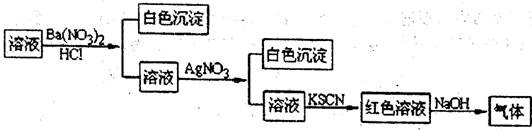
A.原溶液中一定含有SO2-4 B.原溶液中一定含有NH+4
C.原溶液中一定含有Cl- D.原溶液中一定含有Fe3+
7.短周期元素X、Y、Z的原予序数依次递增,其原子的最外层电子数之和为13。X与Y、 Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的3倍,下列说法正确的是 ( )
A.X的最高价氧化物的水化物显弱酸性
B.Y的氧化物是离子化合物
C.X的氢化物的水溶液在空气中存放不易变质
D.X的氢化物和Z的氢化物反应生成一种对热稳定的化合物
6.常温下,在密容器里分别充入两种气体各0.1mol,在一定条件下充分反应后,恢复到原温度时,压强降低为开始的1/4,则混合气体可能是 ( )
A.H2和O2 B.HCl和NH3 C.H2和Cl2 D.CO和O2
5.下列实验操作正确的是 ( )
①用带橡皮塞的棕色试剂瓶存放浓硫酸;
②将0.1 mol/L的氢氧化钠溶液与0.5mol/L的硫酸铜溶液等体积混合制得氢氧化铜悬浊液,用于检验醛基;
③用盐权酸化过的FeCl3溶液除去H2还原CuO实验留在试管内的铜迹;
④测定某溶液的pH,先用蒸馏水润湿pH试纸,再用洁净、干燥的玻璃棒蘸取该溶液滴在试纸上,并与标准比色卡比较
⑤分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出;
⑥蒸馏时,将温度计的水银球靠近蒸馏烧瓶支管口附近
A.①③ B.②③④ C.①③⑥ D.③⑤⑥
4.设NA表示阿伏加德罗常数的值,下列叙述正确的是 ( )
A.1L 0.1mol·L-1的CH3COONa溶液中CH3COO-的总数是0.1NA
B.常温常压下,1.6gO2和O3混合气体中质子总数为0.8NA
C.一定条件下,2mol SO2和1mol O2发生反应,转移的电子总数一定是4NA
D.1L 0.1mol·L-1的葡萄糖溶液中分子总数为0.1NA
3.“复盐”是指含多种简单阳离子和一种酸根离子组成的盐,如KAl(SO4)2而由一种金属离子与多种酸根离子构成的盐则称为“混盐”,如氯化硝酸钙[Ca(NO3)Cl]。下列化合物属于混盐的是 ( )
A.CaOCl2 B.(NH4)2Fe(SO4)2 C.BiONO3 D.K3[Fe(CN)6]
2.在化学反应中,反应前与反应后相比较,肯定不变的是 ( )
①元素种类 ②原子种类 ③分子数目 ④原子数目
⑤反应前物质的质量总和与反应后物质的质量总和
⑥如果在水溶液中反应,则反应前与反应后阳离子所带的正电荷总数
A.①②③④ B.①②⑤⑥ C.①②④⑤ D.②③⑤⑥
1.分类方法在化学学科的发展中起到非常重要的作用。下列分类标准合理的是 ( )
①根据酸分子中含有的氢原子个数将酸分为一元酸、二元酸等
②根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊夜
④根据反应中的热效应将化学反应分为放热反应和吸热反应
A.①② B.③④ C.①③ D.②④
21.(12分)本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.雷尼镍(Raney-Ni)是一种历史悠久、应用广泛的催化剂,由镍-铝合金为原料制得。
(1)元素第一电离能:Al ▲ Mg(选填:“>”、“<”、“=”)
(2)雷尼镍催化的一实例为:
化合物b中进行sp3杂化的原子有: ▲ 。
 (3)一种铝镍合金的结构如下图,与其结构相似的化合物是: ▲ (选填序号:a.氯化钠
b.氯化铯 c.石英
d.金刚石)。
(3)一种铝镍合金的结构如下图,与其结构相似的化合物是: ▲ (选填序号:a.氯化钠
b.氯化铯 c.石英
d.金刚石)。
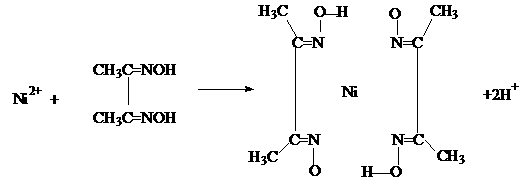
(4)实验室检验Ni2+可用丁二酮肟与之作用生成腥红色配合物沉淀。
①Ni2+在基态时,核外电子排布式为: ▲ 。
②在配合物中用化学键和氢键标出未画出的作用力(镍的配位数为4)。
B.4-氯苯胺是合成橡胶、化学试剂、染料、色素等化工产品,制备4-氯苯胺的原理如下:
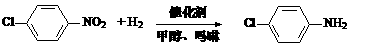 。
。
在1 L密闭容器中加入4-氯硝基苯100 g、雷尼镍(催化剂)及少量吗啉(脱氯抑制剂,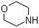 )、甲醇250mL(溶剂),密封;先充入氮气,然后充入氢气至一定压力。在所需氢气压力、温度等条件下加氢反应,充分反应后,冷却,过滤,洗涤,蒸馏并收集64-65℃馏分。
)、甲醇250mL(溶剂),密封;先充入氮气,然后充入氢气至一定压力。在所需氢气压力、温度等条件下加氢反应,充分反应后,冷却,过滤,洗涤,蒸馏并收集64-65℃馏分。
(1)开始时先通入N2的目的是 ▲ 。
(2)上述实验中过滤的目的是 ▲ ,洗涤所用的试剂是 ▲ 。
(3)蒸馏时除用到接引管、锥形瓶、温度计外,还用到的玻璃仪器有: ▲ 、 ▲ 。馏出液的主要成分是 ▲ 。
(4)以下是温度、氢气压力、催化剂用量及吗啉的用量对反应的影响。
|
|
表1温度 |
|
表2氢气压力 |
|
|
表3催化剂用量 |
|
表4吗啉用量 |
|||||||
|
序号 |
温度/℃ |
转化率/% |
选择 性/% |
反应时间/h |
序号 |
氢气压力/MPa |
选择性/% |
反应时间/h |
序号 |
雷尼镍用量/g |
选择性/% |
反应时间/h |
序号 |
吗啉用量/% |
选择性/% |
|
① |
40 |
未完全 |
99.6 |
6 |
① |
0.5 |
99.6 |
3.7 |
① |
2 |
98.25 |
5 |
① |
0.0 |
84.3 |
|
② |
60 |
100 |
99.7 |
4 |
② |
1.0 |
99.7 |
2 |
② |
4 |
99.20 |
2.2 |
② |
0.3 |
99.3 |
|
③ |
80 |
100 |
99.6 |
2.45 |
③ |
1.5 |
99.2 |
1.6 |
③ |
6 |
99.60 |
1.9 |
③ |
0.5 |
99.7 |
|
④ |
100 |
100 |
99.6 |
2 |
④ |
2.0 |
96.4 |
1.15 |
④ |
8 |
99.60 |
1.4 |
④ |
0.7 |
99.6 |
|
⑤ |
120 |
100 |
98.6 |
1.7 |
⑤ |
|
|
|
⑤ |
10 |
99.10 |
1.4 |
⑤ |
1.2 |
99.7 |
优化的条件是:温度、氢气压力、催化剂用量、吗啉用量,选择的序号依次是 ▲ 。
盐城市2010/2011学年度高三年级第一次调研考试
20.(10分)煤制油是一项新兴的、科技含量较高的煤化工技术,发展煤制油对我国而言具有重大意义。下列是煤通过间接液化技术制汽油和丙烯的主要工艺流程图。
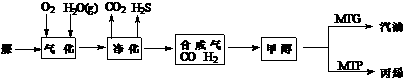
已知甲醇制烃的反应原理为:
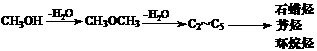
(1)为了提高原料利用率,上述工艺中应控制合成气中V(CO):V(H2)= ▲ 。
(2)由二甲醚在催化剂作用下转化为丙烯的化学方程式为: ▲ 。
(3)每生产1t甲醇约耗煤1.5t,每生产1 t汽油约需耗2.4t甲醇,2015年我国煤制油将达到1000万吨,则2015年当年需消耗原煤约 ▲ 万吨。
(4)采用MTG法生产的汽油中,均四甲苯(1,2,4,5-四甲基苯)质量分数约占4 %-7%,均四甲苯的结构简式为: ▲ 。
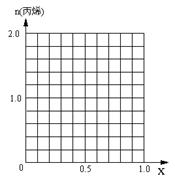
(5)采用DMTO技术,若获得乙烯和丙烯及丁烯3种烃,生成丁烯的选择性(转化丁烯的甲醇的物质的量与甲醇总物质的量之比)为20%,其余生成乙烯和丙烯,设丙烯的选择性为x,今有403.2L(标准状况)合成气,且完全转化为甲醇,甲醇转化为烯烃的总转化率亦为100%,请作出丙烯的物质的量随x变化的曲线。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com