
题目列表(包括答案和解析)
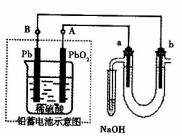
23.用铅蓄电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)
的装置如图所示(a、b为石墨电极)。下列说法中
正确的是 ( )
A.铅蓄电池负极的反应式为:Pb-2e-=Pb2+
B.铅蓄电池放电时,B极质量减轻,A极质量增加
C.铅蓄电池充电时,A极应与外电源负极相连
D.电解苦卤水时,a电极首先放电的是Br-
22.实验是化学研究的基础,关于下列各装置图的叙述正确的是 ( )
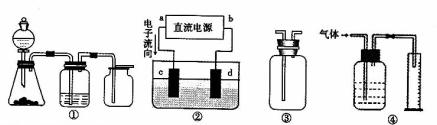
A.装置①可完成多种气体的发生、净化和收集,如铜屑与稀硝酸反应
B.装置②中,a为正扳,d为阳极
C.装置③可用于收集H2、NH3、Cl2,、HCl、NO2等
 D.装置④能用于测量气体体积
D.装置④能用于测量气体体积
21.某些金属卤化物可以跟其对应卤素反应,如KI +I2 KI3,则下列推断错误的是( )
KI3,则下列推断错误的是( )
A.在K溶液中加入淀粉溶液可变蓝色
B.向溶液中滴加AgNO,溶液时,会出现黄色沉淀
C.配制碘水时加入KI可以增大I2在水中的溶解程度
D.将氯气通人KI,液中,I-3的浓度不会发生变化
20.FeCl3、CuCl2的混合溶液中加入铁粉,充分应后仍有固体存在,则下列判断不正确的是
( )
A.加人KSCN溶液一定不变红色 B.溶液中一定含Fe2+
C.溶液中一定含Cu2+ D.剩余固体中一定含铜
19.下图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容,据此,下列说法正确的是 ( )
 A.该硫酸的物质的量浓度为9.2 mol/L
A.该硫酸的物质的量浓度为9.2 mol/L
B.配制200 mL 4.6 mol/L的稀硫酸需取该硫酸25 mL
C.该硫酸与等体积的水混合后所得溶液浓度为9.2 mol/L
D.该硫酸与等体积水混合后质量分数大于49%
18.已知:N2(g)+3H2(g) 2NH3(g)△H=- QkJ/mol
2NH3(g)△H=- QkJ/mol
现分别在相同条件下进行下述三个实验:
|
实验编号 |
N2/mol·L-1 |
H2/mol·L-1 |
NH3/mol·L-1 |
|
① |
0.5 |
1.5 |
0 |
|
② |
0.4 |
1.2 |
0.2 |
|
③ |
0.4 |
1.1 |
0.3 |
充分作用后,测得实验①反应放出热量为Q1kJ,实验②没有热量变化。则下列说法不正确的是 ( )
A.实验①反应放出热量值Q1=0.1Q
B.实验①达平衡时H2转化率为20%
C.实验③恒应吸收热量为Q1kJ
D.该条件下反应的平衡常数约为0.058 L2/mol2
17.设NA代表阿伏加德罗常数,下列说法正确的是( )
A.12g NaHSO4在熔融时离子总数为0.3NA
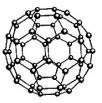
B.28 g Nm单质(见右图)中含有的N-N键个数为3NA
C.在25℃1.01×105Pa时,11.2 L氧气所含的原子数为NA
D.常温下,将5.6 g铁投入足量的浓硫酸中转移电子数为0 3NA
16.下列离子方程式正确的是 ( )
A.硫酸铜溶液与氢氧化钡溶液反应:SO2-4+Ba2+=BaSO4↓
B.碳酸氢钠溶液中加入过量石灰水:
2HCO-3+Ca2++2OH-=CaCO3↓+CO2-3+2H2O
C.硅酸钠溶液与稀盐酸反应制取硅酸凝胶:SiO2-3+2H+=H2SiO3(胶体)
 D.碳酸钠溶液显碱性:CO2-3+H2O=HCO-3+OH-
D.碳酸钠溶液显碱性:CO2-3+H2O=HCO-3+OH-
15.已知:2CO(g)+O2(g)==2CO2(g) △H=-566kJ·mol-1
N2(g)+O2(g)=2NO(g) △H=+180kJ·mol-1
则2CO(g)+2NO(g)===N2(g)+2CO2(g)的△H是 ( )
A.-386 kJ·mol-1 B.+386 kJ·mol-1
C.-746 kJ·mol-1 D.+746 kJ·mol-1
14.22.4L某气态氮氧化物与足量的灼热铜粉完全反应后,气体体积为11.2L(体积均在相同条件下测定),则该氮氧化物的化学式为 ( )
A.NO2 B.N2O3 C.N2O D.N2O4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com