
题目列表(包括答案和解析)
3.下列有关物质分类或归类正确的一组是
①液氨、液氯、干冰、碘化银均为化合物
②氢氟酸、盐酸、水玻璃、氨水均为混合物
③明矾、小苏打、醋酸、次氯酸均为电解质
④碘酒、牛奶、豆浆、漂粉精均为胶体yjw
⑤Na2O2、Na2CO3、NaHCO3、Na2SiO3均为钠盐
A.①和② B.②和③ C.③和④ D.②③⑤
2.下列化学用语错误的是
A.NaCl的电子式  B.甲烷的结构式
B.甲烷的结构式 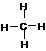

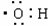
C.氨分子的结构式 D.羟基电子式
在每个小题给出的四个备选答案中,只有一个符合题目的要求。
1.化学与科学、技术、社会、环境密切相关,下列做法中不正确的是yjw
A.回收废旧电池,主要目的是回收其中的金属
B.减少燃煤使用,改用风能、太阳能等能源,符合“低碳生活”的理念
C.在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质
D.用浸泡过高锰酸钾溶液的硅藻土吸收水果中的乙烯,可以实现水果保鲜的目的
30.已知:当羟基与双键碳原子相连接时,易发生如下的转化:
CH2=CH-OH→CH3CHO
化学式为C8H8O2的有机物有如下的转他关系:
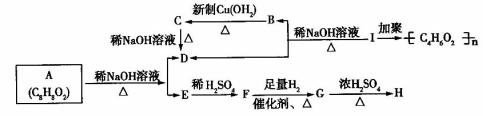
其中F与FeO,溶液能发生显色反应,H能使酸性KMnO4溶液褪色。
请回答下列问题:
(1)结构简式:D H I 。
(2)G→H的反应类型: 。
(3)A生成D和E的化学方程式:___ 。
(4)B→C的化学方程式:___ 。
29. A、B、C、D、E、F为原子序数依次增大的短周期主族元素。A、F原子的最外层电子数均等于其周期序数,F原子的电子层数是A的3倍;B原子核外电子分处3个不同能级,且每个能级上排布的电子数相同;A与C形成的最简单分子为三角锥形;D原子p轨道上成对电子数等于未成对电子数;E原子核外每个原子轨道上的电子都已成对,E电负性小于F。
A、B、C、D、E、F为原子序数依次增大的短周期主族元素。A、F原子的最外层电子数均等于其周期序数,F原子的电子层数是A的3倍;B原子核外电子分处3个不同能级,且每个能级上排布的电子数相同;A与C形成的最简单分子为三角锥形;D原子p轨道上成对电子数等于未成对电子数;E原子核外每个原子轨道上的电子都已成对,E电负性小于F。
(1)写出B的基态原子的核外电子排布式 。
(2)A、C形成的最简单分子极易溶于水,其主要原
因是 ;与该最简单分子互为等电子体的
阳离子为 。
(3)比较E、F的第一电离能:E F(选填“>”或“<”)。
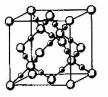
(4) BD,在高温高压下所形成的晶胞如右图所示。该晶体的类型属于 (选填“分子”、“原子”、“离子”或“金属”)晶体,该晶体中B原子的杂化形式为 。
(5)光谱证实单质F与强碱性溶液反应有[F(OH)4]-生成,则[F(OH)4]-中存在 。
a.极性键 b.非极性键
c.配位键 d. 键 e.π键
键 e.π键
28.已知X和Y各是由两种常见元素组成的化合物,A、B为气体,G为白色沉淀,F是一种两性氢氧化物,在电解开始时,溶液中有白色沉淀产生,但随着电解的进行,白色沉淀逐渐溶酶,最后变为澄清溶液C(有两种溶质),X、W、C、E的焰色反应均为黄色。各物质之间的关系如图所示
(部分产物已经省略,除气体间的反应外,其余反应均在溶液中进行)。
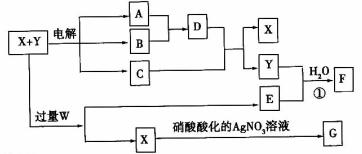
回答下列问题:
(1)X、Y的化学式分别为
(2)写出反应①的离子方程式____ 。
(3)A与B反应生成1mol D时放出热量为92.3kJ,则此反应的热化学方程式为 。
(4)向澄清溶液C中加入1mol·L-1的硫酸,当加至50mL时才开始出现沉淀,假设电解过程中溶液体积变化忽略不计,原X和Y混合液的体积为100mL,Y溶液的物质的量浓度为a mol·L-1,则x溶液的物质的量浓度为 mol·L-1(含a代数式表示)
(选考题)(共12分,请考生从29、30题中任选一道做答。如果多做,则按第一题计分。)
27.某无色溶液X,由Na+、Ag+、Ba2+、Al3+、AlO-2、MnO-4、CO2-3、SO2-4中的若干种离子组成,取溶液进行如下连续实验:
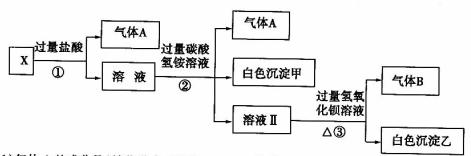
(1)气体A的成分是(填化 学式,下同) ,气体B的成分是 。
(2)X溶液中一定存在的离子是 。
(3)写出步骤①发生所有反应的离子方程式 。
(4)写出步骤②形成白色沉淀甲的离子方程式 。
(5)通过上述实验,溶液X中还有未完全确定的离子是 ;只要设计一个简单的后续实验就可以确定该离子是否存在,该方法是 。
26.T℃时,将3molA和1molB气体通人体积为2L的密闭容器(体积不变),发生反应:
3A(g)+B(g) xC(g)。2nnn时达平衡,剩余0.8moIB,C的浓度为0.4mol/L。
xC(g)。2nnn时达平衡,剩余0.8moIB,C的浓度为0.4mol/L。
(1)x= ;
(2)若向平衡混合物中通入少量He,则平衡 (填“正向移动”、“逆向移动”或“不移动”)
(3)若向平衡混合物中再充入 a mol C,在T℃时达新平衡,此时B的物质的量为
(用含a的式子表示):
(4)若上述反应在相同温度和容器中进行,欲使反应达平衡时c的物质的量分数与原平衡相等,则起始加入三种物质的量n (A)、n (B)、n (C)间应满足的关系式为
。
25.现有下列8种物质:①Na2CO②NaHCO3③SO3④NH4HCO3⑤C2H5OH⑥Al⑦食盐水
⑧CH3COOH。
(1)上述物质中属于强电解质的是 (填序号);既能跟盐酸反应又能跟NaOH溶液反应的是____ (填序号)。
(2)上述②的水溶液中离子浓度从大到小的顺序为 。
(3)④跟足量的NaOH溶液在加热条件下反应的离子方程式是____
24.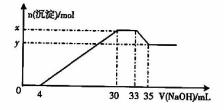 在200mL含Mg2+、Al3+、NH+4、H+、Cl-等离子的溶液中,逐滴加入5mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示。下列叙述不正确的是 ( )
在200mL含Mg2+、Al3+、NH+4、H+、Cl-等离子的溶液中,逐滴加入5mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示。下列叙述不正确的是 ( )
A.x与y的差值为0.01mol
B.原溶液中c(Cl-)=0.75mol/L
C.原溶液的pH=1
D.原溶液中n(Mg2+):n(Al3+)=5:1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com