
题目列表(包括答案和解析)
22.(11分)
I.实验室有一瓶失去标签的某白色固体,已知其成份可能是碳酸或亚硫酸的钠盐或钾盐,
且其成分单一。现某化学小组通过如下步骤来确定其成分:
(1)阳离子的确定:
实验方法及现象:
结论:此白色固体是钠盐。
(2)阴离子的确定:
①取少量白色固体于试管中,然后向试管中加入稀盐酸,白色固体全部溶解,产生
无色气体,此气体能使溴水褪色。
②要进一步确定其成分需补做如下实验:取适量白色固体配成溶液,取少许溶液于试管中,加入BaCl2溶液,出现白色沉淀。
II.确认其成分后,,由于某些原因,此白固体部分被空气氧化,该化学小组想用已知
浓度的酸性KMnO4溶液来确定变质固体中X的含量,具体步骤如下:
步骤I 称取样品1.000g。
步骤II 将样品溶解后,完全转移到250mL容量瓶中,定容,充分摇匀。
步骤III 移取25.00mL样品溶液于250mL锥形瓶中,用0.01mol·L-1KMnO4标准溶液
滴定至终点。
按上述操作方法再重复2次。
(1)写出步骤III所发生反应的离子方程式 。
(2)在配制0.01mol·L-1KMnO4溶液时若仰视定容,则最终测得变质固体中X的含量
(填“偏大”、“偏小”或“无影响”)
(3)滴定结果如下表所示:
|
滴定次数 |
待测溶液的体积 /mL |
标准溶液的体积 |
|
|
滴定前刻度/mL |
滴定后刻度/mL |
||
|
1 |
25.00 |
1.02 |
21.03 |
|
2 |
25.00 |
2.00 |
21.99 |
|
3 |
25.00 |
2.20 |
20.20 |
则该变质固体中X的质量分数为 。
21.(12分)有A、B、C、D、E、F六种元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D、F为常见金属元素。A元素原子核内只有一个质子,元素A与B形成的气态化合物甲在标准状况下的密度为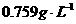 ,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族。均含D元素的乙(金属阳离子)、丙、丁微粒间的转化全为非氧化还原反应:均含F元素的乙(单质)、丙、丁微粒间的转化全为氧化还原反应。
,C元素原子的最外层电子数是其电子层数的3倍,E与C同主族。均含D元素的乙(金属阳离子)、丙、丁微粒间的转化全为非氧化还原反应:均含F元素的乙(单质)、丙、丁微粒间的转化全为氧化还原反应。
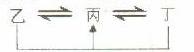
请回答下列问题:
(1)单质B的结构式: 。
(2)F元素周期表中的位置: 。
(3)均含有F元素的乙与丁在溶液中发生反应的离子方程式 ;均含有D元素的乙与丁在溶液中发生反应的离子方程式 。
(4)由A、C元素组成化合物良和A、E元素组成的化合物辛,式量均为34。其中庚的溶沸点比辛 (填“高”或“低”),原因是 。
20.向mg镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体bL。向反应后的溶液中加入cmol/L氢氧化钾溶液VmL,使金属离子刚好沉淀完全,得到的沉淀质量为ng。再将得到的沉淀灼烧至质量不再改变为止,得到固体pg。则下列关系不正确的是 ( )
A. B.
B. C.
C.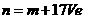 D.
D.
19.某同学按右图所示的装置进行试验。A、B两种常见金属,它们的硫酸盐可溶于水,当K闭合时,在交换膜处SO2-4从右向左移动。下列说法错误的是 ( )
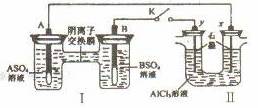
A.电解一段时间后,向II装置通入适量的HCl气体可以恢复原来的浓度
B.反应初期,y电极周围出现白色沉淀
C.B电极质量增加
D.x电极产生气泡,且生成1mol气体的同时,有1molA参与反应
18.在25mL0.1mol/LNaOH溶液中逐滴加入0.2mol/L溶醋酸溶液,曲线如下图所示,有关粒子浓度关系不正确的是 ( )
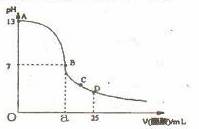
A.在A、B间任一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.在B点:a>12.5
C.在C点:(c(CH3C OO-)>c(Na+)>c(H+)>c(OH-)
D.在D点:c(CH3COO-)+c(CH3COOH)=2c(Na+)
17.如图是某研究小组采用电解法处理石油炼制过程中产生的大量H2S废气的工艺流程。该方法对H2S的吸收率达99%以上,并可制取H2和S。下列说法正确的是 ( )

A.吸收H2S的离子方程式为:Fe3++H2S==F2++S↓+2H+
B.电解过程中的阳极反应主要为:2Cl--2e-==Cl2↑
C.该工艺流程体现绿色化学思想
D.实验室可用点燃充分燃烧的方法消除H2S污染
16.等质量的三份锌a、b和c,分别加入足量的稀H2SO4中,a中同时加入选题CuSO4溶液,c中加入适量CH3COONa。下列各图中表示其产生氢气总体积(V)与时间(t)的关系,其中正确的是 ( )

15.在一定温度下,将等量的气体分别通入起始体积相同的密闭容器I(恒溶)和II(司压中,使其发生反应,t0时容器I中达到化学平衡,X、Y、Z的物质的量的变化如图所示),则下列有关推断正确的是 ( )

 A.该反应的化学方程式为:3X+2Y 2Z
A.该反应的化学方程式为:3X+2Y 2Z
B.若两容器中均达到平衡后,两容器的体积V(I)<V(II),则容器II达到平衡所用
时间小于t0
C.若两容器中均达到平衡时,两容器中Z的物质的量分数相同,则Y为固态或液态
D.达平衡后,若对容器II升高温度时其体积增大,说明Z发生的反应为吸热反应
14.可用右侧示意图像表示的是 ( )

13.下列各选项中所述的两个量,前者一定大于后者的是 ( )
A.pH=10的NaOH和Na2CO3溶液中,水的电离程度
B.物质的量浓度相等的(NH4)2SO4溶液与(NH2)CO3溶液中NH4的物质的量浓度
C.将pH=3的盐酸和醋酸分别稀释成pH=5的溶液,所加水的量
D.相同温度下,10mL0.1mol/L的醋酸与100mL0.01mol/L的醋酸中的H物质的量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com