
题目列表(包括答案和解析)
4、能正确表示下列反应的离子方程式是
A.将铜屑加入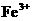 溶液中:
溶液中: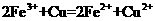
B.将磁性氧化铁溶于盐酸: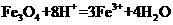
C.将氯化亚铁溶液和稀硝酸混合: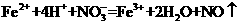
D.将铁粉加入稀硫酸中: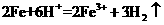
3、下列试剂:①浓氨水 ②氯水 ③硝酸银 ④浓硝酸 ⑤浓盐酸 ⑥溴化银,其中必须用棕色试剂瓶装的有
A.①②③④⑤⑥ B.②③④⑥ C.②③⑤⑥ D.①③④⑤
2、下列判断错误的是
A.沸点: NH3 > PH3 > AsH3 B.熔点: Si3N4 > NaCl > SiI4
C.酸性:HClO4 > H2SO4 > H3PO4 D.碱性:NaOH > Mg(OH)2 > Al(OH)3
1、北京大学和中国科学院的化学工作者已成功研制出碱金属与C60形成的球碳盐K3C60,实验测知该物质属于离子晶体,具有良好的超导性。下列有关分析正确的是
A.K3C60中只有离子键 B.K3C60中碳元素显-3价
C.该晶体在熔融状态下能导电 D.C60与12C互为同素异形体
21.(12分) 某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,用下图装置进行有关实验,请回答:
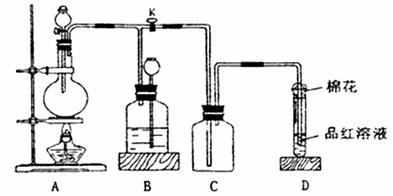
(1)装置D中试管口放置的棉花中应浸一种液体,这种液体的作用是 。
(2)装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是 。 B中应放置的液体是(填字母) 。
a.NaOH溶液 b.酸性KMnO4 溶液
c.浓溴水 d.饱和NaHSO3溶液
(3)铜不能与稀硫酸直接反应得到硫酸铜,但可用下面方法制取:将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发浓缩、冷却结晶可制得硫酸铜晶体(装置如图1、2所示)。
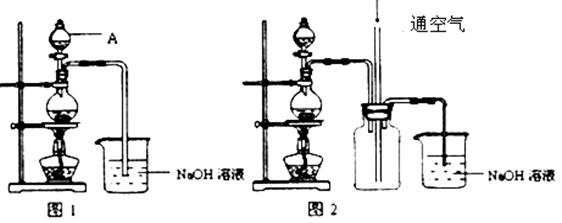
①把浓硝酸分多次加入到铜粉与稀硫酸的混合物中的目的是________ _____
__ __。
②已知NO不能被NaOH溶液直接吸收,但已知有如下两个反应:
NO+NO2+2NaOH=2NaNO2+H2O;2NO2+2NaOH=NaNO3+NaNO2+H2O。图2是图1的改进装置,其优点除可以防止倒吸外还有:_______________________。
③如果用1molCu来制取1molCuSO4 ,则所需浓硝酸中HNO3的质量为________,(假设HNO3的还原产物全为NO),若所得尾气恰好被NaOH溶液吸收为NaNO2,需通入空气的体积为_____(假设实验体积为标准状况下测定,保留小数点后一位,并忽略装置中原有空气的影响)
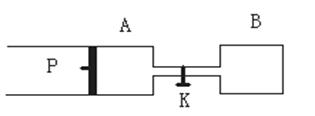
20. (10分)右下图中P为一可自由滑动的活塞,K为容器A和B之间的旋塞。将K关闭,在A中充有1molX和1molY,B中充有3molX和3molY。起始时,V(A)=V(B)=1L,在相同的温度和有催化剂存在的条件下,两容器中各自发生反应:
 X(g)+Y(g)
X(g)+Y(g)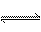 2Z(g)+W(g);△H<0。
2Z(g)+W(g);△H<0。
当达到平衡时,V (A)=1.25L。问:
(1)A中Y的转化率为 ,A、B中Y的转化率的关系是a(A) a(B)(填“<”、“>”或“=”)。
 (2)如果将B端改装成与A端一致(如右图),
(2)如果将B端改装成与A端一致(如右图),
将K关闭,达到平衡后,B的体积为______L,
B中X的体积分数为___________________。
此时,如果将K打开,A中活塞_________(填“移动”或“不移动”,)
19.(12分)A、D、E、X、Y五种短周期元素,它们的原子序数依次增大,A元素的原子
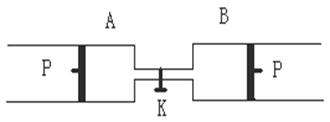
是半径最小的原子,D元素的最高价氧化物对应的水化物与其氢化物反应生成一种盐;X与A同主族;Y元素的最外层电子数是其次外层电子数的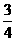 倍;A、D、X、Y四种元素,每一种均能与E元素形成原子个数比不相同的若干化合物。
倍;A、D、X、Y四种元素,每一种均能与E元素形成原子个数比不相同的若干化合物。
(1)画出Y元素离子的结构示意图 ;写出常温下Y的氢化物与其最高价氧化物对应水化物的浓溶液反应的化学方程式 。
(2)由A、D、E、Y四种元素形成的强酸的酸式盐的名称为 ,该盐的水溶液中各离子浓度由大到小的顺序为 。
(3)科学家用D、E、X 三种元素形成的化合物XDE3和X2E,在573K时反应制得了离子化合物X3DE4;经测定X3DE4中各原子的最外层电子都达到了8电子稳定结构,则DE43-的电子式为 ,X3DE4与水能剧烈反应转化为常见物质,写出反应的化学方程式: 。
17.(14分)现有浓度均为0.1 mol/L的下列溶液:①硫酸 ②醋酸 ③氢氧化钠
④氯化铵 ⑤醋酸铵 ⑥硫酸铵 ⑦硫酸氢铵 ⑧氨水,请回答下列问题:
(1)①②③④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)_ 。
(2)④⑤⑥⑦⑧五种溶液中NH4+浓度由大到小的顺序是(填序号)___ ___。
 (3)将③和④等体积混合后,混合液中各离子浓度由大到小的顺序是 _____。
(3)将③和④等体积混合后,混合液中各离子浓度由大到小的顺序是 _____。
(4)已知t℃,KW=1×10-13,则t℃(填“>”或“<”或“=”) 25℃。在t℃时将pH=11的NaOH溶液a L与pH=1的H2SO4的溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=10,则a∶b= 。
(5)25℃时,有pH=x的盐酸和pH=y 的氢氧化钠溶液(x≤6,y≥8),取aL该盐酸与该氢氧化钠溶液中和,消耗bL的氢氧化钠溶液,问:
①若x+y=14,则a/b=__ __(填数据);②若x+y=13,则a/b=__ __
(填数据);
③若x+y>14,则a/b=__ __(填表达式);
④该盐酸与该氢氧化钠溶液完全中和,两溶液的pH x和y的关系式 (填表达式)。
|
|
Q |
R |
|
|
T |
|
|
W |
18 (12分)Q、R、T、W四种短周期元素在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:
(1)T的原子结构示意图为_______.
(2)元素的非金属性为(原子的得电子能力):Q______W(填“强于”或“弱于”)。 (3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为_____. (4)原子序数比R多1的元素的一种氢化物A能分解为其另一种氢化物B,写出A的电子式______. (5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是__________. (6)在298K下,Q、T的单质各1mol完全燃烧,分别放出热量aKJ和bKJ。又知一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3molQ的单质,则该反应在298K下的△H =________kJ/mol(注:题中所设单质均为最稳定单质)
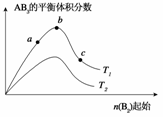
16.某化学科研小组研究在其他条件不变,改变某一条件对A2(g)+3B2(g)
 2AB3(g)化学平衡状态的影响时,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据图示得出的结论正确的是
( )
2AB3(g)化学平衡状态的影响时,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据图示得出的结论正确的是
( )
A.反应速率a>b>c
B.达到平衡时,A2的转化率大小为:b>a>c
C.若T2>T1,则正反应是吸热反应
D.达到平衡时,AB3的物质的量大小为:c>b>a
第Ⅱ卷(共60分)
15.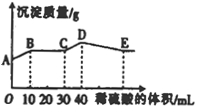 将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解,向混合溶液中滴加1mol·L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示。下列有关判断不正确的( )
将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解,向混合溶液中滴加1mol·L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示。下列有关判断不正确的( )
A.AB段发生反应的离子方程式为:
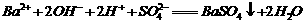
B.BC段发生反应的离子方程式为:H+ + OH-=H2O
C.D点表示的沉淀的化学式为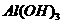 、
、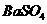
 D.E点表示的溶液呈中性
D.E点表示的溶液呈中性
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com