
题目列表(包括答案和解析)
16.某温度下,0.1mol/L醋酸溶液的pH=3。将该温度下0.2mol/L醋酸溶液和0.2mol/L醋酸钠溶液等体积混合后,混合液的pH=4.7。下列说法正确的是 ( )
A.该温度下,0.01mol/L醋酸溶液的pH=4
B.该温度下,用0.Imol/L醋酸和0.0lmol/L醋酸分别完全中和等体积0.1 mol/L的NaOH溶液,消耗两醋酸的体积比为1:10
C.该温度下,0.2 mol/L醋酸溶液和0.4 moI/L醋酸钠溶液等体积混合后,混合液的pH<4.7
D.该温度下,0.2 mol/L醋酸溶液和0.4 mol/L醋酸钠溶液等体积混合后,混合液的pH=4.7
第Ⅱ卷 非选择题(共52分)
15.0.1mol/L的K2S溶液中,有关粒子的浓度大小关系正确的是 ( )
A.c(K+)+c( H+)一c(S2-)+c(HS-)+c(OH-)
B.c(K+)+c(S2-)=0.3mol/L
C.c(K+)-c(g-)+c(HS-)+c(H2S)
D.c(OH-)=c(H+)+c(HS-)+2c(H2S)
14.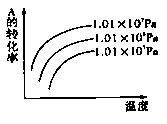 有一化学平衡:mA(妙十nB(g)
有一化学平衡:mA(妙十nB(g) C(g)+qD(g),
C(g)+qD(g),
的右图是表示A的转化率与压强、温度的关系,分析右图
可以得出的正确结论是 ( )
A.正反应是吸热反应,且m+n>p+q
B.正反应是吸热反应,且m+n<p+q
C.正反应是放热反应,且优十n>p+q
D.正反应是放热反应,且m+n< p+q
13.在密闭容器中,对于反应:2SO2(g)+O2(g) 2SO2(g),SO2和O2起始时分别为2mol和1mol;达平衡时,SO2的转化率为70%。若从SO3开始进行反应,在相同的温度下,欲使平衡时各成分的百分含量与前者相同,则起始时SO3的物质的量及其转化率为 ( )
2SO2(g),SO2和O2起始时分别为2mol和1mol;达平衡时,SO2的转化率为70%。若从SO3开始进行反应,在相同的温度下,欲使平衡时各成分的百分含量与前者相同,则起始时SO3的物质的量及其转化率为 ( )
A.1 mol和20% B.2 mol和30%
C.2 mol和40% D.2 mol和70%
12.下列关于物质性质变化的比较,不正确的是 ( )
A.稳定性:HI>HBr>HCl
B.原子半径大小:Na>S>O
C.碱性强弱:KOH>NaOH>LiOH
D.还原性强弱:F- <CI- <I-
11.已知:CH4(g)+2O2(g) COz (g)+2 Hz 0(1) △H= - Q1kJ. mol-l
2H2(g)+O2(g)=2H2O(g) △H= -Q2kJ·mol-1
2H2(g)+O2(g)=2H2O(1) △H= -Q3kJ·mol-1
常温下,取体积比为3:2的甲烷和氢气的混合气体33.6L(标准状况),
经完全燃烧后恢复到常温,放出的热量(单位:kJ)为 ( )
A.0.9Qi+o.6Q2 B.0.6Q1+0.4Q2
C.0.9Q11+o.3Q3 D.0.6Q1+0.4Q3
10.下列关于热化学反应的描述,正确的是 ( )
A.甲烷的标准燃烧热为890.3kJ.mol-l,则甲烷燃烧的热化学方程式可表示为:
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H= - 890.3kJ· mol-1
B.500℃、30MPa下,将0.5mol N2和1.5mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为(条件略):
N2(g)+3H2(g) 2NH3(g) △H= -38.6kJ·mol-1
2NH3(g) △H= -38.6kJ·mol-1
C.CO(g)的燃烧热是283.0 kJ·mol-1,则有热化学方程式为:2CO2(g) 2CO(g)+O2(g) △H= + 2×283.0 kJ·mol-1
D.HC1和NaOH反应的中和热△H= - 57.3 kJ·mol-1,则H2 SO4和Ca(OH)2反应的中和热△H=2×(- 57.3)kJ·mol-1
9.某密闭容器中发生如下反应:X(g)+3Y(g) 2Z(g);△H<O。下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是 ( )
2Z(g);△H<O。下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是 ( )
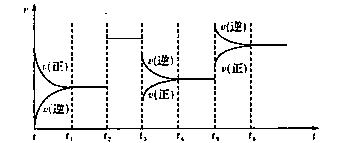
A.t2时加入了催化剂 B.t3时降低了温度
C.t3时增大了压强 D.t4-t5时间内反应物的转化率一定最低
8.在由水电离的OH-浓度为2.0×10-1z mollL的溶液中不可能大量共存的离子组是( )
A.K+、MnO4-、Mg2+、NO3- B.Fe2+、Na+、NO-3、Cu2+
C.Na+、H+、NO3-、SO2-4 D.Fe3+、Na+、C1-、SO2-4
7.有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法中,正确的是 ( )
A.X、M两种元素只能形成XzM型化合物
B.由于W、Z、M元素的氢化物相对分子质量依次减小,所以其沸点依次降低
C.X、Y、Z、W的原子半径依次增大
D.元素W和M的某些单质可作为水处理中的消毒剂
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com