
题目列表(包括答案和解析)
11.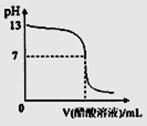 常温下,向10mL 0.1 mol·L-1NaOH溶液中逐滴加入0.1 mol·L-1醋酸溶液,所得滴定曲线如下图所示。下列说法正确的是 ( )
常温下,向10mL 0.1 mol·L-1NaOH溶液中逐滴加入0.1 mol·L-1醋酸溶液,所得滴定曲线如下图所示。下列说法正确的是 ( )
A.pH=7时,所加醋酸溶液的体积为10mL
B.pH<7时,溶液中:c(CH3COO-)>c(Na+)
C.7<pH<13时,溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.继续滴加0.1 mol·L-1醋酸溶液,溶液pH可以变为1
[答案]B
[解析]当NaOH溶液和醋酸恰好完全反应时,生成醋酸钠水解而使溶液显碱性,故A错。当pH<7时有c(H+)>c(OH-),根据电荷守恒可得c(CH3COO-)>c(Na+),故B正确。当7<pH<13时,溶液也有c(Na+)> c(OH-)> c(CH3COO-)>c(H+)这一种情况,C错。对于选项D可作一极端设想,若溶液就是0.1 mol·L-1醋酸,由于醋酸是弱酸,溶液的pH也大于1,故D也错。
[考点]电解质溶液--离子浓度的大小比较
10.下列化学原理表述正确的是 ( )
A.氢硫酸溶液加水稀释,电离程度增大,H+浓度增大
B.Na2CO3溶液中满足:c(Na+)=2c(CO32-)+2 c(HCO3-)+ 2c(H2CO3)
C.NaHCO3溶液不显中性的原因:HCO3-+H2O CO32-+H3O+
CO32-+H3O+
D.同体积同pH的盐酸和醋酸,与足量的锌反应,盐酸的反应速率快,生成H2的物质的量多
[答案]B
[解析]氢硫酸溶液加水稀释,电离程度增大,但c(H+)会变小,A错。选项B是Na2CO3溶液中的物料守恒式,正确。根据所学知识可知NaHCO3溶液显碱性,说明NaHCO3的水解程度大于电离程度,因此不显中性的原因应用水解方程式表示,而不应用电离方程式表示,C错。由于醋酸是弱酸,故同体积同pH的盐酸和醋酸,醋酸所能提供的n(H+)的多,在反应过程中醋酸的反应速率快,生成H2的物质的量也多,D错。
[考点]电解质溶液--弱电解质的电离与水解
9.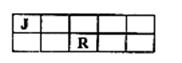 J、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右下表。已知:J元素最低负化合价的绝对值与其原子最外层电子数相等,M是地壳中含量最多的金属元素。下列说法错误的是 ( )
J、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右下表。已知:J元素最低负化合价的绝对值与其原子最外层电子数相等,M是地壳中含量最多的金属元素。下列说法错误的是 ( )
A.J和氢组成的化合物分子中只含有极性共价键
B.工业上用电解熔融的M的氧化物方法来制备M
C.R、T两元素的气态氢化物中,T的气态氢化物更稳定
D.J、M、R、T元素最高价氧化物对应的水化物中酸性最强的是HTO4
[答案]A
[解析]已知四种元素均是短周期元素,故J必为第二周期元素,由于J元素最低负化合价的绝对值与其原子最外层电子数相等,故J为第二周期第IVA元素碳,由此可知R为S,考虑到J、M、R、T是原子序数依次增大的短周期主族元素,故T必为Cl。由M是地壳中含量最多的金属元素,故M为Al。对于选项A,考试到碳和氢可组成种类繁多的烃类,如C2H4、C2H6等,它们的分子中既存在极性键又存在非极性键,故A错。
[考点]物质结构 元素周期律--“位--构--性”的综合考查
8. 用NA表示阿伏加德罗常数。下列说法中,正确的是 ( )
A.1.8g重水(D2O)中含有的质子数为1.0 NA
B.500℃、30MPa下:N2(g)+3H2(g) 2NH3(g);△H=-38.6kJ·mol-1;将1.5NA的H2和过量N2在此条件下充分反应,放出热量19.3kJ
2NH3(g);△H=-38.6kJ·mol-1;将1.5NA的H2和过量N2在此条件下充分反应,放出热量19.3kJ
C.标准状况下,11.2 L Cl2通入足量的石灰乳中制备漂白粉,转移的电子数为0.5NA
D.60 g石英晶体中含有的Si-O键数目为2NA
[答案]C
[解析]重水的摩尔质量为20 g·mol-1,一个重水分子中含有10个质子,故1.8g重水中含有的质子数为1.8×10×NA /20=0.9NA,故A错。可逆反应中的反应热表示该反应完全进行到底时的热效应,由于1.5mol的H2在合成氨反应中不可能完全完全转化,因此放出的热量必小于19.3kJ,故B错。由于SiO2是呈空间网状的正四面体结构,60 g石英相当于1molSiO2,含有的Si-O键数目应为4NA,故D错。
[考点]化学用语及常用计量--阿氏常数
7.下列叙述不正确的是 ( )
A.漂白粉的有效成分是Ca(ClO)2 B.胆矾的成分是CuSO4·5H2O
C.医疗上用的“钡餐”成分是BaSO4 D.光导纤维主要成分是Si
[答案]D
[解析]光导纤维主要成分是SiO2而不是单质Si。
[考点]物质的组成、性质和分类--重要无机物的组成和用途
21.(每空2分,共10分)已知S1O2、SO2和CO2都是酸性氧化物,化学性质具有一定的相似性;Mg和Na的化学性质也具有一定相似性。
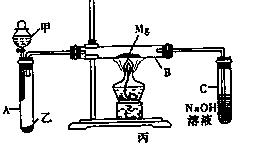
I.用如图所示装置进行Mg与S02反应的实验。
(1)选择制取SO=2的合适试剂 。
①10%的H2SO4溶液 ②80%的H2SO4溶液
③Na2SO3固体 ④CaSO3固体
(2)写出装置B中发生的主要反应的化学方程式 。
(3)该装置还有不足之处,除在A和B之间缺少干燥装置外,还有一处 。
Ⅱ.某研究小组进行了“实验室制Si”的研究,他们以课本为基础,查阅料得到以下可供参考的信息:
①工业上在高温时用C还原SiO2可制得Si
②Mg在点燃的条件下即可与SiO2反应
③金属硅化物与稀H2SO4反应生成硫酸盐与SiH4
④Si和S1O2均不与稀H2SO4反应
⑤S1H4在空气中自燃
他们在研究报告中记载着“……选用合适的物质在适宜的条件下充分应;再用足量稀硫酸溶解固体产物;然后过滤、洗涤、干燥;最后称量…在用稀硫酸溶解固体产物时,发现有爆鸣声和火花,其产率也只有预值的63%左右”。
(1)该小组“实验室制Si”的化学方程式是 。
(2)你估计“用稀硫酸溶解固体产物时,发现有爆鸣声和火花”的原因是
。

20.(每空2分,共10分)几种中学化学常见的单质及其化合物相互转化的关系图如下:
可供参考的信息有:
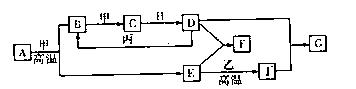
①甲、乙、丙、丁为单质,其余为化合物。
②A由X和Y两种元素组成,其原子个数比为1:2,元素质量之比为7 2 8。
③B气体是引起酸雨的主要物质,H常温下为无色无味的液体,E常用作红色油漆和涂料。
试根据上述信息回答下列问题:
(1)A的化学式为 ,每反应Imol的A转移的电子数为 mol。
(2)F与丁单质也可以化合生成G,试写出该反应的离子方程式: .
(3)少量F的饱和溶液分别滴加到下列物质中,得到三种分散系①、②、③。
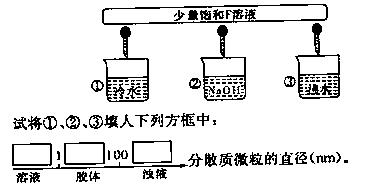
(4)化合物M与H组成元素相同,可以将G氧化为F,且不引进新的离子。试写出M在酸性环境下将G氧化为F的离子方程式: 。
19.(每空2分,共14分)向体积为2L的固定密闭容器中通人3mol X气体,在一定温度下发生如下反应:2X(g) Y(g)+3Z(g)
Y(g)+3Z(g)
(1)经5min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y表示的速率为 mol/(L·min)。
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一段时间内测得容器内的反应速率分别为:甲:v(X)=3.5 mol/(L·min);乙:v(Y)=2 mol/(L·min);丙:v(Z)=4.5 mol/(L·min);丁:v(X)=0.075 mol/(L·s)。若其它条件相同,温度不同,则温度由高到低的顺序是(填序号) 。
(3)若向达到(1)的平衡体系中充人氮气,则平衡向 (填“左”或“右”或“不”>移动;若向达到(1)的平衡体系中移走部分混合气体,则平衡向 .(填“左”或“右”或“不”)移动。
(4)若在相同条件下向达到(1)所述的平衡体系中再充入0.5mol X气体,则平衡后X的转化率与(1)的平衡中X的转化率相比较: 。
A.无法确定 B.前者一定大于后者
C.前者一定等于后者 D.前者一定小于后者
(5)若保持温度和压强不变,起始时加入X、Y、Z物质的量分别为a mol、b mol、c mol,达到平衡时仍与(1)的平衡等效,则a、b、c应该满足的关系为
(6)若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为a mol、b mol、c mol,到平衡时仍与(1)的平衡等效,且起始时维持化学反应向逆反应方向进行,则c的取值范围应该为 。
18.(每空2分,共8分)氮是地球上含量最丰富
的一种元素,氮及其化合物在工农业生产、生
活中有着重要作用。请回答下列问题:
(1)右图是1mol NO2和1mol CO反应生成CO2
和NO过程中能量变化示意图,请写出NO2
和CO反应的热化学方程式 。
(2)在0.5L的密闭容器中,一定量的氮气和氢气进行如下化学反应:
N2(g)+3H2(g) 2NH3(g)△H<O,其化学平衡常数K与温度t的关系如下表:
2NH3(g)△H<O,其化学平衡常数K与温度t的关系如下表:
|
t/℃ |
200 |
300 |
400 |
|
K |
K1 |
K2 |
0.5 |
请完成下列问题;
①试比较K1、K2的大小,K1____K2(填写“>”、“=”或“<”);
②400℃时,反应2NH3(g) N2(g)+3H=2(g)的化学平衡常数的值为_
___。
N2(g)+3H=2(g)的化学平衡常数的值为_
___。
当测得NH3和N2、H2的物质的量分别为3mol和2mol、1mol时,则该反应的v(N2)(正)____v(N2)(逆)(填写“>”、“=”或“<”)。
17.(每空2分,共10分)W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素。
(1)W、X的最高价氧化物对应的水化物可以反应生成盐和水,该反应的离子方程式为:
(2)W与Y可形成化合物W2Y,该化合物电子式为;其水溶液pH=8,则c(HY-)+2c(H2Y)= (填精确值)。
 (3)将Y的低价氧化物通人W的最高价氧化物对应水化物中,经充分反应后,所得溶液呈中性,则混合溶液中的溶质主要为
;溶液中c(W+)=
。
(3)将Y的低价氧化物通人W的最高价氧化物对应水化物中,经充分反应后,所得溶液呈中性,则混合溶液中的溶质主要为
;溶液中c(W+)=
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com