
题目列表(包括答案和解析)
14.常温下,将0.1 mol·L-1氢氧化钠溶液与0.06 mol·L-1硫酸溶液等体积混合,该混合溶液的pH等于 ( )
A.1.7 B.2.0 C.12.0 D.12.4
13. 低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:
低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:
2NH3(g)+NO(g)+NO2(g) 2N2(g)+3H2O(g);ΔH<0,在恒容密闭容器中,下列有关说法正确的是 ( )
A.平衡时,其他条件不变,升高温度可使正反应速率减小,平衡逆向移动
B.平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小
C.单位时间内消耗NO和N2的物质的量比为1∶2时,反应达到平衡
D.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
12.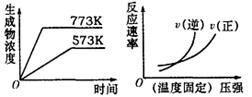 下列反应中符合下图图象的是 ( )
下列反应中符合下图图象的是 ( )
A.N2(g)+3H2(g) 2NH3(g);
2NH3(g);
△H=-Q1kJ·mol-1 (Q1>0)
B.2SO3(g) 2SO2(g)+O2(g);
2SO2(g)+O2(g);
△H=+Q2kJ·mol-1 (Q2>0)
C.4NH3(g)+5O2(g) 4NO(g)+6H2O(g);△H=-Q3kJ·mol-1(Q3>0)
4NO(g)+6H2O(g);△H=-Q3kJ·mol-1(Q3>0)
D.H2(g)+CO(g) C(s)+H2O(g);△H=+Q4kJ·mol-1-1(Q4>0)
C(s)+H2O(g);△H=+Q4kJ·mol-1-1(Q4>0)
11.体积相同的盐酸和醋酸两种溶液,n(Cl-)=n(CH3COO-)=0.01mol,下列叙述错误的是( )
A.它们分别与足量CaCO3反应时,放出的CO2一样多
B.它们与NaOH完全中和时,醋酸溶液所消耗的NaOH多
C.两种溶液的pH相同 D.分别用水稀释相同倍数时,n(Cl-)<n(CH3COO-)
10.一定温度下,用水稀释0.1mol·L-1的一元弱酸HA,随稀释进行,下列数值一定增大的是(Kw表示水的离子积,Ka表示HA的电离常数) ( )
A.Kw B.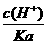 C.
C.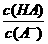 D.c(OH-)
D.c(OH-)
9.短周期元素W 、X、Y、Z的原子序数依次增大,且W 、X、Y+、Z的最外层电子数与其电子层数的比值依次为2 、3、4、2(不考虑零族元素)。下列关于这些元素的叙述错误的是( )
A.X和其他三种元素均可形成至少2种二元化合物
B.W和X、Z两种元素分别形成的二元化合物中,均有直线形分子
C.W 、X和Y三种元素可以形成其水溶液呈碱性的化合物
D.Z和其他三种元素形成的二元化合物,其水溶液均呈酸性
8.下列说法或表示方法正确的是 ( )
A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由H+(aq)+OH-(aq)===H2O(l);△H=-57.3kJ·mol-1可知,若将含1 mol CH3COOH的稀溶液与含1 mol NaOH的稀溶液混合,放出的热量小于57.3 kJ
C.由C(石墨)===C(金刚石);△H= +1.90 kJ·mol-1可知,金刚石比石墨稳定
D.500℃、30MPa下,将0.5molN2(g)和1.5mol H2(g)置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g);△H=-38.6kJ·mol-1
2NH3(g);△H=-38.6kJ·mol-1
7.下列溶液中离子浓度的关系正确的是 ( )
A.0.1 mol·L-1NaHA溶液,其pH等于4:c(HA-)> c(A2-) > c(H2A)
B.0.1 mol·L-1Na2CO3溶液:c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-)
C.加入适量CH3COONa(s)的0.1 mol·L-1CH3COOH溶液,其pH<7:
c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D.相同温度下,pH=12的NaOH溶液和pH=12的CH3COONa溶液中,由水电离产生的
c(OH-)相等。
6.一定条件下,CH3COONa溶液存在水解平衡:CH3COO-+H2O CH3COOH+OH-;下列说法正确的是 ( )
CH3COOH+OH-;下列说法正确的是 ( )
A.加入少量NaOH固体,c(CH3COO-)减小
B.升高温度,溶液的pH增大
C.稀释溶液,溶液的pH增大
D.通入少量HCl气体,水解平衡常数减小
5.用NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
A.25℃时,pH=13的1L Ba(OH)2溶液中含有OH-数目为0.1NA
B.200mL 5mol·L-1Na2S溶液中,含NA个S2-
C.常温下,pH=12的1L氨水中含有的NH3·H2O分子数是0.01 NA
D.电解精炼铜时,若阴极得到电子数为2NA个,则阳极质量减少64g
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com