
题目列表(包括答案和解析)
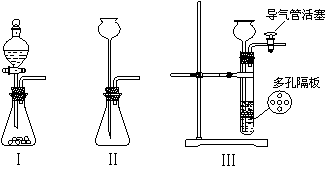
22. (12分)某兴趣小组的学生根据活泼金属Mg与CO2发生反应,推测活泼金属钠也能与CO2发生反应,因此兴趣小组用下列装置进行“钠与二氧化碳反应”的实验探究(尾气处理装置已略去)。已知:常温下,CO能使一些化合物中的金属离子还原
 例如:PdCl2 + CO +
H2O=Pd↓+ CO2
+2HCl 。反应生成黑色的金属钯,此反应也可用来检测微量CO的存在。
例如:PdCl2 + CO +
H2O=Pd↓+ CO2
+2HCl 。反应生成黑色的金属钯,此反应也可用来检测微量CO的存在。
请回答下列问题:
(1)通常实验室制取CO2气体的离子方程式是 ,为了使制气装置能“随开随用,随关随停”,上图A处应选用的装置是___ (填写 “Ⅰ”、“Ⅱ”或“Ⅲ”)。
(2)观察实验装置图可知Na与CO2反应的条件是_____________。检查装置的气密性完好并装入药品后,在点燃酒精喷灯前,必须进行的操作是____________________,这步操作的目的是 。
(3)假设CO2气体为足量,在实验过程中分别产生以下①、②两种不同情况,请分析并回答问题:
①若装置F中溶液无明显变化,装置D中生成两种固体物质,取少量固体生成物与盐酸反应后,有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是 。
②若装置F中有黑色沉淀生成,装置D中只生成一种固体物质,取少量该固体与盐酸反应后,也有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是 。
(4)请用文字简要说明你判断②中D装置生成固体的成分是钠的正盐或酸式盐的理由。 。
21.(9分)A+B→X+Y+H2O(未配平,反应条件略去)是中学常见反应的化学方程式,其中A、B的物质的量之比为1:4。请回答:
(1)若Y是黄绿色气体,则Y的电子式是 ,该反应的化学方程式是:
。
(2)若A为非金属单质,构成它的原子核外最外层电子数是次外层电子数的2倍,B的溶液为某浓酸,则反应中氧化剂与还原剂的物质的量之比是 。
(3)若A为金属单质,常温下A在B的浓溶液中“钝化”,且A可溶于X溶液中
①A元素在周期表中的位置是 (填所在周期和族);Y的化学式是 。
②含a mol X的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量恰好相等,则被还原的X是
mol。
(4)若A、B、X、Y均为化合物。A溶于水电离出的阳离子和水作用的生成物可净化水,向A溶液中加入硝酸酸化的AgNO3溶液,产生白色沉淀;B的焰色为黄色。则A与B按物质的量之比1:4恰好反应后,溶液中离子浓度从大到小的顺序是 。
20. 25℃时,某硫酸铜溶液的溶质质量分数为w,物质的量浓度为cmol/L,密度为ρg/mL,将此溶液蒸去a g水或再向原溶液中加入b g无水硫酸铜粉末,充分静置并恢复至25℃时,均恰好全部转化为CuSO4·5H2O晶体。则下列关系式正确的是 ( )
A.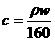 B.
B.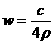 C.
C.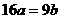 D.
D.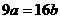
第Ⅱ卷(非选择题 共40分)
( 共4题,共40分 )
19.关于下列各图的叙述正确的是 ( )
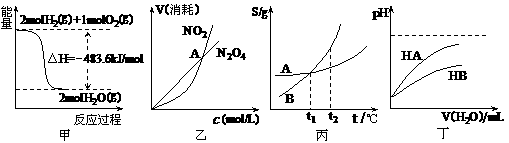
A.甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6kJ·mol-1
B.乙表示恒温恒容条件下发生的可逆反应2NO2 N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
C.丙表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由t1℃升温至t2℃时,溶质的质量分数B>A
D.丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液
18.铅蓄电池是典型的可充电电池,在现代生活中有着广泛的应用,其充电、放电按下式进行:
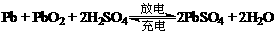
有关该电池的说法正确的是 ( )
A. 充电时,铅蓄电池的负极与外接电源的负极相连
B. 充电时,阳极反应:PbSO4 +2e- = Pb + SO42-
C. 放电时,每通过1mol电子,蓄电池就要消耗2mol H2SO4
D. 放电时,蓄电池内电路中H+ 向负极移动
17.近年来,我国储氢碳纳米管研究获重大进展,电弧法合成的碳纳米管,常伴有大量的碳纳米颗粒生成。这种碳纳米颗粒可用氧化气化法提纯。其反应的离子方程式为(其中a、b、c、d、e 、f为反应计量数):aC + bCr2O72-+ cH+ = dCO2↑+ eCr3+ + f H2O。有关上述反应的叙述中正确的是 ( )
A.当a = 3时,e = 2
B.反应中既可用稀硫酸又可用浓硝酸酸化
C.若产生11 g气体物质,则有6.02×1023个电子发生转移
D.反应计量数b、c、e有如下关系:3e =2b + c
16.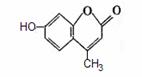 香豆素-4是一种激光染料,应用于可调谐染料激光器,其结构简式如图,下列有关叙述正确的是
香豆素-4是一种激光染料,应用于可调谐染料激光器,其结构简式如图,下列有关叙述正确的是
( )
A.分子式为C10H9O3
B. 不能使酸性KMnO4溶液褪色
C. 1mol香豆素-4最多能与含2molNaOH的溶液反应
D. 能与溴水发生取代反应、加成反应
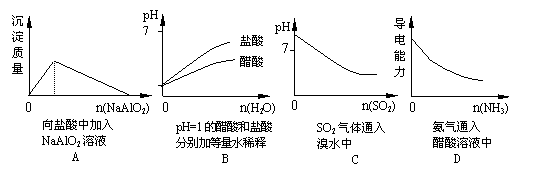
15.下列实验过程中产生的现象与对应图形相符合的是 ( )
14.三氟化氮(NF3)是微电子工业中一种优良的等离子蚀刻气体。它无色、无臭,在潮湿的空气中能发生下列反应:3NF3+5H2O=2NO+HNO3+9HF,下列有关说法正确的是
A.反应中NF3是氧化剂,H2O是还原剂 ( )
B.反应中被氧化与被还原的原子物质的量之比为2∶1
C.若反应中生成0.2mol HNO3,则反应共转移0.2mol e-
D.NF3在潮湿的空气中泄漏会产生白雾、红棕色气体等现象
13.下列各溶液中,有关成分的物质的量浓度关系正确的是 ( )
A.10mL 0.5mol/L CH3COONa溶液与6mL 1mol/L盐酸混合:
c(Cl-)>c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
B.0.1mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
C.硫酸氢铵溶液中滴加氢氧化钠至溶液恰好呈中性:
c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
D.pH相等的(NH4)2SO4溶液,(NH4)2Fe (SO4)2溶液和NH4Cl溶液:
c[(NH4)2SO4]<c[(NH4)2Fe (SO4)2]<c(NH4Cl)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com