
题目列表(包括答案和解析)
8、下列化学用语书写正确的是 ( )
A、次氯酸的电离方程式:HClO === H+ + ClO-
B、铝溶于烧碱溶液的离子方程式:Al + OH- + 3H2O == [Al(OH)4]- + H2↑
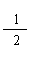 C、在298K时,1 molH2(g)和0.5 mol O2(g)反应生成1 molH2O(l)放热285.8kJ,此反应的热化学方程式为: H2(g) + O2(g)== H2O(l) △H= -285.8kJ/mol
C、在298K时,1 molH2(g)和0.5 mol O2(g)反应生成1 molH2O(l)放热285.8kJ,此反应的热化学方程式为: H2(g) + O2(g)== H2O(l) △H= -285.8kJ/mol
D、电解精炼铜的阴极反应式:Cu -2e- == Cu2+
7、食盐、食醋、纯碱等均为家庭厨房中常用的物质,利用这些物质不能完成的家庭小实验是 ( )
A、检验自来水中是否含Cl- B、鉴别食盐和纯碱
C、检验蛋壳能否溶于酸 D、除去热水瓶内壁上的水垢
6、下列实验设计不合理的是 ( )
A、配制FeCl3溶液时,需加入少量稀盐酸
B、用硝酸清除CO还原CuO的实验中在试管内壁附着的铜
C、用KMnO4溶液除去C2H4气体中的少量CH4
D、往FeCl2溶液中滴入KSCN溶液,检验FeCl2是否已氧化变质
5、 可一次性鉴别氯化镁、氯化铝、碳酸钾等三种溶液的试剂是 ( )
A、Ba(NO3)2 溶液 B、AgNO3溶液 C、NaOH溶液 D、CH3COOH溶液
4、 设NA为阿伏伽德罗常数,下列叙述正确的是
( )
设NA为阿伏伽德罗常数,下列叙述正确的是
( )
 A. 24g镁的原子量最外层电子数为NA B. 1L0.1mol·L-1盐酸溶液中H+数为0.1NA
A. 24g镁的原子量最外层电子数为NA B. 1L0.1mol·L-1盐酸溶液中H+数为0.1NA
 C. 1mol甲烷分子所含质子数为16NA D. 标准状况下,22.4L乙醇的分子数为NA
C. 1mol甲烷分子所含质子数为16NA D. 标准状况下,22.4L乙醇的分子数为NA
3、下列关于.物质用途的叙述中,不正确的是 ( )
A、硅可以用做制造变压器的铁芯材料 B、二氧化硅可用于制造光导纤维
C、石墨可用做绝缘材料 D、石英玻璃可用于制造光学仪器
2、在溶液中加入足量Na2O2后仍能大量共存的离子组是 ( )
A、NH4+、Ba2+、Cl-、NO3- B、Ca2+、Mg2+、NO3-、HCO3-
C、K+、AlO2-、Cl-、SO42- D、 Na+、Cl-、CO32-、SO32-
1、下列化学观点中,不正确的是 ( )
A、化学的主要特点是在原子、分子水平上认识物质,了解化学可以识别和创造分子
B、一种元素不仅可以有多种离子,还可以有多种原子和分子
C、根据分散系是否具有丁达尔现象,将分散系分为溶液、胶体和浊液
D、对物质进行科学的分类,有助于我们进一步研究物质的结构、性质和用途
31.大多金属碳化物能与水剧烈反应,生成相应氢氧化物和气态烃,如:
Na4C+4H2O→4NaOH+CH4↑, MgC2+2H2O→Mg(OH)2+C2H2↑
现有CaC2与某常见金属碳化物A的混合物,与足量盐酸反应,得一澄清溶液,并有大量气体产生,将气体通过碱石灰干燥除杂后,测其体积为V1,将所得气体充分燃烧,生成的CO2的体积为V2,相同条件下,V1:V2=5:7:向澄清溶液中逐渐加入足量Na2CO3溶液后,再继续加入NaOH溶液,沉淀物质的量变化如下图所示,试回答下列问题:
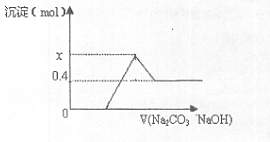
(1)已知A中的金属元素是短周期元素,则该元素是: (写元素符号),写出CaC2与浓盐酸反应的化学方程式: ;
(2)根据Vl:V2=5:7,可算出混合烃中平均每Imol烃分子含有____mol C,由此可知气态混合烃中含有乙炔和 ,
(3)A的化学式为 ;
(4)原混合物中CaC2的物质的量为 mol, A的质量为 g。



30.氯化亚铜(CuCl)是重要的化工原料。国家标准规定合格的CuCI产品的主要质量指标为CuCI的质量分数大于96.50%工业上常用下列反应制备CuC1
2CuSO4+Na2SO3+2NaCl+Na2CO3→2CuC1↓+3Na2SO4+CO2↑
(l)CuC1制备过程中需要配置质量分数为20.0%的CuSO4溶液,试计算配制该溶液所需的CuSO4·5H2O与H2O的物质的量之比。
(2)准确称取所醌置的0.2500g CuCI样品置于一定量的0.5mol·L-1FeCl3溶液中,待样品完全溶解后,加水20mL,用0.l000mol·L-1的Ce(SO4)2溶液滴定到终点,消耗24.00mLCe(SO4)2溶液。有关反化学反应为:Fe3++CuCl→Fe2++Cu2++Cl-;
Ce4++Fe2+→Fe3+Ce3+
通过计算说明上述样品中CuCl’的质量分数是否符合标准。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com