
题目列表(包括答案和解析)
6. 研究外界条件对金属钠和氧气反应的产物的影响采用的方法是 A.分类法 B. 观察法 C.实验法 D.推理法
5.氨水中存在着下列平衡:NH3·H2O NH
NH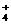 +OH-,若要使平衡向逆反应方向移动,同时使[OH-]增大,应加入的物质是
+OH-,若要使平衡向逆反应方向移动,同时使[OH-]增大,应加入的物质是
A. NH4Cl固体 B. 硫酸 C. NaOH固体 D. 水
4.颜色不褪去的是
A.酸性高锰钾溶液加入亚硫酸溶液 B.品红溶液中通入二氧化硫
C. 鲜花通入干燥的氯气 D.溴水通入二氧化碳
3.在Cu2S+2Cu2O=6Cu+SO2↑反应中,说法正确的是
A.Cu2S在反应中既是氧化剂,又是还原剂 B.Cu是氧化产物
C.氧化剂只有Cu2O D.生成1mol Cu,反应中转移2mol电子
2.下列关于酸、碱、盐、氧化物的元素组成的说法中,正确的是
A.酸、碱一定含有氢,盐一定不含氢 B.碱、盐可能含氧,酸一定含氧
C.酸、碱、盐可能都不含金属元素 D.金属氧化物一定是碱性氧化物
1. “温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体。下列方法
不能控制和治理CO2解决温室效应的是
A.减少化石燃料的使用 B.植树造林,增大植被面积
C.尽量用木材作燃料 D.利用太阳能、风能
29. (12分) .有机物A 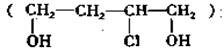 是合成高分子化合物HPMA的中间体,HPMA可用于锅炉阻垢剂。
是合成高分子化合物HPMA的中间体,HPMA可用于锅炉阻垢剂。
(1)有机物A能够发生的反应有: (填写字母)
a.取代反应 b.加成 c.消去反应 .
(2)有机物A在Cu做催化剂和加热条件下,与氧气反应生成有机物B。B中含有的官能团除-Cl以外,还含有的官能团是: 。

 (3)有机物B经氧化后生成有机物C,C可有如下图所示的转化关系:
(3)有机物B经氧化后生成有机物C,C可有如下图所示的转化关系:
写出E的结构简式: ;
(4)D在高温、高压和催化剂作用下反应生成HPMA,写出反应的化学方程
式 ;
(5)F是E的一种同分异构体。0.1mol F与足量金属Na反应放出3.36L H2
(标准状况下);0.1mol F与足量NaHCO3反应放出2.24L CO2(标准状况下);
F能发生银镜反应。F的结构简式可能是: 、
。
28.(12分)市场销售的某种食用精制盐包装袋上有如下说明:
|
产品标准 |
GB5461 |
|
产品等级 |
一级 |
|
配料 |
食盐、碘酸钾、抗结剂 |
|
碘含量(以I计) |
20-50 mg/kg |
|
分装日期 |
|
|
分装企业 |
|
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学
计量数填于空白处):
___KIO3+___KI+___H2SO4 =___K2SO4+___I2+___H2O
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3
稀溶液将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的离子方程式是 。
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体。
以上设计中遗漏的操作及在上述步骤中的位置是______________ ____ 。
(3)已知:I2+2S2O32- = 2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂,逐滴加入物质的量浓度为2.0×10-3 mol/L的Na2S2O3
溶液10.0 mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是 。[
②b中反应所产生的I2的物质的量是 mol。
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示)_________________mg/kg。
27.(14分)下列物质有如下转化关系(有的反应物生成物未列出),其中:D为碱,G为酸,金属甲在G的浓溶液中会钝化;F的溶液中只含一种溶质。
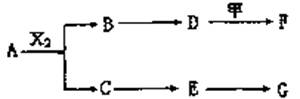
A、B、C、D、E均由Q、R、X、T四种短周期元素中的两种或三种组成,且Q、R、X、T原子序数依次增大;X的最外层电子数是电子层数的3倍;R和X相邻;Q和T同主族,Q为非金属元素,T为金属元素。则:
(1)X是 ,在周期表中的位置是 ,R、X、T的原子半径从小到大的顺序为 (用元素符号表示);
(2)A和G等物质的量反应产物的水溶液显 性,其原因用离子方程式表示为 ;
(3)A和X2反应的化学方程式为 ;
(4)为保护环境,通过安装汽车尾气处理装置,使尾气中的E和CO反应转化为两种空气的成分,当反应转移l mol电子时,生成的气体在标准状况下的总体积为 L。
26.(12分)一瓶澄清透明的溶液,可能含有下列离子中的一种或几种:Fe2+、Fe3+、Ba2+、Al3+、NH4+、SO42-、 HCO3-、NO3-、Cl-取溶液进行如下实验:
①溶液滴在蓝色石蕊试纸上,试纸呈红色。
②取少量溶液浓缩后加入铜片和浓硫酸共热,有红棕色气体生成。
③取少量溶液,加入用硝酸酸化的氯化钡溶液,产生白色沉淀。
④另将③中的沉淀过滤出,滤液中加入硝酸银溶液,生成白色沉淀
⑤另取原溶液,逐滴加入氢氧化钠溶液至过量,并加热,无气体产生,但看到生成沉淀,随之该沉淀部分溶解,且呈红褐色。根据上述实验现象推断:
(1)由①说明溶液呈 性,⑤中红褐色沉淀为 (写出化学式 )
(2)溶液中肯定存在的离子有 。
(3)溶液中肯定不存在的离子有 。
(4)溶液中不能确定是否存在的离子有 。
(5)对上述实验操作做何改进,才能确定(3)中的离子是否存在
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com