
题目列表(包括答案和解析)
7.在标准状况下,将1.12L由X、Y组成的混合气体用水全部吸收得到1L溶液,测得溶液的PH=1,则X、Y及其体积比可能是
A.H2、Cl2:1:1 B.NO2、O2:4:1 C.HCl、HBr:1:1 D.Cl2、SO2:1:1
6.X元素的一个原子失去2个电子转移到Y元素的2个原子中去,形成离子化合物Z,下列说法中正确的是
A.Z的电子式为::Y:X:Y: B.X元素一定是第IIA族元素
C.Z不能电离 D.Z与Y两种元素的单质反应生成的化合物也可能为XY3
5.在下列物质中,含有分子数目最多的是
A.22.4LH2(标准状况) B.1000g质量分数为4.6%的酒精溶液
C.3.01×1023个Cl2 D.117gNaCl
4.下列说法正确的是
A.常温常压下呈固态的含有共价键的晶体一定是原子晶体
B.L层电子为奇数的所有元素所在族的序数与该元素原子的L层电子数相等
C.同一周期从左至右原子半径逐渐减小
D.构成单质分子的微粒一定含有共价键
3.38.4g铜与过量稀硝酸充分反应,发生氧化还原反应的HNO3的物质的量为
A.1.2mol B.1.6mol C.0.4mol D.0.2mol
2.今有下列物质:①Na2O ②Li2O2 ③CO ④SO3 ⑤H2Te ⑥CuS ⑦FeCl3 ⑧FeI3不能由两种单质直接化合生成的是
A.④⑤⑥ B.①③④⑤⑧ C.②④⑤⑥⑧ D.②③④⑤⑦⑧
1.下列分子中,具有非极性键的非极性分子是
A.CH4 B.C2H2 C.H2O2 D.CO2
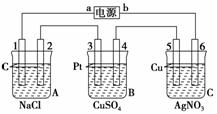
25.如下图,通电5 min后,电极5质量增加2.16 g,如果B池中共收集到224 mL气体(标准状况),且溶液体积为200 mL(设电解过程中溶液体积不变),求通电前溶液中Cu2+的物质的量浓度?
24.(16分)过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用于消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。
Ⅰ.测定过氧化氢的含量
请填写下列空白:
(1)移取10.00 mL密度为ρ g/mL的过氧化氢溶液至250 mL________(填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00 mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在横线上。
____MnO4- + ____ H2O2 + ____ H+ =____ Mn2++____ H2O + ___ _____
(3)滴定时,将高锰酸钾标准溶液注入________(填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是__________________________________________________。
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为________。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果________(填“偏高”或“偏低”或“不变”)。
Ⅱ.探究过氧化氢的性质
该化学兴趣小组根据所提供的试剂设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(试剂:①过氧化氢溶液、②氯水、③高锰酸钾溶液、④饱和硫化氢溶液、⑤MnO2,实验仪器及用品可自选)
(1)若要证明过氧化氢的氧化性,应选用的试剂为________(填序号),相应的化学方程式为__________________________。
(2)证明过氧化氢不稳定性的实验方法为__________________________________________
_____________________________________________________________________________
23.(12分)在中学化学实验室中,可通过如右图所示的方法制得一种常见的有毒气体Z。
X是黑色粉末,Y是白色固体(焰色反应透过蓝色钴玻璃呈紫色,可用于制备火柴),且都是常见的氧化剂。
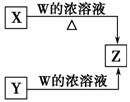 (1)写出X与W的浓溶液共热生成Z的离子方程式:
(1)写出X与W的浓溶液共热生成Z的离子方程式:
__________________________________________。
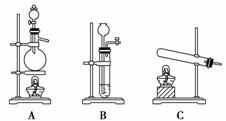
(2)X与Y混合后共热可产生一种无毒气体,反应的化学方程式
为____________________,下图是实验室常见的气体发生装
置,此反应应选用的发生装置是________(填字母编号),X与W的浓溶液制取Z应选用的发生装置是________(填字母编号)。

(3)在实验室中制取气体Z时,通常可用排某种溶液的方法收集Z,则该溶液是________;
也可用排空气集气法收集Z,若用右图装置(不能改变瓶口朝向),
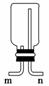 则气体应该从________(填“m”或“n”)口进。
则气体应该从________(填“m”或“n”)口进。
(4)有人设想利用原电池原理以Z和氢气制备一种重要的化工原料,同时
获取电能。假设这种想法可行,用石墨作电极材料,用稀盐酸作电解质
溶液,则通入Z的电极为原电池的 ________极,其电极反应式为
______________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com