
题目列表(包括答案和解析)
5.下面说法,其中正确的是 ( )
A.凡是生成两种或两种以上物质的反应都是分解反应
B.一种元素可能有多种氧化物,但一种化合价只对应一种氧化物
C.有些化学反应不属于化合、分解、置换、复分解反应中的任何一种反应
D.直径介于1nm~10nm之间的微粒称为胶体
4.下列叙述中正确的是 ( )
A.除零族元素外,短周期元素的最高化合价在数值上都等于该元素所属的族序数
B.除短周期外,其他周期均有18种元素
C.副族元素中没有非金属元素
D.碱金属元素是指ⅠA族的所有元素
3.下列说法正确的是 ( )
A.发酵粉中主要含有氢氧化钠,能使焙制出的糕点疏松多孔
B.含碘食盐中的碘元素遇淀粉溶液变蓝
C.日常生活中常用75%乙醇溶液来杀菌消毒
D.硫酸氢钠属于盐类,是强酸强碱盐,其水溶液显中性
2.氮气是空气中的主要成分,且含量很大,现已有科学家设计出了液氮蒸汽机,即利用液氮的蒸发来驱动机车,从而达到保护环境的目的。其主要依据是 ( )
A.液氮的沸点为-195.8°C,远低于常温 B.氮气与氧气反应放热
C.氮气在空气中燃烧放热 D.氮气在空气中约78%(体积分数)
1.K2O、KOH、K2CO3、KCl、K2SO4可按某种标准划为同一类物质,①钾的化合物②钾盐 ③钾的含氧化合物 ④电解质 ⑤能与硝酸反应的物质 ⑥溶于水并形成溶液的物质
下列分类标准正确的是 ( )
A.①④⑥ B.①②③④⑤⑥ C.②④⑤⑥ D.①②④⑤
2011。。l
本试卷分选择题和非选择题两部分,共120分。考试用时l00分钟。
(二)选考题:共15分。请考生从给出的2道化学题中任选一题作答,并用2B铅笔在答题卡上把所选题目的题号涂黑。注意所做题目的题号必须与所涂题目的题号一致,在答题卡上选答区域指定位置答题。如果多做,则按所做的第一题计分。
11.[化学--选修物质结构与性质](15分)
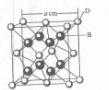
已知A、B、c、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B原子的L层p轨道中有5个电子;C是周期表中1-18列中的第14列元素;D和E属同一周期,又知E原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1,D跟B可形成离子化合物,其晶胞结构如右图。请回答:
(1)A与c形成的共价化合物的分子式是 ,杂化轨道是____,分子的立体结构是____。
(2)B与C比较,电负性较小的是 (填元素符号);B与c形成的化合物晶体类型是 。
(3)E属元素周期表中第 周期,第 族的元素,其元素名称是 ,
它的+2价离子的电子排布式为 。
(4)从图中可以看出,D踉B形成的离子化合物的化学式为 ;若设该晶胞的边长为a cm,则该离子化合物晶体的密度是 (只要求列出算式)。
12.[化学--选修有机化学基础](15分)
有机物A只含有C.H、O三种元素,常用作有机合成的中间体。16. 8g该有机物经燃烧生成44.0g CO2和14.4g H2O;质谱图表明其相对分子质量为84,红外光谱分析表明A分子中含有O-H键和位于分子端的C≡C键,核磁共振氢谱有三个峰,峰面积为6:1:1。
(1)A的分子式是____。A的结构简式是 。
(2)下列物质中,一定条件能与A发生反应的是--。
A.H2 B.Na C.KMnO4 D.Br2
(3)有机物B是A的同分异构体,1mol B可与1mol Br2加成。该有机物所有碳原子在同一个平面,没有顺反异构现象。B中含氧官能团的名称是 ,B的结构简式是____ 。
(4)B可以通过下列变化得到四元环状化合物F
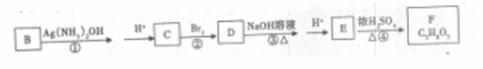
请写出反应③化学方程式 ;
上述转化关系中①、②、④的反应类型是:____ , , 。

(一)必考题(3题,共43分)
8.(15分)“材料”的发现和使用往往会极大地推动生产、生活的发展,一些材料的出现甚至具有里程碑式划时代的意义。请你回答以下问题:
(1)无机非金属材料。高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”。这种材料可以按下列方法制备:
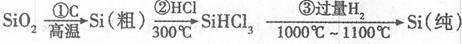
①写出步骤①的化学方程式 。
②步骤②经过冷凝得到的SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHCl3的主要化学操作的名称是 。
(2)磁性材料。这种材料一般含有铁元素,铁是用途最为广泛的金属,也较为活泼,所以从它的使用开始就不断实施着对它的防护。最常见的铁制品腐蚀就是电化学腐蚀,请写出最为普遍的电化学腐蚀的负极反应式 。
(3)激光材料。我国是激光技术先进的国家,红宝石(Al2O3)是最早用于产生激光的材料,它是一种两性氧化物,请用离子方程式加以说明: , 。
(4)纳米材料。胶体是一种物质以“纳米”颗粒的形式分散到另一种物质里形成的分散系,胶体粒子的直经大约是 ,三氯化铁溶液可以加速伤口止血,请简述原因 。
(5)高分子材料。可以分成无机高分子材料和有机高分子材料。一种新型高效净水剂[A1Fe(OH)nCl6-n]m就属于无机高分子材料,广泛应用于生活用水和工业污水处理,其中铁元素的化合价为 ;一种合成纤维腈纶,又称“人造羊毛”,由丙烯腈(CH2==CH-CN)为原料聚合生成,请写出生成该有机高分子材料的化学方程式 。
9.(15分)某矿样含有大量的CuS、少量铁的氧化物及少量其它不溶于酸的杂质。某化学课外小组设计以下流程,以该矿样为原料生产CuCl2•2H2O晶体。
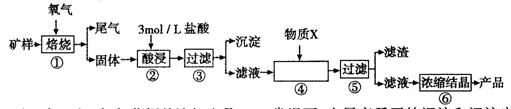
已知:在20℃时,氯化铜的溶解度是73g;常温下,金属离子开始沉淀和沉淀完全时的pH见下表。
|
金属离子 |
开始形成氢氧化物沉淀的pH |
完全形成氢氧化物沉淀的pH |
|
Fe2+ |
7.0 |
9.0 |
|
Fe3+ |
1.9 |
3.2 |
|
Cu2+[来源:高&考%资(源#网] |
4.7 |
6.7 |
 回答下列问题:
回答下列问题:
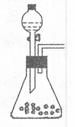
(1)步骤①的焙烧过程中需要通入氧气。在实验室中使用中学化学
常见物质、右图所示装置制取氧气,试写出你熟悉的、符合上
述条件的两个化学方程式
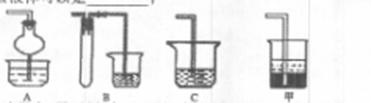
(2)在焙烧过程中还有废气产生,其中一种是主要的大气污染物。
若在实验室中以碱液吸收处理之,下列A、B、C装置中可
行的是____(填字母);若选用甲装置,则烧杯中的下层液体
可以是 (填字母);若选用甲装置,则烧杯中的下层液体可以是 。
(3)步骤②酸浸过程中,需要用到3 mollL的盐酸l00mL,配制该盐酸溶液时,除了用到烧杯、玻璃棒、胶头滴管外,还需要的仪器有____;
(4)步骤④加入物质X的目的是 ,物质X可以选用下列物质中的 ;
A.氧化铜 B.稀盐酸 C.氨水 D.氧化亚铁
(5)在整个生产流程中,共需要进行 次过滤操作。
10.(13分)CO2是目前大气中含量最高的一种温室气体,控制和治理CO2是解决温室效应的有效途径。
(1)其中一种途径是将CO2转化成有机物实现碳循环。如:
2CO2(g)+2H2O(l)===C2 H4 (g)+3O2(g) △H=十1411.0kJ/mol
2CO2(g) +3H2 O(l)=C2 H5OH(1)十3O2(g)△H = +1366.8kJ/mol
则由乙烯水化制乙醇反应的热化学方程式为 。
 (2)在一定条件下,6H2(g)+2CO2(g) CH3CH2OH(g)+3H2O(g)。
(2)在一定条件下,6H2(g)+2CO2(g) CH3CH2OH(g)+3H2O(g)。
 温度(K)
温度(K)CO2转化率(%) n(H2)/n(CO2) |
500 |
600 |
700 |
800 |
|
1.5 |
45 |
33 |
20 |
12 |
|
2 |
60 |
43 |
28 |
15 |
|
3 |
83 |
62 |
37 |
22 |
根据上表中数据分析:
①温度一定时,提高氢碳比[著轰击],CO2的转化率 (填“增大”“减小”
“不变”)。
②该反应的正反应为 (填“吸”或“放”)热反应。
 (3)定条件下,将3 rrlolH2和ImolCO2两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3H2(g)+CO2(g) CH3OH(g)+H2O(g)。2min末该反应达到平衡,测得CH30H的浓度为0.2mol/L。下列判断不正确的是___ _。
(3)定条件下,将3 rrlolH2和ImolCO2两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3H2(g)+CO2(g) CH3OH(g)+H2O(g)。2min末该反应达到平衡,测得CH30H的浓度为0.2mol/L。下列判断不正确的是___ _。
 a.该条件下此反应的化学平衡常数表达式为
a.该条件下此反应的化学平衡常数表达式为
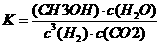
b.H2的平均反应速率为0.3mol/(L.s)
c.CO2的转化率为60%
d.若混合气体的密度不再改变时,该反应一
定达到平衡状态
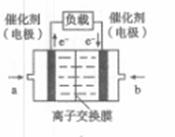
(4)如图是乙醇燃料电池(电解质溶液为KOH溶液)的结构示意图,则a处通入的是 (填“乙醇”或“氧气”),b处电极上发生的电极反应是: 。
(5)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其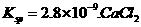 溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为
溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为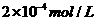 ,则生成沉淀所需CaCl2溶液的最小浓度为
。
,则生成沉淀所需CaCl2溶液的最小浓度为
。
7.现有甲、乙两种氧化物,所含R元素的质量分数分别为0.50和0.40。若已知甲是三原子分子,则乙的化学式是 ( )
A.RO2 B.RO3 C.R2O3 D.R2O5
6.已知25℃时,AgI饱和溶液中c(Ag+)为1.23×10-8mol/L,AgCl的饱和溶液中c(Ag+)为1.25×10-5mol/L。若在5mL含有KCI和KI各为0.01 mol/L的溶液中,加入8mL 0.01 mol/L AgNO3溶液,下列叙述正确是 ( )
A.混合溶液中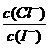 约为1.02×103
约为1.02×103
B.加入AgNO3溶液时首先生成AgCl沉淀
C.混合溶液中c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-)
D.混合溶液中c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com