
题目列表(包括答案和解析)
23.元素周期表是学习物质结构和性质的重要工具,元素周期律反映了元素性质的周期性变化规律。
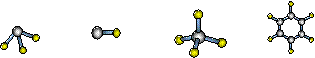 (1)元素A的原子最外层电子排布式为nsnnpn,该原子最外层共有 种不同运动状态的电子,该原子核外共有 种能量不同的电子。元素A与氢元素形成的分子,其空间结构可能是(填序号)
。
(1)元素A的原子最外层电子排布式为nsnnpn,该原子最外层共有 种不同运动状态的电子,该原子核外共有 种能量不同的电子。元素A与氢元素形成的分子,其空间结构可能是(填序号)
。
a b c d
(2)下列变化规律中正确的是 。
A.金属K、Na、Mg的熔沸点由低到高
B.C1-、Br-、I-的失电子能力由弱到强
C.H+、Li+、H-的半径由大到小
D.H3PO4、HClO4、H2SO4的酸性由弱到强
(3)第二周期元素中,除Be、B、Ne三种元素外,其他元素的氢化物沸点如下表所示,其中A的电子式为 ,E的化学式为 。
|
氢化物 |
A |
B |
HF |
D |
E |
|
沸点/℃ |
1317 |
100 |
19.5 |
 33 33 |
 164 164 |
22.含有1mol HNO3的稀硝酸分别与不同质量的铁粉反 应, 所得氧化产物a、b与铁粉物质的量关系如图所示(已知稀硝酸的还原产物只有NO)。下列有关判断正确的是
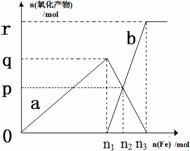 A.a是Fe(NO3)3
A.a是Fe(NO3)3
B.n1 = 0.375
C.p点时,n(Fe3+)=0.15mol
D.n2 = 0.50
第II卷(共84分)
21.pH与体积都相同的硫酸和醋酸溶液,分别与同物质的量浓度、同体积的Na2CO3溶液反应,若在相同条件下放出CO2的量相同,则下列推断合理的是
A.Na2CO3过量 B.Na2CO3恰好与醋酸完全反应
C.Na2CO3恰好与硫酸完全反应 D.两种酸都过量
20.亚硫酸(H2SO3)是二元弱酸,KHSO3溶液呈酸性。向10mL 0.01mol/L的H2SO3溶液滴加0.01mol/LKOH溶液VmL,下列判断错误的是
A.当V=10mL时,c(K+)>c(HSO3―) >c(H2SO3)>c(SO32―)
B.当V=20mL时,c(K+)>c(SO32―)>c(OH―)>c(HSO3―)>c(H+)
C.当V>0时,c(K+)+ c(H+)=2c(SO32―)+c(OH―)+c(HSO3―)
D.当V=20mL时,再滴入NaOH溶液,则溶液中n(K+) / n(SO32-)的值将变大
19.NA代表阿伏伽德罗常数,下列叙述正确的是
A.H2O2中加入MnO2,当产生0.1 mol O2时转移电子数为0.4 NA
B.常温常压下,0.1mol氖气含有的电子数为NA
C.标准状况下,11.2L氯仿中含有C-Cl键的数目为1.5NA
D.lmolC15H32分子中含碳碳共价键数目为14NA
18.下列反应的离子方程式正确的是
A.纯碱溶液中滴加少量盐酸:CO32- + H+ → HCO3-
B.乙炔气体中混有的硫化氢,可通过盛有CuSO4溶液的洗气瓶:
Cu2+ + S2-→ CuS↓
C.NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42-+Ba2++OH- → BaSO4↓+H2O
D.小苏打溶液中加入足量的石灰水: Ca2+ +2OH-+2HCO3-→CaCO3↓+CO32- +2H2O
17.标准状况下,将2.24LNH3通入1L 0.1mol/L的甲酸溶液中,欲确定所得溶液中NH4+、HCOO-、H+和OH-浓度大小顺序,通过下列数据即可得出正确结论的是
①NH3·H2O和HCOOH的电离常数 ②NH3·H2O和HCOONH4的电离常数
③溶液的pH
A.不需任何数据 B.必需知道①、②、③三组数据
C.只需知道①、③中的任一组数据 D.只需知道①、②、③中的任一组数据
16.右表是一些共价键的键能(kJ/mol)数据, 则以下表达肯定正确的是
|
共价键 |
键能 |
共价键 |
键能 |
|
H-H |
436 |
H-F |
565 |
|
C-F |
427 |
H-S |
339 |
|
C-Cl |
330 |
H-Se |
314 |
A.相同压强下,H2S的沸点比H2Se的沸点高
B.键长越短, 共价键越牢固
C.同条件下CH3Cl比CH3F更易发生水解反应
D.H2(g)→2H (g)+436kJ
15.类比(比较)是研究物质性质的常用方法之一,可预测许多物质的性质。但类比是相对的,不能违背客观实际。下列各说法中正确的是
A.根据化合价Fe3O4可表示为FeO·Fe2O3 ,则Fe3I8也可表示为FeI2·2FeI3
B.CaC2能水解:CaC2+2H2O → Ca(OH)2 + C2H2↑ ,
则Al4C3也能水解:Al4C3 + 12H2O → 4Al(OH)3↓+ 3CH4↑
C.O2与Cu反应加热生成CuO,则S与Cu反应加热生成CuS
D.SO2通入BaCl2溶液中不产生沉淀,则SO2通入Ba(NO3)2溶液中也不产生沉淀
14.化学是以实验为基础的自然科学,下列实验操作方法不正确的是
A.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
B.用稀氨水洗涤做“银镜反应”实验后附着在试管壁上的银
C.检查容量瓶是否漏水的方法是:向容量瓶中加水,塞好瓶塞,将容量瓶倒过来,若不漏水,将瓶塞旋转180°,再倒过来,看是否漏水
D. 用电石制备乙炔时,为防止产生气体的速率过快,可用饱和食盐水代替蒸馏水
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com