
题目列表(包括答案和解析)
5.下列有关叙述正确的是
A.研究质子和中子的结构是化学学科研究的一项新任务
B.在通风橱进行有毒气体的实验是一种符合“绿色化学”思想的防污染手段
C.根据能量守恒定律,燃烧一定量的煤和燃烧同量的煤干馏后的焦炭产生的能量一样多
D.随着化学的发展,化学实验方法并不是化学研究的唯一手段
4.有机物的种类繁多,下列有机物命名正确的是
A.CH3CH(OH)CH3 丙醇 B.CH2=CHCH2CH3 1-丁烯 yjw
C.CH3CCl2CH3 2-二氯丙烷 D.CH3CH(CH2CH3)CH3 2-乙基丙烷
3.最近科学家确认世界上还存在的另一种“分子足球”N60,它与C60的结构相似。下列说法正确的是
A.N60是一种新型化合物 B. N60和N2是同系物
C.N60和N2互为同素异形体 D. N60和14N都是氮的同位素
2.下列各项叙述中正确的是
A.H2O的电子式为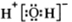
B.4℃时,纯水的pH=7yjw
 C.D216O中,质量数之和是质子数之和的两倍
C.D216O中,质量数之和是质子数之和的两倍
D.Cl-的结构示意图为
1.节能减排对发展经济、保护环境有重要意义。下列不能减少二氧化碳排放的措施是
A.推广使用煤液化技术 B.关停小火电企业
C.举行““地球一小时”熄灯活动 D.利用太阳能制氢yjw
31.在标准状况下进行下列实验:甲、乙、丙各取30.00mL同浓度的盐酸,加入同一镁、铝合金,产生气体,测得有关数据列表如下:
|
实验序号 |
甲 |
乙 |
丙 |
|
合金质量 |
0.255g |
0.385g |
0.459g |
|
气体体积 |
280mL |
336mL |
336mL |
(1)分析上表数据后填空:
①盐酸的物质的量浓度为 mol/L,在表中可作为计算依据的是(填实验序号,要求全部写出)
②据(填实验序号) 中的数据,可计算出合金中镁与铝的物质的量之比为
(2)在丙实验之后,向容器中加入一定量1.00mol/L的NaOH溶液,使合金中的铝恰好完全溶解,再滤出不溶固体请计算:
①滤液中溶质的物质的量
②加入NaOH溶液的体积
2010学年第一学期高三化学
30.(6分)一定量的氢气在氯气中燃烧,所得混合物用100mL 3.00mol/L的NaOH溶液(密度为1.12g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0600mol。
(1)原NaOH溶液的质量分数为
(2)所得溶液中Cl-的物质的量为 mol
(3)所用氯气和参加反应的氢气的物质的量之比n(Cl2):n(H2)= 。
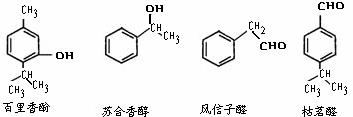
29. 以下几种物质是常用香精的主要成分(1)鉴别百里香酚和苏合香醇可采用的试剂为
;
(2)苏合香醇能发生的有机反应类型有
;(填序号)
A.加成反应
B.消去反应
C.加聚反应
D.缩聚反应
(3)写出符合下列条件的风信子醛的同分异构体的结构简式
;(任写一种)
a.含有苯环,苯环上有两个支链
b.与新制氢氧化铜悬浊液共热无砖红色沉淀
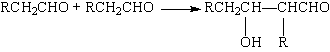 (4)已知醛在一定条件下可以两分子加成:
(4)已知醛在一定条件下可以两分子加成:
由枯茗醛合成兔耳草醛的路线如下:

①写出有机物A、B的结构简式 、 。 ②写出有机物C→兔耳草醛的化学方程式 。
28.有机物A的结构简式为:
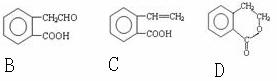
它可通过不同化学反应分别制得B、C和D三种物质。
(1)B中的含氧官能团名称是 、 。 (2)A→B的反应类型是 ;A-D中互为同分异构体的是 。 (3)由A生成C的化学方程式是 。 (4)C在一定条件下发生加聚反应的化学方程式是 。
27. 印刷电路的废腐蚀液含有大量CuCl2、FeCl2和FeCl3,任意排放将导致环境污染及资源的浪费。可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。测得某废腐蚀液中含CuCl2 1.5mol/L、FeCl2 3.0mol/L、FeCl3 1.0mol/L、HCl 3.0mol/L。取废腐蚀液200mL按如下流程在实验室进行实验:
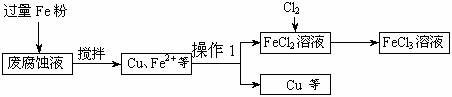
回答下列问题:
 (1)操作1的名称是
,上述方法获得的铜粉中含有杂质,除杂所需试剂是
(填化学式)。
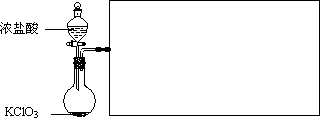
(2)实验室可用固体KClO3与浓HCl反应制备Cl2,此反应中Cl2既是氧化产物,又是还原产物。反应的化学方程式为
。
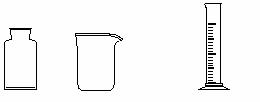
(3)右图是实验室制备Cl2并通入FeCl2溶液中获得FeCl3溶液的部分装置。
从下图挑选所需的仪器,完成上述装置简图(添加必要的塞子、玻璃导管、胶皮管。固定装置不用画),并标明容器中所装试剂。
(4)实验中,必需控制氯气的速度,使导管口逸出的气泡每秒1~2个,以便被FeCl2溶液完全吸收。控制生成氯气速度的操作是:
。
(5)按上述流程操作,需称取Fe粉的质量应不少于
g(精确到0.1g),需通入Cl2的物质的量不少于
mol,加入烧瓶中的KClO3的质量应不少于 g(精确到0.1g)。
(1)操作1的名称是
,上述方法获得的铜粉中含有杂质,除杂所需试剂是
(填化学式)。
(2)实验室可用固体KClO3与浓HCl反应制备Cl2,此反应中Cl2既是氧化产物,又是还原产物。反应的化学方程式为
。
(3)右图是实验室制备Cl2并通入FeCl2溶液中获得FeCl3溶液的部分装置。
从下图挑选所需的仪器,完成上述装置简图(添加必要的塞子、玻璃导管、胶皮管。固定装置不用画),并标明容器中所装试剂。
(4)实验中,必需控制氯气的速度,使导管口逸出的气泡每秒1~2个,以便被FeCl2溶液完全吸收。控制生成氯气速度的操作是:
。
(5)按上述流程操作,需称取Fe粉的质量应不少于
g(精确到0.1g),需通入Cl2的物质的量不少于
mol,加入烧瓶中的KClO3的质量应不少于 g(精确到0.1g)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com