
题目列表(包括答案和解析)
2. 被誉为“太空金属”的钛,在室温下,不与水、稀硫酸、稀盐酸和稀硝酸作用,但易溶于氢氟酸,这是因为 ( )
A.氢氟酸的酸性比其它酸强 B.氢氟酸的氧化性比其它酸强
C.氢氟酸的还原性其它酸强 D.钛离子易与氟离子形成可溶性难电离物质
1.下列说法中,正确的是 ( )
A.铅笔芯的原材料为铅,儿童使用铅笔时如果用嘴吮咬能够引起铅中毒
B.化学反应的过程中除了有物质的变化外还伴随着能量的变化
C.胶体与溶液的分离可用滤纸过滤的方法
D.金属钠、镁等活泼金属着火时,可以使用泡沫灭火器来灭火
31.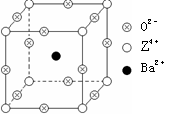 (15分)已知X、Y和Z三种元素的原子序数之和等于48。X的一种1:1型氢化物分子中既有σ键又有π键。Z是金属元素,Z的单质和化合物有广泛的用途。已知Z的核电荷数小于28,且次外层有2个未成对电子。工业上利用ZO2和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐)。M有显著的“压电性能”,应用于超声波的发生装置。经X射线分析,M晶体的最小重复单位为正方体(如右图),边长为4.03×10-10 m,顶点位置为Z4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占。
(15分)已知X、Y和Z三种元素的原子序数之和等于48。X的一种1:1型氢化物分子中既有σ键又有π键。Z是金属元素,Z的单质和化合物有广泛的用途。已知Z的核电荷数小于28,且次外层有2个未成对电子。工业上利用ZO2和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐)。M有显著的“压电性能”,应用于超声波的发生装置。经X射线分析,M晶体的最小重复单位为正方体(如右图),边长为4.03×10-10 m,顶点位置为Z4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占。
⑴Y在周期表中位于________________;Z4+的核外电子排布式为
______________;
⑵X的该种氢化物分子构型为 ,X在该氢化物中以 方式杂化。X和Y形成的化合物的熔点应该 (填“高于”或“低于”)X氢化物的熔点。
⑶①制备M的化学反应方程式是________________________________________;
②在M晶体中,若将Z4+置于立方体的体心,Ba2+置于立方体的顶点,则O2-处于立方体的_________;
③在M晶体中,Z4+的氧配位数为________;
④已知O2-半径为1.40×10-10 m,则Z4+半径为___________m。
[答案](15分)
⑴第四周期 第ⅡA族 1s22s22p63s23p6
⑵直线型 sp 高于
⑶①TiO2+BaCO3==BaTiO3+CO2↑ ②面心 ③6 ④6.15×10-11
[解析]由X的一种1:1型氢化物分子中既有σ键又有π键,可得氢化物中既有单键又有重键,X应是碳,氢化物是乙炔,分子中碳原子采用sp杂化。次外层有2个未成对电子的价电子排布式为3d24s2或3d104s2,又由于Z的核电荷数小于28,则只有3d24s2符合题意,是钛,根据X、Y和Z三种元素的原子序数之和等于48,可得Y的核电荷数等于20,位于第四周期IIA。
[考点]物质结构与性质
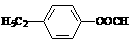
30.(15分)甲苯是有机化工生产的基本原料之一。利用乙醇和甲苯为原料,可按下列路线合成分子式均为C9H10O2的有机化工产品E和J。

已知: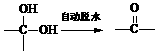
请回答:
⑴写出下列反应方程式
①B+D→E______________________________________________________。
②G→H ______________________________________________________。
⑵①的反应类型为____ ____;②的反应类型为____ ;F的结构简式为___________。
⑶E、J有多种同分异构体,写出符合下列条件的4种同分异构体结构简式。
要求:①与E、J属同类物质②苯环上有两个取代基且苯环上的一氯代物只有两种。
① ;② ;③ ;④ 。
[答案](15分)
⑴①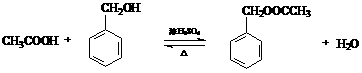
②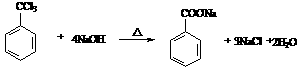
⑵取代 酯化(或取代) 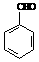
⑶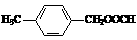 、
、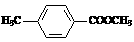 、
、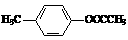 、
、
[解析]分析整个流程图:A是乙醇氧化产物乙醛,B是CH3COO-,B和D发生酯化反应生成E,由E的化学式可反推知D是苯甲醇,即C是甲苯侧链上的一氯取代产物。由题中信息:2个羟基连在同一碳原子上会失水形成羰基,故F是苯甲醛,其氧化产物I是苯甲酸,由苯甲酸反推得G是甲苯侧链上的三氯取代产物,水解产物H是苯甲酸钠。
[考点]有机化学基础
29.(8分)红矾钠(重铬酸钠:Na2Cr2O7·2H2O)是重要的基本化工原料,在印染工业、电镀工业和皮革工业中作辅助剂,在化学工业和制药工业中也可作氧化剂,应用领域十分广泛。
实验室中红矾钠可用一种铬铁矿(主要成分:FeO·Cr2O3,还含有少量铝的氧化物)通过以下过程来制取。
|


 铬铁矿等原料
Na2CrO4溶液
铬铁矿等原料
Na2CrO4溶液

|



铬渣(含硫酸钠)
回答下列问题:
⑴步骤I中反应化学方程式为:4FeO·Cr2O3+8Na2CO3+7O2→8Na2CrO4+2Fe2O3+8CO2在常温下该反应速率极慢,下列措施中能使反应速率增大的是 。(填字母)
A.将原料粉碎 B.增加纯碱的用量 C.升高温度
⑵步骤III需将溶液的pH调至7~8,并煮沸,其目的是 。
⑶步骤IV中发生反应的离子方程式为 。
⑷利用下面的复分解反应,将红矾钠与KCl固体按1:2物质的量之比混合溶于水后经适当操作可得到K2Cr2O7晶体:Na2Cr2O7+2KCl=K2Cr2O7+2NaCl (已知:温度对氯化钠的溶解度影响很小,对重铬酸钾的溶解度影响较大)。基本实验步骤为:①溶解;② ;③ ;④冷却、结晶,再过滤得K2Cr2O7晶体。其中③应在 (填“高温”或“低温”)条件下进行。
[答案](8分)
⑴A、C(2分) ⑵除去AlO2-杂质(1分)
⑶2CrO42-+2H+==Cr2O72-+H2O(2分)
⑷②蒸发(1分) ③过滤(1分) 高温(1分)
[解析]⑴将原料粉碎,即增大反应物的接触面积,可加快反应速率,由于纯碱是固体,固体用量的多少不影响化学反应速率,升高温度可加快反应速率。⑵由于题中明确铬铁矿中含有少量铝的氧化物,故后续操作必须除去铝,要注意的是本题不能回答除铁,原因是步骤I中反应已生成Fe2O3。⑶利用步骤V的反应可反推步骤IV中生成物是Na2Cr2O7,由此可知酸化时发生了CrO42-离子的缩合反应。⑷由于④进行冷却结晶,故③必为趁热过滤。
[考点]化学实验--化学生产中流程图分析
选考题(选择30、31题其中一道作答,请在答题纸上标明所选题号)
28. (8分)电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示。
(8分)电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示。

⑴实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的__________。
a.BaSO4 b.CH3CH2OH c.Na2SO4 d.NaOH
⑵电解池阳极发生了两个电极反应,其中一个反应生成一种无色气体,则阳极的电极反应式分别是
Ⅰ._____________________________;Ⅱ.______________________________。
⑶电极反应Ⅰ和Ⅱ的生成物反应得到Fe(OH)3沉淀的离子方程式是___________________________。
⑷该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料做电极。为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环(见上图)。A物质的化学式是_________________;
[答案](10分)
⑴c (2分) ⑵Fe-2e-=Fe2+ 4OH-- 4 e-= 2H2O+O2↑ (各2分)
⑶4Fe2++10H2O + O2= 4Fe(OH)3↓+8H+ (2分)
⑷CO2 (2分)
[解析]⑴为了增强溶液的导电性,因此可选用易溶性强电解质溶液,排除a和b。考虑到题中要求电解时保持污水的pH在5.0~6.0之间,因此不能添加NaOH。⑵电解时铁作阳极,因此主要发生Fe-2e-=Fe2+,同时也发生副反应,即溶液中的OH-失电子被氧化生成O2。⑶根据得失电子守恒和电荷守恒即可得离子方程式。⑷由于原电池的负极产物有水生成,所以负极必有CO32-参加,同时根据碳守恒可知A必为CO2,负极反应式可表示为CH4+4CO32-8e-=5CO2+2H2O。
[考点]电化学基础--电解原理的综合应用
27.(9分)以下是25℃时几种难溶电解质的溶解度:
|
难溶电解质 |
Mg(OH)2 |
Cu(OH)2 |
Fe(OH)2 |
Fe(OH)3 |
|
溶解度/g |
9×10-4 |
1.7×10-6 |
1.5×10-4 |
3.0×10-9 |
在无机化合物的提纯中,常利用难溶电解质的溶解平衡原理除去某些离子。例如:
①为了除去氯化铵中的杂质Fe3+,先将混合物溶于水,加入一定量的试剂反应,过滤结晶。
②为了除去氯化镁晶体中的杂质Fe3+,先将混合物溶于水,加入足量的Mg(OH)2,充分反应,过滤结晶。
③为了除去硫酸铜晶体中的杂质Fe2+,先将混合物溶于水,加入一定量的H2O2,将Fe2+氧化成Fe3+,调节溶液的pH=4,过滤结晶。请回答下列问题:
⑴上述三个除杂方案都能够达到很好效果,Fe2+、Fe3+都被转化为 而除去。
⑵①中加入的试剂应该选择___________________________为宜。
⑶②中除去Fe3+所发生的总反应的离子方程式为_____________________________。
⑷下列与方案③相关的叙述中,正确的是__________________(填字母)。
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.调节溶液pH=4可选择的试剂是氢氧化铜或碱式碳酸铜
D.Cu2+可以大量存在于pH=4的溶液中
E.在pH>4的溶液中Fe3+一定不能大量存在
[答案](9分)⑴氢氧化铁(1分) ⑵氨水(1分)
⑶2Fe3++3Mg(OH)2 == 3 Mg2+ +2Fe(OH)3 (3分)
⑷A C D E(4分)
[解析]①中为了不引入杂质离子,应加入氨水使Fe3+沉淀,而不能用NaOH溶液。②中根据溶解度表可明确Mg(OH)2能较容易转化为Fe(OH)3,因此在MgCl2溶液中加入足量Mg(OH)2可除去Fe3+,然后将沉淀一并过滤。③中利用高价阳离子Fe3+极易水解的特点,据题意可知调节溶液的pH=4可使Fe3+沉淀完全,为了不引入杂质离子,因此可使用CuO、Cu(OH)2、CuCO3等调节溶液的pH。
[考点]电解质溶解--沉淀溶解平衡
26. (10分)A、B、C、D、E是短周期元素组成的中学常见的物质,它们的转化关系如图所示(部分产物和反应条件略去)
(10分)A、B、C、D、E是短周期元素组成的中学常见的物质,它们的转化关系如图所示(部分产物和反应条件略去)
⑴若C为当今需要减排的一种热点温室气体,B为一种弱酸,则A化学式为______________。
⑵若D为白色胶状难溶物,且与A摩尔质量相等,则反应③的离子方程式为 ____________。
⑶若A为CO,则D的化学式为____________;t ℃时,在2 L的密闭的容器中加入3 mol CO和0.75 mol水蒸气,达到平衡时,CO的转化率为20%,在相同温度下再加入3.75 mol 水蒸气,再次达到平衡时,CO的转化率为_________。
[答案](8分)
⑴ F2 (2分) ⑵3Al3++3AlO2-+6H2O=4Al(OH)3↓(2分) ⑶Na2CO3 (2分)60%(2分)
[解析]⑴若C为CO2,则符合转化关系“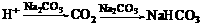 的A有三种:
的A有三种: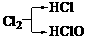 、
、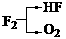 、
、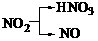 ,考虑到E为弱酸,则A应是F2。
,考虑到E为弱酸,则A应是F2。
⑵若D为白色胶状难溶物,设X为铝盐,D为Al(OH)3。先看转化关系:应有OH-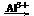 AlO2-
AlO2- 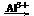 Al(OH)3。再看相对分子质量:Mr(D) = 78,与Na2O2的摩尔质量相同,且转化关系也吻合,故反应③的离子方程式为3Al3++3AlO2-+6H2O=4Al(OH)3↓。
Al(OH)3。再看相对分子质量:Mr(D) = 78,与Na2O2的摩尔质量相同,且转化关系也吻合,故反应③的离子方程式为3Al3++3AlO2-+6H2O=4Al(OH)3↓。
⑶若“A为CO”,则B为CO2、X为NaOH,C为NaHCO3,D为Na2CO3。
根据CO的转化率为20%可求得在t ℃时该反应的平衡常数等于1,设再次达平衡时消耗xmolCO
CO+H2O CO+H2
CO+H2
起始:3 4.5
变化:x x x x
平衡:3-x 4.5-x x x
则有:x2/[(3-x)(4.5-x)]=1,解得x=1.8mol,由此求得a (CO)=1.8/3×100%=60%。
[考点]元素及其化合物、化学反应速率与化学平衡
25.将质量相等的Ag片和铂片插入硝酸银溶液(足量)中,银片与电源正极相连,铂片与电源负极相连。以电流强度1A通电10min,然后反接电源,以电流强度2A继续通电10min。下列为表示银电极的质量、铂电极的质量、电解池中产生气体的质量和电解时间的关系图,正确的是 ( )
A.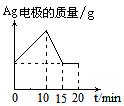 B.
B.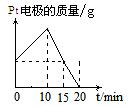
C.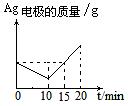 D.
D.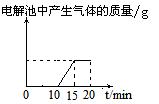
[答案]C
[解析]前10min,阳极(银片)上发生氧化反应:Ag-e-=Ag+,银电极质量减轻,阴极(铂片)发生还原反应:Ag++e-=Ag,铂电极质量增加。当电源反接后,由于电流强度是原来的2倍,故先考虑前5min的情况,此时附有Ag的铂片作阳极:电极反应式为Ag-e-=Ag+,通电5min后,前一过程析出的银全部溶解,阴极反应式为Ag++e-=Ag,前一过程溶解的银又复原,银电极又恢复为原来的质量。通电后5min,阳极(铂片)上溶液中的阴离子氢氧根离子放电生成O2,而阴极(银片)上继续析出银,且析出银的质量和溶解的银的质量相等。对照图像得只有选项C符合题意。
[考点]电化学基础--电解原理的应用
第Ⅱ卷(非选择题 共50分)
24. 有一反应:2A+B
有一反应:2A+B 2C,其中A、B、C均为气体,下图中的曲线是该反应在不同温度下的平衡曲线,x轴表示温度,y轴表示B的转化率,图中有a、b、c三点,如图所示,则下列描述正确的是 ( )
2C,其中A、B、C均为气体,下图中的曲线是该反应在不同温度下的平衡曲线,x轴表示温度,y轴表示B的转化率,图中有a、b、c三点,如图所示,则下列描述正确的是 ( )
A.该反应是放热反应
B.b点时混合气体的平均摩尔质量不再变化
C.T1温度下若由a点达到平衡,可以采取增大压强的方法
D.c点v (正)<v (逆)
[答案]B
[解析]由于温度升高,B的转化率增大,说明平衡正向移动,推知该反应是吸热反应,A错。在T1温度下,由a点达平衡时,B的转化率不断减小,若采取加压措施,结合化学方程式可知B的转化率会不断增大,故C错。在T2温度下,c点会达到平衡状态,此过程中B的转化率不断增大,说明该过程v (正)>v (逆),D错。
[考点]化学反应速率和化学平衡
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com