
题目列表(包括答案和解析)
7. 常温下pH为2的盐酸,下列叙述正确的是 ( )
A.将10mL该溶液稀释至100mL后,pH小于3
B.向该溶液中加入等体积pH为12的氨水恰好完全中和
C.该溶液中由水电离出的c(H+)(水)×c(OH-)(水)==1×10-14
D.该溶液中盐酸电离的c(H+)与水电离出的c(H+)之比为1010:1
6. 四种短周期元素X、Y、Z、W在元素周期表中的相对位置如下表所示,Y、Z质子数
之和为21,下列说法中不正确的是 ( )
|
|
X |
|
Y |
|
Z |
|
W |
|
A.X、Y、Z、W均为非金属元素
B.X、Y、W的氢化物中,Y的氢化物沸点最高
C.Z的阳离子与Y的阴离子电子层结构相同
D.W元素的简单离子半径大于Z元素的简单离子半径
5. 下列化学反应的离子方程式正确的是 ( )
A.石灰石溶于醋酸中:CaCO3+2H+=Ca2++CO2↑+H2O
B.向Ba(OH)2溶液中滴加NH4HSO4溶液至刚好沉淀完全:
Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3·H2O+H2O
C.将少量SO2气体通入足量的NaClO溶液中:SO2+2ClO-+H2O=SO32-+2HClO
D.稀硝酸中加入过量的铁屑:3Fe+8H++2NO3-=3Fe3++2NO↑+4H2O
4.下列化学原理表述正确的是
A.氢硫酸溶液加水稀释,电离程度增大,H+浓度增大;
B.Na2CO3溶液中满足:c(Na+)=2c( CO32-)+2 c( HCO3-)+ 2c (H2CO3)
C.NaHCO3溶液不显中性的原因:HCO3-+H2O CO32-+H3O+
CO32-+H3O+
D.同体积同pH的盐酸和醋酸,与足量的锌反应,盐酸的反应速率快,生成H2的物质的量多;
3. 下图所示对实验仪器名称的标注或实验操作正确的是 ( )
yjw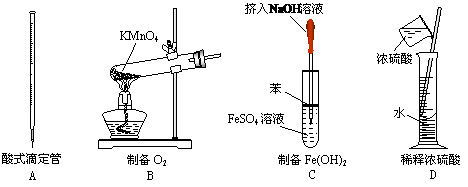
2. 实验室里不宜长期放置,应在使用时才配制的试剂是 ( )
①酚酞试液 ②银氨溶液 ③Na2CO3溶液 ④Cu(OH)2悬浊液
⑤酸性FeCl3溶液 ⑥FeSO4溶液 ⑦NaCl溶液 ⑧氯水
A. ②⑤⑥⑧ B. ①③④⑤ C. ①②⑤⑦ D. ②④⑥⑧
1. 2009年4月22日是第40个世界地球日,这年世界地球日的主题是“绿色世纪”。下列行为不符合这一主题的是 ( )
A. 分类回收、利用垃圾,减少资源浪费
B. 推广使用一次性木筷,减少疾病传染yjw
C. 开发风能等洁净能源,减少使用化石燃料
D. 研究煤和石油脱硫新技术,减少酸雨发生
25.(15分)胆矾(五水硫酸铜)是一种常见的化合物,工业上它也是一种制取其它含铜化含物的原料。现有废铜(主要杂质为Fe)来制备胆矾。有人设计了如下流程:
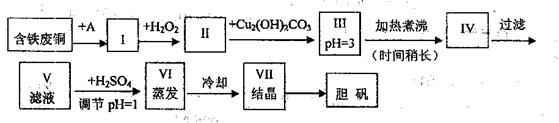
pH控制可参考下列数据
|
物质 |
开始沉淀时的pH |
完全沉淀对的pH |
|
氢氧化铁 |
2.7 |
3.7 |
|
氢氧化亚铁 |
7.6 |
9.6 |
|
氢氧化铜 |
5.2 |
6.4 |
请根据上述流程回答下列问题:
(1)A物质可选用 。(填字母)。
a.稀H2SO4 b.浓H2SO4/△ c.一浓FeC13溶液 d.浓HNO3
写出A物质溶解铜的化学方程式
(2)I中加H2O2的目的 。
(3)II中也可以加入下列物质中的 代替Cu2(OH)2CO3 (填字母)。
A.NH3 B.CuO C.NaOH D.Na2CO3 E.Cu(OH)2
(4)Ⅲ加热煮沸时发生的化学反应的离子方程式为 。
已知25℃时Fe(OH)3的溶度积为2.6×10-39,试计算25℃时,用溶液中Fe3+的浓度为
(5)IV过滤所需要的玻璃仪器除烧杯外还有 。
(6)V中加H2SO4调节pH=1是为了 。
(7)某工程师认为上述流程中所加的A物质并不理想,需作改进,其理由是 。

24.I(7分)将1 mof I2(g)1和2 molH2置于2L密闭容器中,在一定温度下发生反应:
I2(g)+ H2(g) 2H1(g);△H<0:,并达平衡。H1的体积分数w(HI)随时间变化如图晦线(II)所示:
2H1(g);△H<0:,并达平衡。H1的体积分数w(HI)随时间变化如图晦线(II)所示:
(1)达平衡时,I2(g)的物质的量浓度为____ 。
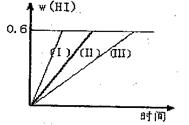 (2)若改变反应条件,在甲条件下w(HI)的变传如曲线(I)所示,在乙条件下w(HI)的变化如曲线(Ⅲ)所示。则甲条件可能是
,则乙条件可能是
。(填入下列条件的序号)
(2)若改变反应条件,在甲条件下w(HI)的变传如曲线(I)所示,在乙条件下w(HI)的变化如曲线(Ⅲ)所示。则甲条件可能是
,则乙条件可能是
。(填入下列条件的序号)
A.恒容条件下,升高温度;
B.恒容条件下,降低温度;
C.恒温条件下,缩小反应容器体积;
D.恒温祭件下,扩大反应容器体积:
E.恒温恒容条件下,加入适当催化剂。
(3)若保持温度不变,在另一个相同的2L密闭容器中加入a mo1 I2(g)、bmo1H2(g)和c mol HI(a、b、c均大于0),发生反应,达平衡时,HI的体积分数仍为0.6,则a、b、c的关系是 。
II.(8分)某二元酸(化学式用H2B表示)在水中的电离方程式是:
H2B H++HB- HB一 H++B2一
H++B2一
回答下列问题:
(1)Na2B溶液显_ ___(填“酸性”,“中性”,或“碱性”)。
理由是 (用离子方程式表示)。
(3)已知0.1.mol/L NaHB溶液的pH =2,则0.1 mol·L-1H2B溶液中氢离子的物质的量浓度可能是 0.ll mo1·L-l(填“<”,“>”或“=”),理由是: 。
(3)0.1 mol·L-1NaHB溶液中各种离子浓度由大到小的顺序是 。
23.(10分)
(1)肼(N2H4)义称联氨,是一种可燃性的液体,
可用作火箭燃料。已知在 101kPa时,32.0gN2H4
在氧气中完全燃烧生成氮气,放出热量624kJ
(25℃时),N2H4完全燃烧反应的热化学方程式是 。
(2)肼一空气燃料电池是一种碱性燃料电池,电解质溶液是20%-30%的KOH溶液。
肼一空气燃料电池放电时:
正极的电极反应式是 。
负极的电极反应式是 。
(3)右图是一个电化学过程示意图。
①锌片上发生的电极反应是 。
②假设使用肼一空气燃料电池作为本过程中的电源,铜片的质量变化128g,则肼一空气燃料电池理论上消耗标准状况下的空气 L(假设空气中氧气体积分数为20%)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com