
题目列表(包括答案和解析)
6.下列叙述正确的是
A.某元素由化合态变为游离态,该元素一定被还原
B.具有氧化性的物质在反应中一定做氧化剂
C.阳离子只能得到电子被还原,阴离子只能失去电子被氧化
D.置换反应一定是氧化还原反应
5.若ⅣA表示阿伏加德罗常数的值,下列说法正确的是 。
A.含有ⅣA个氖原子的氖气在标准状况下的体积约为ll.2L
B.2.39Na被O2完全氧化时,失去0.1 NA个电子
C.2Llmol·L-1的醋酸溶液中含有2NA个醋酸分子
D.标准状况下,5.6L苯含有O.25NA个分子
4.钢铁在潮湿的空气中会形成原电池而被腐蚀,下列说法正确的是
A.钢铁设备上连接铜块可以防止腐蚀
B.原电池的正极反应为:o2+2H20+4e一叫0H-
C.原电池的负极反应为:Fe---,Fe3++3e-
D.钢铁与外加直流电源的正极相连可以防止腐蚀 ’ .
3.短周期元素X、Y、Z在元素周期表中的位置如下图所示,下列说法正确的是
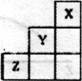
A.X、Y、z三种元素中,Y的非金属性最强
B.Y的气态氢化物的稳定性比Z的弱
C.Y的原子半径在同周期元素中最大
D.X单质的熔点比2单质的熔点高
2.下列分类正确的是
A.同位素:1H、D+、T2
B.电解质:H20、CH3COOH、NH4HC03
C.胶体:饱和氯化铁溶液、淀粉溶液、牛奶
D.硅酸盐产品:水晶、水泥、陶瓷
1.下列叙述正确的是
A.“雨后彩虹”是一种自然现象,;与胶体的知识有关
B.“农夫山泉”纯净水不含任何化学成分
C.“通风橱”是一种负责任的防污染手段,可使有害气体得到转化或吸收
D.长期盛放NaOH溶液的滴瓶不易打开,是因为NaOH与瓶中的C02反应使瓶内气体减少形成“负压”之故
16.将Fe和Cu的混合粉末ag加入到100mL 4mol/L稀硝酸中充分反应后(假设还原产物只有NO),下列说法正确的是(D)
A.若反应后有Cu剩余,则反应后溶液中含有的金属阳离子一定是Cu2+
B.若反应后的溶液中有Cu2+,则反应后溶液中含有的金属阳离子一定是Fe2+、Fe3+
C.若反应后的溶液中无金属剩余,则加入金属粉末质量8.4g<a<9.6g
D.若加入的Fe和Cu的质量比为7∶8,则使HNO3完全反应的金属粉末质量最小为7.2g
[解析](1)若反应后有Cu剩余,则此溶液中肯定没有Fe3+,一定有Fe2+,可能有Cu2+;(2)若反应后的溶液中有Cu2+,则此溶液中铁元素的存在形式是Fe3+或Fe2+或Fe3+和Fe2+;(3)由铁、铜分别与稀硝酸的反应可知,只发生铜与稀硝酸的反应时所需的金属质量最多,由3Cu-8HNO3可解得需Cu的质量为9.6g;而类似的可推知,只发生铁与稀硝酸的反应且铁完全变成Fe3+时所需的金属质量最少,由Fe-4HNO3可知需铁的质量为5.6g。(4)HNO3完全反应且金属质量最小,所以加入的铁要尽可能多耗酸,所以生成的是Fe3+,而Fe和Cu的质量比为7∶8,可得到两者的物质的量之比为1 ∶1,根据Fe-4HNO3,3Cu-8HNO3可解得需要Fe和Cu的物质的量均为0.06mol,从而可得金属粉末的质量为7.2g。
15.下列说法正确的是(D)
A.镁与极稀硝酸反应生成硝酸铵的离子方程式为:4Mg+6H++NO===4Mg2++NH+3H2O
B.25℃时,将20mL 0.1mol·L-1H2SO4溶液和30mL 0.15mol·L-1NaOH溶液混合,若混合后溶液体积不变,则混合溶液的pH为11
C.将10mL 0.1mol·L-1KAl(SO4)2溶液和10mL 0.2mol·L-1Ba(OH)2溶液混合,得到的沉淀中Al(OH)3和BaSO4的物质的量之比为1∶2
D.浓度均为0.1mol·L-1的醋酸和CH3COONa溶液等体积混合,溶液中有下列关系:c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-)
14.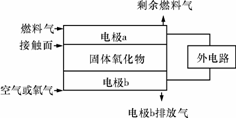 固体氧化物燃料电池(SOFC)以固体氧化物作为电解质。其工作原理如右图所示,下列关于固体燃料电池的有关说法正确的是(D)
固体氧化物燃料电池(SOFC)以固体氧化物作为电解质。其工作原理如右图所示,下列关于固体燃料电池的有关说法正确的是(D)
A.电极b为电池负极,电极反应式为O2+4e-===4O2-
B.固体氧化物的作用是让电子在电池内通过
C.若H2作为燃料气,则接触面上发生的反应为H2+2OH--4e-===2H++H2O
D.若C2H4作为燃料气,则接触面上发生的反应为C2H4+6O2--12e-===2CO2+2H2O
13.某溶液中只可能含有下列离子中的几种:K+、NH、NO、SO、SO、CO,取200mL该溶液分成两等份,进行以下实验:
(1)第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL。
(2)第二份先加足量的盐酸无现象,现加足量的BaCl2得到2.33g固体,则该溶液中(B)
A.可能含有K+、CO B.一定含有K+且c(K+)≥0.1mol/L
C.一定不含有NO D.肯定含有NO、SO、NH
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com