
题目列表(包括答案和解析)
4.下表为各物质中所含有的少量杂质,以及除去这些杂质应选用的试剂或操作方法。正确的一组为 ( )
|
序号 |
物质 |
杂质 |
除杂质应选用的试剂或操作方法 |
|
① |
KNO3溶液 |
KOH |
加入FeCl3溶液,并过滤 |
|
② |
FeSO4溶液 |
CuSO4 |
加入过量铁粉,并过滤 |
|
③ |
H2 |
CO2 |
通过盛有NaOH溶液的洗气瓶,再通过盛有浓硫酸的洗气瓶 |
|
④ |
NaNO3 |
CaCO3 |
溶解、过滤、蒸发 |
A.①②③④ B.③④ C.②③④ D.①②③
3.右图是元素周期表的一部分,下列说法中正确的是 ( )
|
B.气态氢化物的稳定性:④>②
C.最高价氧化物对应水化物酸性:⑤>④
D.元素的最高正化合价:③=⑤
2.下列实验仪器的选用合理的是 ( )
A.用蒸发皿加热NaCl溶液 B.用带橡胶塞的棕色瓶盛放溴水
C.用碱式滴定管量取20.00 mL KMnO4溶液
D.用瓷坩埚中熔化氢氧化钠固体
1.长征2号火箭承担运载“神六”的使命,氢化锂、氘化锂、氚化锂可以作为启动长征2号(CZ2F)火箭的优良炸药。下列说法正确的是 ( )
A.LiH、LiD、LiT的摩尔质量之比为1:2:3
B.它们都是强氧化剂
C.H、D、T之间互称为同素异形体
D.它们都是强还原剂
22.(10分)一定条件下,在体积为3L的密闭容器中化学反应
CO(g)+2H2(g)-"CH30H(g)达到平衡状态。


21.(8分)已知某溶液中只存在OH一、H+、NH:、Cl一四种离子,某同
学推测其离子浓度大小顺序可能有如下四种关系:


填写下列空白
(1)若溶液中只溶解一种溶质,则该溶质是--(填化学式),上述四种离子浓度的大小顺序为(填序号)--。 。
(2)若溶液中溶质为NI-kCl和NH3.H20,则溶液中四种离子浓度的大小顺序可能为
--(填序号)。
(3)将pH相同的NI-I+C1溶液和HCl溶液稀释相同的倍数,下列图像正确的是(填图像符号)--。

(4)若该溶液是由体积相等的稀盐酸和氨水湛合而成,且恰好呈中性,azJ删c(}硇C1)
--(NH3.H20)(填‘‘>”、“?或“=”)。
20.(15分)已知在pI-1为4-5的环境中,Cu2+几乎不水解,而Fe3+几乎完全水解。某学生欲用电解纯净的CuS04溶液的方法,根据电极上析出铜的质量以及电极上产生气体的体积来测定铜的相对原子质量。其实验过程如下图所示:
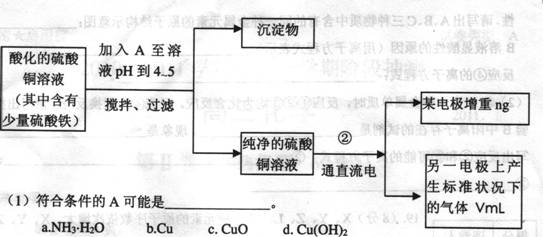
(2)过滤操作中用到的玻璃仪器有--;步骤②中所用的部分仪器如右图:则A连接直流电源的 极,B电极上发生的电极反应为--。
(3)电解开始一段时间后,在U形管中观察到的现象有
 电解的离子方程式为--。
电解的离子方程式为--。
(4)下列实验操作中必要的是(填字母)--。
A.称量电解前电极的质量
B.电解后,电极在烘干称重前,必须用蒸馏水冲洗‘
C.刮下电解后电极上析出的铜,并清洗、称重
D.电极在烘干称重的操作中必须按“烘干_+称重一再烘干_再称重,,进行
E.在有空气存在的情况下,烘干电极必须采用低温烘干的方法
(5)铜的相对原子质量为--(用带有Il、V的计算式表示)。
19.(8分)X、Y、Z、L、M五种元素的原子序数依次增大。x、Y、z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。请回答下列问题:
(1)M在元素周期表中的位置为--;五种元素的原子半径从大到小的顺序是--(用元素符号表示)。
(2)硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子
层,则Se的原子序数为--,其最高价氧化物对应的水化物化学式为--。该族2-5周期元素单质分别与H2反应生成l tool气态氢化物的焓变如下,表示生成1 mol硒化氢焓变的是--(填字母代号)。
a.+99.7 kJ·mol-1 b.+29.7 kJ·mol-1
c.--20.6 1 kJ·mol-1 d.一241.8 kJ·mol-1
(3)用M单质作阳极,石墨作阴极,NaHC03溶液作电解液进行电解,生成难溶物
R, R受热可分解。 写出生成R的反应式:--。
18.(12分)A、B、C三种物质中均含有同一种元素,它们之间有如下图所示的转化关系
(部分反应物质已略去)。
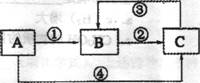
(1)若A是一种两性氧化物,B的水溶液呈酸性,请写出A、B、C三种物质中含有的同一种金属元素的原子结构示意图:--,
B溶液显酸性的原因(用离子方程式表示)--,反应④的离子方程式:--。
(2)若A为一种金属单质时,反应①②③均为化合反应,反应④为置换反应。请写出检验B中阳离子存在的试剂是--,现象是--,
写出反应②和⑨可能的离子方程式: ②--;
③ 。
16.将一定量的Fe、Fe203、Cu0的混合物放入体积为100mL、浓度为2.2m01.L-1的H2S04
溶液中,充分反应后,生成气体896mL(标况),得到不溶固体1.289,过滤后,滤
液中的金属离子只有FeZ+(滤液体积仍为l00mL)。向滤液中滴加2t001.L-1的NaOH
溶液至30mL时开始出现沉淀。则未滴加NaOH溶液前滤液中FeS04的物质的量浓
度为
A.2tool·L B.1.8mol·L C.1.9mol·L D.无法计算
保密★启甩前 试卷类型:A
2010--2011学年度第一学期阶段抽测
高三化学 2011.l
第Ⅱ卷(非选择题60分)
A.用新制备的Cu(OHh悬浊液与病人尿液共热,可检验人尿液中是否含有葡萄糖
B.用量筒量取5.0一ml.液体时俯视读数,会使液体体积小于5.0mL
C.用天平称量20.59某物质,砝码放在左盘,药品放在右盘
D.10%的硫酸和90%的硫酸等体积混合可配得50%的硫酸溶液
E.用灼烧闻气味的方法不能区别合成纤维和羊毛
F.紫外线、医用酒精能杀菌消毒,是因为使细菌的蛋白质性质改变
(2)将足量AgCl分别放入:①5ml水, ②10m10.2t001.1。!MgCl2溶液,③20m10.5
m01.10NaCl溶液,(4)40m10.1 m01.1’1盐酸中溶解至溶液饱和,各溶液中Ag+的浓度分别为a、b、c、d,它们由大到小的排列顺序是--。
(3)已知:

根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有
少量Fe203的Ti02)表面与水发生反应生成氨气,试写出此反应的热化学方程式:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com