
题目列表(包括答案和解析)
20.往100mL pH=0的硫酸和硝酸混合液中投入3.84g铜粉,微热使反应充分完成后,生成一氧化氮气体448mL(标准状况)。则反应前的混合溶液中含硝酸的物质的量为
A.0.02mol B.0.08ml C.0.10mol D.0.16mol
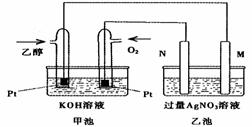
19.下图是一个乙醇燃料电池常温工作原理示意图,乙池中的两个电极一个
是石墨电极,一个是铁电极。工作时M、N两个电极的质量都不减少,则下列说法正确的是
 ( )
( )
A.M电极的材料是石墨
B.若乙池中某一电极质量增加4.32g时,理论上消耗氧气为448ml
C.在此过程中,甲池中OH-向通乙醇的一极移动
D.在此过程中,乙池溶液中电子从M电极向N电极移动
18.有关晶体的下列说法中正确的是( )
A.分子晶体中分子间作用力越大,分子越稳定
B.原子晶体中共价键越强,熔点越高
C.金属晶体发生形变时,金属键发生断裂
D.氯化钠熔化时离子键未被破坏
17.下面图像是从NaCl或CsCl晶体结构图中分割出来的部分结构图,试判断属于NaCl晶体结构的是 ( )
①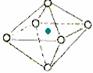 ②
② 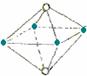 ③
③ 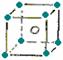 ④
④ 
A.①和④ B.②和③ C.①和③ D.②和④
16.现有A、B、C、D四种溶液,它们分别是AlCl3溶液、盐酸、氨水、Na2SO4溶液中的一种,已知A、B 溶液中水的电离程度相同,A、C溶液的PH相同,则下列说法正确的是: ( )
A.A为AlCl3溶液,C为盐酸
B.C中加入足量B反应的离子方程式为:Al3++3OH-=Al(OH)3↓
C.A、B等体积混合后,溶液中各离子浓度由大到小的顺序为:
c(NH4+)>c(Cl-)>c(OH-)>c(H+)
D.溶液中水的电离程度:A=B<C<D
15. 已知H2B在溶液中的电离方程式:H2B = H++HB-, HB-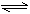 H++B2-。下列叙述一定正确的是
H++B2-。下列叙述一定正确的是
A. Na2B溶液存在:c (Na+) = 2c (HB-) + 2c(B2-) + 2c(H2B) ( )
B.NaHB溶液一定显酸性
C.HB-的水解方程式:HB-+H2O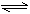 H2B+OH-
H2B+OH-
D.NaHB溶液与稀盐酸反应的离子方程式是:HB-+H+ = H2B
14.下列实验中,操作正确且能达到相应实验目的的是 ( )
A.做中和热测定实验时,若没有环形玻璃搅拌棒,可用环形铜质搅拌棒代替
B.中和滴定实验中,左手调控滴定管的活塞,右手持锥形瓶,眼睛注视滴定管中液面的变化
C. 溴蒸汽和二氧化氮两种红棕色气体可用淀粉碘化钾溶液来鉴别
D.除去蛋白质溶液中少量的NaCl,可将装有混合液的半透膜袋浸入流动的蒸馏水中
13.为提纯下列物质(括号内的物质是杂质),所选用的除杂试剂和分离方法都正确的是( )
|
|
被提纯的物质 |
除杂试剂 |
分离方法 |
|
A |
乙酸乙酯(乙酸) |
CCl4 |
萃取、分液 |
|
B |
乙烷(乙烯) |
高锰酸钾溶液 |
洗气 |
|
C |
乙醇(乙酸) |
新制氧化钙 |
蒸馏 |
|
D |
苯(溴) |
碘化钾溶液 |
分液 |
11.3种气态烃混合物VmL和足量氧气混合后,经点燃爆炸后并恢复到原状况下时,体积共缩小了2VmL。若所有气体体积均在25℃,1.01×105Pa下测定,则这3种烃的组合不可能是( )
A.CH4、C2H4、C3H4 B.C2H6、C3H6、C4H8
C.C2H2、C2H6、C3H8 D.CH4、C2H6、C2H2
12.下列说法中可能正确的是 ( )
A.标准状况下,pH=7的醋酸和醋酸钠的混合溶液中,c(CH3COO-)=c(Na+)
B.pH相同的NH4Cl溶液和硫酸溶液,稀释相同倍数后,硫酸溶液的pH小
C.Ba(NO3)2溶液可以鉴别SO2气体和CO2气体
D.向足量饱和石灰水中加入0.56 g CaO,可析出0.74 g Ca(OH)2固体
10.下列反应所产生的气体体积在标准状况下为22.4L的是 ( )
A.将2mol金属Cu与含2molH2SO4的浓硫酸共热
B.将1 mol MnO2固体与含4molHCl的浓盐酸共热
C.常温下,将32.2g金属钠和5.4g金属铝同时投入到足量水中
D.常温下,将10.8g的Al和22.4g的Fe投入到300g 98%的硫酸中
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com