
题目列表(包括答案和解析)
1.2010年上海世博会的目标是实现环保世博,生态世博。下列做法中不符合这一理念的是
( )
A.积极推行和使用能被微生物降解的新型聚合物材料
B.把生活垃圾焚烧或深埋处理
C.引进电动汽车,减少汽车尾气排放
D.停车场安装催化光解设施,用于处理汽车尾气
21.(10分)
有机物G广泛用作香精的调香剂,科技人员设计了如下路线合成该物质:
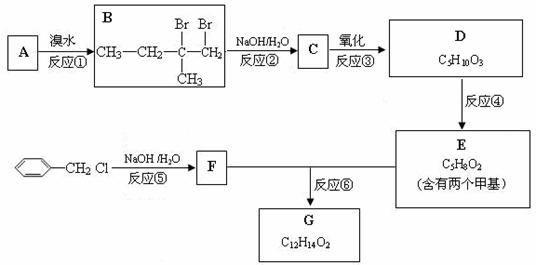
试回答下列问题:
(1)按系统命名法给B物质命名 。
(2)D物质的官能团名称 。
(3)上述合成路线中属于取代反应的是  (填编号)。
(填编号)。

(4)反应④的化学方程式为 。
(5)F有多种同分异构体,其中满足:(ⅰ)属于芳香族化合物;(ⅱ)不能使与FeCl3溶液显色的同分异构体的结构简式为 。
承德市联校2010-2011学年第一学期期末联考
20.(10分)
下图中,B、D、E、F、G是氧化物,F、K是氢化物,C、H是日常生活中常见的金属单质,J是黄绿色气态单质,M与氨水反应生成的O是白色沉淀。在B、H、L、M、N、O中含有同种元素,I是基础化学工业的重要产品(图中部分反应物和生成物没有列出)。
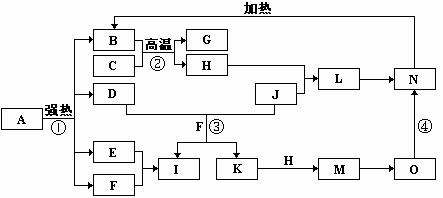
请按要求回答:
(1)H元素在周期表中的位置 。
(2)反应③的离子方程式 ;
反应④的化学方程式 。
(3)实验室用固体L配制溶液的方法是:
。
(4)由L的饱和溶液可以制得胶体,胶体中粒子直径的大小范围是 。若要提纯该胶体,采用的方法叫 。
19.(11分)
(1)某课外活动小组同学用图 1装置进行实验,试回答下列问题。
1装置进行实验,试回答下列问题。
①若开始时开关K与a连接,则铁发生电化学腐蚀中的 腐蚀;
②若开始时开关K与b连接,则总反应的离子方程式 。
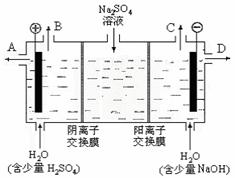
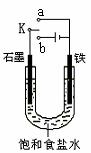
图1 图2
(2)芒硝化学式Na2SO4·10H2O,无色晶体,易溶于水,是一 种分布很广泛的硫酸盐矿物。该小组同学设想,如果模拟工业上离子交换膜法制烧碱的方法,用如图2所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠,无论从节省能源还是提高原料的利用率而言都更加符合绿色化学理念。
种分布很广泛的硫酸盐矿物。该小组同学设想,如果模拟工业上离子交换膜法制烧碱的方法,用如图2所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠,无论从节省能源还是提高原料的利用率而言都更加符合绿色化学理念。
①该电解槽的阳极反应式为 。此时通过阴离子交换膜的离子数 (填“大于”或“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钠溶液从出口(选填“A”、“B”、“C”、“D”) 导出。
③若将制得的氢气、氧气和氢氧化钠溶液组合为氢氧燃料电池,则电池负极的电极反应式为 。已知H2的燃烧热为285.8 kJ/mol,则该燃料电池工作产生36 g H2O时,理论上有 kJ的能量转化为电能。
18.(8分)
现用如下实验装置测定铜和氧化铜混合物中铜元素的含量。
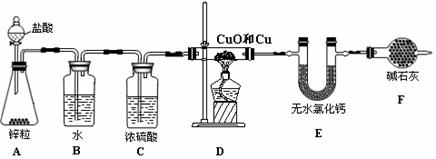
试回答下列问题:
(1)A中盛装盐酸的仪器名称为 。
(2)A中可观察到的现象为 。
(3)B装置的作用是 。
(4)在给D装置加热前,应该进行的一步操作是 ,其目的是:
。
(5)已知D装置中铜和氧化铜混合物的质量为10 g,经称量,反应前后E装置的质量分别为100.2 g和102.0 g,原混合物中铜元素的质量分数为 (假设各装置中的反应或吸收都是完全的)。
(6)如不加F装置,会使实验结果 (填“偏低”或“偏高”)。
17.(6分)
有甲、乙两个容积均为1 L的密闭容器,在控制两容器的温度相同且恒定的情况下进行反应:2A(g)+B(g) 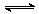 xC(g),①向甲中通入4
mol A、2 mol
xC(g),①向甲中通入4
mol A、2 mol  B,达平衡时测得其中C的体积分数为40%;②向乙中通入1 mol A、0.5
mol B和3 mol C,平衡时测得C的体积分数为W%。试回答:
B,达平衡时测得其中C的体积分数为40%;②向乙中通入1 mol A、0.5
mol B和3 mol C,平衡时测得C的体积分数为W%。试回答:
(1)若乙W%=40%,且建立平衡的过程中乙压强有变化 ,则x = 。
(2)若乙W%=40%,且平衡时甲、乙压强不同,则乙平衡时c(A) = 。
(3)若x =4,则W% 40% (填“大于”、“小于”或“等于”)。
16.(10分)
实验室制取氯气方法很多,通常有如下三种:
(1)用二氧化锰与浓盐酸共热制取氯气。如果将过量二氧化锰与20 mL 12 mol/L的浓盐酸混合加热,充分反应后生成的氯气明显少于0.06 mol。产生该结果的主要原因是:① ,② 。
(2)高锰酸钾与浓盐酸反应可制取氯气,其反应的化学方程式为:
。
 若消耗0.1 mol氧化剂,则被氧化的还原剂的物质的量为
mol。
若消耗0.1 mol氧化剂,则被氧化的还原剂的物质的量为
mol。
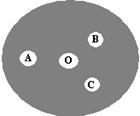
(3)现按如下操作进行有关氯气的制备及性质实验:在一片下衬白纸的圆形玻璃片上(如右图),A点滴一滴0.1 mol/L KI溶液(含淀粉溶液),B点滴一滴FeSO4(含KSCN)溶液,C点滴一滴NaOH(含酚酞)溶液,O点放少量KClO3晶体。向KClO3晶体滴加一滴浓盐酸,立即用表面皿盖好。试回答下列问题:
①A点反应的离子方程式为 ;
②B点的现象为 ;
③C点的溶液由红色变为无色,是因为中和褪色还是漂白而褪色,请你设计实验证明之。
。
15.在40 mL稀硫酸中加入1.6 g氧化铁后溶液仍呈酸性,再加入5 g 铁粉后,滴入硫氰化钾溶液,没有红色出现,此时溶液尚残留铁粉1.64 g,原硫酸溶液的物质的量浓度是 A.4 mol/L B.3.5 mol/L C.3 mol/L D.2 mol/L
承德市联校2010-2011学年第一学期期末联考
高 三 化 学 试 卷

 第Ⅱ卷 非选择题(共55分)
第Ⅱ卷 非选择题(共55分)
14.类推思维是化学解题中常用的一种思维方法,下列有关反应方程式的类推正确的是
|
|
已知 |
类推 |
|
A |
将Fe加入CuSO4溶液中 Fe+Cu2+=Cu+Fe2+ |
将Na加入到CuSO4溶液中 2Na+Cu2+=Cu+2Na+ |
|
B |
稀硫酸与Ba(OH)2溶液反应至中性 2H++SO 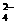 +Ba2++2OH-=BaSO4↓+2H2O +Ba2++2OH-=BaSO4↓+2H2O |
NaHSO4溶液与Ba(OH)2溶液反应至中性 2H++ SO 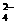 +Ba2++2OH-=BaSO4↓+2H2O +Ba2++2OH-=BaSO4↓+2H2O |
|
C |
铁和氯气反应 2Fe+3Cl2  2FeCl3 2FeCl3 |
铁和碘单质反应 2Fe +3I2  2FeI3 2FeI3 |
|
D |
向Ca(ClO)2溶液中通入少量CO2 Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO |
向Ca(ClO)2溶液中通入少量SO2 Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
13.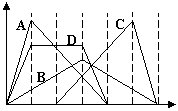 右图中横坐标为加入反应物的物质的量,纵坐标为产生沉
右图中横坐标为加入反应物的物质的量,纵坐标为产生沉
淀的物质的量。下列选项编号对应的曲线编号错误的是
A.向NaAlO2溶液中逐渐滴入HCl至过量
B.向澄清石灰水中通入CO2至过量
C.向含有盐酸的AlCl3溶液中滴入NaOH溶液至过量
D.向含有等物质的量的Ca(OH)2、KOH的混合溶液中通入CO2至过量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com