
题目列表(包括答案和解析)
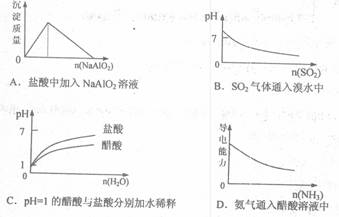
9.下列实验过程中产生的现象与对应的图形符合的是 ( )
8.已知常温常压下,饱和CO2的水溶液pH =3.9,可推断用标准盐酸溶液滴定NaHCO3水溶液时,适宜选用的指示剂及滴定终点时颜色变化的情况是 ( )
A.石蕊 由蓝变红 B.甲基橙 由黄变橙
C.酚酞 红色褪去 D.甲基橙 由黄变红
7.0.03molCu投入到一定量的浓HNO3中,Cu完全溶解,生成气体颜色越米越浅,共收集到标准状况下672mL气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的O2,恰好使气体完全溶于水,则通入O2的体积为 ( )
A.504mL, B.336mL C.224mL D.168mL
6.钢铁生锈过程发生如下反应:
①2Fe+O2+2H2O=2Fe(OH)2;②4Fe(OH)2+O2+2H2O=4Fe(OH)3;
③2Fe(OH)3=Fe2O3+3H2O。
下列说法正确的是 ( )
A.反应①、②中电子转移数日相等
B.反应①中氧化荆是氧气和水
C.与铜质水龙头连接处的钢质水管不易发生腐蚀
D.钢铁在潮湿的空气中不能发生电化学腐蚀
5.海洋中有丰富的食品、矿产,能源、药物和水产资源(如下图所示),下列有关说法不正确的是 ( )
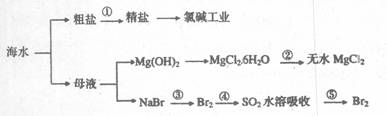
A.含有大量氮、磷的废水排入海洋,易引发赤潮
B.②中由MgCl2·6H2O制备无水MgCl2的过程为化学变化
C.在③④⑤中溴元素均被氧化
D.①中除去粗盐中的SO2-4、Ca2+、Mg2+等杂质,加入的药品顺序为:NaOH溶液→BaCl溶液→Na2CO3溶液→过滤后加盐酸
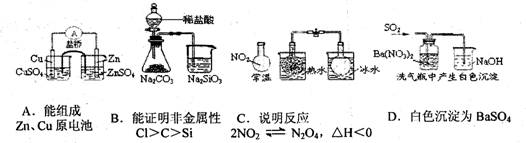
4.下列实验对应的结论不正确的是 ( )
3.已知NH3和HCl都能用来作喷泉实验的气体,若在同温同压下用等体积
烧瓶各收集满NH3和HCl气体,实验后二个烧瓶内溶液的关系是(两烧
瓶内充满溶液且不考虑溶质的扩散) ( )
A.溶质的物质的量浓度相同、溶质的质量分数不同
B.溶质的质量分数相同,溶质的物质的量浓度不同
C.溶质的物质的量浓度和溶质的质量分数都不同
D.溶质的物质的量浓度和溶质的质量分数都相同
2.下列推断合理的是 ( )
A.明矾[KAl(SO4)2·12H2O在水中能形成Al (OH)3胶体,可用作净水剂
B.金刚石是自然界中硬度最大的物质,不可能与氧气发生反应
C.浓H2SO4有强氧化性,不能与Cu发生剧烈反应
 D.将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水褪色后加热也能恢复原色
D.将SO2通入品红溶液,溶液褪色后加热恢复原色;将SO2通入溴水,溴水褪色后加热也能恢复原色
1.用NA表示阿伏加德罗常数的值。下列叙述正确的是 ( )
A.25℃时,pH=13的1.0L Ba (OH)2溶液中含有的OH-数日为0.2NA
B.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA
C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数日为1.5NA
D.标准状况下,22.4L甲醇中含有的氧原子数为1.0NA
21. B.(12分)铝镁合金是飞机制造、化工生产等行业的重要材料。研究性学习小组的同学,为测定某含镁30/0-5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究。填写下列空白。
[方案一]
[实验方案]将铝镁合金与足量NaOH溶液反应,测定剩余固体质量。
实验中发生反应的化学方程式是
[实验步骤]
(1)称取10. 8g铝镁合金粉末样品,溶于VmL4. 0mol·L-1'NaOH溶液中,充分反应。则NaOH溶液的体积V≥ 。
(2)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质量分数将
(填“偏高”、“偏低”或“无影响”)。
[方案二]
[实验方案]将铝镁合金与足量稀硫酸溶液反应,测定生成气体的体积。
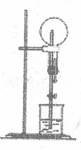
(1)同学们拟选用下列实验装置完成实验:
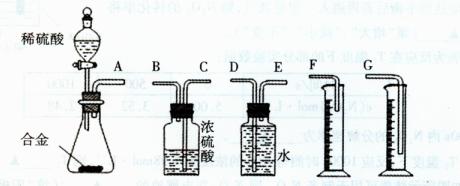
你认为最简易的装置其连接顺序是:A接( )( )接( )( )接( )(填接口字母,可不填满。)
(2)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:稀硫酸滴人锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小。于是他们设计了右图所示的实验装置。
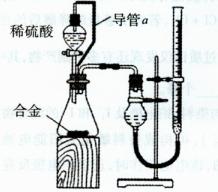
①装置中导管a的作用是 。
②实验前后碱式滴定管中液面读数分别为V1mL、V2mL。则产生氢气的体积为
mol。
③若需确定产生氢气的量,还需测定的数据是: , 。


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com