
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
22.(10Зж)вбжЊЗДгІЃК


(1)аДГіЗДгІЕФЦНКтГЃЪ§БэДяЪНK=ЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЃЛ
(2)гвЭМБэЪОЗДгІЙ§ГЬжагаЙиЮяжЪЕФФмСПЃЌдђЗДгІЕФ ЁЁЁЁЁЁЁЁЁЁ
0(ЬюЁА>ЁБЁЂЁА<ЁБЛђЁА=ЁБ)ЃЛ
ЁЁЁЁЁЁЁЁЁЁ
0(ЬюЁА>ЁБЁЂЁА<ЁБЛђЁА=ЁБ)ЃЛ
(Ђё)ЁЂ(Ђђ)СНЯпжаЃЌЪЙгУДпЛЏМСЕФЪЧЁЁЁЁЁЁЁЁ ЯпЃЛ
(3)ЗДгІжаЗЂЩњЗДгІЕФI-гыБЛбѕЛЏЕФI-ЕФЮяжЪЕФСПБШЮЊЁЁЁЁЁЁЁЁЁЁ ЃЛ
(4)ЗДгІЕФЫйТЪПЩвдгУ гыМгШыЕФЕэЗлШмвКЗДгІЯдРЖЩЋЕФЪБМфtРДЖШСПЃЌtдНаЁЃЌЗДгІЫйТЪдНДѓЁЃФГЬНОПадбЇЯАаЁзщдк20ЁцНјааЪЕбщЃЌМЧТМЕФЪ§ОнШчЯТЃК
гыМгШыЕФЕэЗлШмвКЗДгІЯдРЖЩЋЕФЪБМфtРДЖШСПЃЌtдНаЁЃЌЗДгІЫйТЪдНДѓЁЃФГЬНОПадбЇЯАаЁзщдк20ЁцНјааЪЕбщЃЌМЧТМЕФЪ§ОнШчЯТЃК
|
ЪЕбщБрКХ |
Ђй |
Ђк |
Ђл |
Ђм |
Ђн |
|
c(I-)/molЁЄL-1 |
0.040 |
0.080 |
0.080 |
0.160 |
0.160 |
c(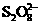 )/molЁЄL-1 )/molЁЄL-1 |
0.040 |
0.040 |
0.080 |
0.080 |
0.040 |
|
t/s |
88 |
44 |
22 |
11 |
t1 |
дђЃКИУЪЕбщЕФФПЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌ
ЯдЩЋЪБМфt1=ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ sЃЌ
ЗжЮіБэжаЪ§ОнЃЌЕУГіЕФНсТлЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
21.(10Зж)КЌгаШѕЫсHAКЭЦфФЦбЮNaAЕФЛьКЯШмвКЃЌдкЛЏбЇЩЯгУзїЛКГхШмвКЁЃЯђЦфжаМгШыЩйСПЫсЛђМюЪБЃЌШмвКЕФЫсМюадБфЛЏВЛДѓЁЃ
(1)ЯђИУШмвКжаМгШыЩйСПбЮЫсЪБЃЌЗЂЩњЗДгІЕФРызгЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌЯђЦфжаМгШыЩйСПKOHШмвКЪБЃЌЗЂЩњЗДгІЕФРызгЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
(2)ЯжНЋ0.04molЁЄL-1HAШмвККЭ0.02molЁЄL-1NaOHШмвКЕШЬхЛ§ЛьКЯЃЌЕУЕНЛКГхШмвКЁЃ
ЂйШєHAЮЊHCNЃЌИУШмвКЯдМюадЃЌдђШмвКжаc(Na+)ЁЁЁЁЁЁЁЁ c(CN-)(ЬюЁА<ЁБЁЂЁА=ЁБЛђЁА>ЁБ)ЃЌФуЕУГіИУНсТлЕФвРОнЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЛ
ЂкШєHAЮЊCH3COOHЃЌИУШмвКЯдЫсадЁЃШмвКжаЫљгаЕФРызгАДХЈЖШгЩДѓЕНаЁХХСаЕФЫГађЪЧ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
20. (8Зж)вбжЊFe(OH)2ЪЧАзЩЋФбШмгкЫЎЕФЮяжЪЃЌКмШнвзБЛПеЦјжаЕФбѕЦјбѕЛЏЮЊFe(OH)3ЁЃШчЭМЫљЪОзАжУПЩгУРДжЦШЁКЭЙлВьFe(OH)2дкПеЦјжаБЛбѕЛЏЪБбеЩЋЕФБфЛЏЁЃЪЕбщЪББиаыЪЙгУЬњаМКЭ6mol/LЕФСђЫсЃЌЦфЫќЪдМСздбЁЁЃ
(8Зж)вбжЊFe(OH)2ЪЧАзЩЋФбШмгкЫЎЕФЮяжЪЃЌКмШнвзБЛПеЦјжаЕФбѕЦјбѕЛЏЮЊFe(OH)3ЁЃШчЭМЫљЪОзАжУПЩгУРДжЦШЁКЭЙлВьFe(OH)2дкПеЦјжаБЛбѕЛЏЪБбеЩЋЕФБфЛЏЁЃЪЕбщЪББиаыЪЙгУЬњаМКЭ6mol/LЕФСђЫсЃЌЦфЫќЪдМСздбЁЁЃ
ЧыЬюаДЯТСаПеАзЃК
(1)BжаЪЂгавЛЖЈСПЕФNaOHШмвКЃЌAжагІдЄЯШМгШыЕФЪдМСЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЃЛ
(2)ЪЕбщПЊЪМЪБгІЯШНЋЛюШћEЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЁАДђПЊЁБЛђЁАЙиБеЁБ)ЃЌCжаЪеМЏЕНЕФЦјЬхЕФжївЊГЩЗнЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
(3)МђЪіЩњГЩFe(OH)2ЕФВйзїЙ§ГЬЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
(4)(3)ВйзїКѓАЮГізАжУBжаЕФЯ№ЦЄШћЃЌЪЙПеЦјНјШыЃЌаДГігаЙиЗДгІЕФЛЏбЇЗНГЬЪН
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
19.(6Зж)ФГЛЏбЇаЁзщЕФЭЌбЇЕНЪЕбщЪвбЇЯАЁЃдкЪЕбщзРЩЯАкгаЯТСавЧЦїЃК
 (1)жИЕМНЬЪІвЊЧѓЭЌбЇУЧаДГівЧЦїЕФУћГЦЃЌМзЭЌбЇЪщаДЕФД№АИШчЯТБэЃЌЧыФуевГіЦфжаЕФДэЮѓЃЌНЋИФе§КѓЕФУћГЦЬюаДдкЯТБэжа(Шєе§ШЗЃЌдђИУПеВЛашвЊЬюаД)ЁЃ
(1)жИЕМНЬЪІвЊЧѓЭЌбЇУЧаДГівЧЦїЕФУћГЦЃЌМзЭЌбЇЪщаДЕФД№АИШчЯТБэЃЌЧыФуевГіЦфжаЕФДэЮѓЃЌНЋИФе§КѓЕФУћГЦЬюаДдкЯТБэжа(Шєе§ШЗЃЌдђИУПеВЛашвЊЬюаД)ЁЃ
|
вЧЦїБрКХ |
a |
b |
c |
d |
e |
|
УћГЦ |
ЪдЙм |
ШмСПЦП |
МЏЦјЦП |
МюЪНЕЮЖЈЙм |
ЦеЭЈТЉЖЗ |
|
ИФе§ЕФУћГЦ |
ЁЁ |
ЁЁ |
ЁЁ |
ЁЁ |
ЁЁ |
(2)ЙигкeЕФгУЭОЃЌввЭЌбЇЫЕЃКзщГЩЗРЕЙЮќзАжУЁЃФуЛЙФмЫЕГіЦфЫћСНжжгУЭОТ№ЃП
ЂйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЂкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
 (3)БћЭЌбЇЯыгУгвЭМзАжУвдДѓРэЪЏКЭЯЁбЮЫсЗДгІжЦШЁCO2ЁЃНЬЪІжИГіЃЌеташвЊЬЋЖрЕФЯЁбЮЫсЃЌдьГЩРЫЗбЁЃИУЭЌбЇбЁгУСЫЩЯУцЕФвЛжжвЧЦїЃЌМгдкзАжУЩЯЃЌНтОіСЫетИіЮЪЬтЁЃЧыФуАбИУвЧЦїЛдкЭМжаКЯЪЪЕФЮЛжУЁЃ
(3)БћЭЌбЇЯыгУгвЭМзАжУвдДѓРэЪЏКЭЯЁбЮЫсЗДгІжЦШЁCO2ЁЃНЬЪІжИГіЃЌеташвЊЬЋЖрЕФЯЁбЮЫсЃЌдьГЩРЫЗбЁЃИУЭЌбЇбЁгУСЫЩЯУцЕФвЛжжвЧЦїЃЌМгдкзАжУЩЯЃЌНтОіСЫетИіЮЪЬтЁЃЧыФуАбИУвЧЦїЛдкЭМжаКЯЪЪЕФЮЛжУЁЃ
18. ЯТСаБэИёжаЕФИїжжЧщПіЃЌПЩвдгУЯТУцЕФЭМЯѓЧњЯпБэЪОЕФЪЧ
ЯТСаБэИёжаЕФИїжжЧщПіЃЌПЩвдгУЯТУцЕФЭМЯѓЧњЯпБэЪОЕФЪЧ
|
ЁЁ |
ЗДгІ |
знзјБъ |
Мз |
вв |
|
A |
ЯрЭЌжЪСПАБЃЌдкЭЌвЛШнЦїжа |
АБЦјЕФзЊЛЏТЪ |
500Ёц |
400Ёц |
|
B |
ЕШжЪСПМиЁЂФЦЗжБ№гызуСПЫЎЗДгІ |
H2жЪСП |
ФЦ |
Ми |
|
C |
дкЬхЛ§ПЩБфЕФКубЙШнЦїжаЃЌЬхЛ§БШ1ЁУ3ЕФN2ЁЂH2ЃЌ |
АБЦјЕФХЈЖШ |
ЛюадИпЕФДпЛЏМС |
ЛюадвЛАуЕФДпЛЏМС |
|
D |
2mol SO2гы1mol O2ЃЌдкЯрЭЌЮТЖШЯТ |
SO3ЮяжЪЕФСП |
10ИіДѓЦјбЙ |
2ИіДѓЦјбЙ |
 Ип Ш§ Фъ МЖ ПМ Ъд
Ип Ш§ Фъ МЖ ПМ Ъд
 ЛЏ бЇ Ъд Ьт
ЛЏ бЇ Ъд Ьт
ГЩМЈЭГМЦБэ(ПМЩњВЛвЊЬюаД)
ЕкЂђОэ(ЗЧбЁдёЬтЁЁ ЙВ54Зж)
ЕкЂђОэЙВ6ИіаЁЬтЁЃ
17.ЯТСаИїзщРызгдкжИЖЈШмвКжаЃЌвЛЖЈФмДѓСПЙВДцЕФЪЧ
ЁЁ A.ЮоЩЋШмвКжаЃК ЁЂ
ЁЂ ЁЂ
ЁЂ ЁЂ
ЁЂ
ЁЁ B.ФмгыТСЦЌЗДгІВњЩњЧтЦјЕФШмвКжаЃК ЁЂ
ЁЂ ЁЂ
ЁЂ ЁЂ
ЁЂ
ЁЁ C.ГЃЮТЯТЃЌ ЕФШмвКжаЃК
ЕФШмвКжаЃК ЁЂ
ЁЂ ЁЂ
ЁЂ ЁЂ
ЁЂ
ЁЁ D.КЌгаНЯЖр ЕФШмвКжаЃК
ЕФШмвКжаЃК ЁЂ
ЁЂ ЁЂ
ЁЂ ЁЂ
ЁЂ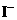
16. XЁЂYЁЂZЁЂWОљЮЊЖЬжмЦкдЊЫиЃЌЫќУЧдкжмЦкБэжаЯрЖдЮЛжУШчЭМЫљЪОЁЃШєYдзгЕФзюЭтВуЕчзгЪ§
XЁЂYЁЂZЁЂWОљЮЊЖЬжмЦкдЊЫиЃЌЫќУЧдкжмЦкБэжаЯрЖдЮЛжУШчЭМЫљЪОЁЃШєYдзгЕФзюЭтВуЕчзгЪ§
ЪЧФкВуЕчзгЪ§ЕФ3БЖЃЌЯТСаЫЕЗЈжае§ШЗЕФЪЧ
A.жЛгЩетЫФжждЊЫиВЛФмзщГЩгаЛњЛЏКЯЮя
B.зюИпМлбѕЛЏЮяЖдгІЫЎЛЏЮяЕФЫсадWБШZШѕ
C.ZЕФЕЅжЪгыЧтЦјЗДгІНЯYОчСв
D.XЁЂYаЮГЩЕФЛЏКЯЮяЖМвзШмгкЫЎ
15.вбжЊШШЛЏбЇЗНГЬЪНЃК ЁЃЯТСаЫЕЗЈе§ШЗ
ЁЃЯТСаЫЕЗЈе§ШЗ
ЁЁ ЕФЪЧ
ЁЁ A.ЯрЭЌЬѕМўЯТЃЌ2mol SO2(g)КЭ1mol O2(g)ЫљОпгаЕФФмСПаЁгк2mol SO3(g)ЫљОпгаЕФФм
ЁЁЁЁ СП
ЁЁ B.НЋ2mol SO2(g)КЭ1mol O2(g)жУгквЛУмБеШнЦїжаГфЗжЗДгІКѓЃЌЗХГіШШСПЮЊQkJ
ЁЁ C.діДѓбЙЧПЛђЩ§ИпЮТЖШЃЌИУЦНКтЖМЯђФцЗДгІЗНЯђвЦЖЏ
ЁЁ D.ШчНЋвЛЖЈСПSO2(g)КЭO2(g)жУгкФГУмБеШнЦїжаГфЗжЗДгІКѓЗХШШQkJЃЌдђДЫЙ§ГЬжага2mol
SO2(g)БЛбѕЛЏ
14. ЯТСаЦјЬхЂйNH3ЁЁ ЂкNO2ЁЁ ЂлNOЁЁ ЂмO2ЁЁ ЂнSO2жаЃЌЪЪгкгУЯТЭМзАжУжЦШЁКЭЪеМЏЕФЦјЬхЪЧ
ЯТСаЦјЬхЂйNH3ЁЁ ЂкNO2ЁЁ ЂлNOЁЁ ЂмO2ЁЁ ЂнSO2жаЃЌЪЪгкгУЯТЭМзАжУжЦШЁКЭЪеМЏЕФЦјЬхЪЧ
ЁЁ A.НіЂйЂкЁЁЁЁЁЁЁЁ B.НіЂкЂлЁЁЁЁЁЁЁЁЁЁЁЁ C.НіЂлЂмЁЁЁЁЁЁЁЁЁЁЁЁ D.НіЂкЂн
13.вЛЖЈЬѕМўЯТЃЌдкЬхЛ§ЮЊ10LЕФУмБеШнЦїжаЃЌ1mol XКЭ1mol YНјааЗДгІЃК2X(g)+ Y(g)
Z(g)ЃЌО60sДяЕНЦНКтЃЌЩњГЩ0.3mol ZЁЃЯТСаЫЕЗЈе§ШЗЕФЪЧ
ЁЁ A.вдXХЈЖШБфЛЏБэЪОЕФЗДгІЫйТЪЮЊ0.001molЁЄL-1ЁЄs-1
ЁЁ B.ЦфЫќЬѕМўВЛБфЃЌНЋШнЦїЬхЛ§БфЮЊ20LЃЌZЕФЦНКтХЈЖШБфЮЊдРДЕФ
ЁЁ C.ЦфЫќЬѕМўВЛБфЃЌШєдіДѓбЙЧПЃЌдђЮяжЪYЕФзЊЛЏТЪМѕаЁ
ЁЁ D.ЦфЫќЬѕМўВЛБфЃЌШєЩ§ИпЮТЖШЃЌXЕФЬхЛ§ЗжЪ§діДѓЃЌдђИУЗДгІЕФ
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com