
题目列表(包括答案和解析)
24.(8分)
(1)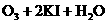 ===
===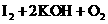 (2分)
(2分)
(2)淀粉 (1分) 溶液由蓝色变为无色(1分)
(3)由化学方程式得:
O3------------I2------------2Na2S2O3
1mol 2mol
n(O3) 0.0100mol/L×0.0600L
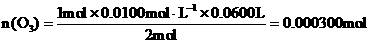 ………………(2分)
………………(2分)
则大气中臭氧的体积分数为: 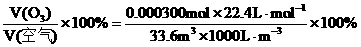
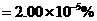 ……………………………………(2分)
……………………………………(2分)
23. (12分)
(12分)
(1) (2分) (2)N<Al<Na(2分)
(3)Al2O3+2OH-+3H2O=2[Al(OH)4]- (2分)
(4)酸(2分) 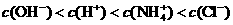 (2分)
(2分)
(5)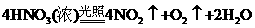 (2分)
(2分)
22.(10分)
(1)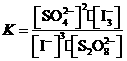 (2分) (2)<(1分),(Ⅱ)(1分) (3)3∶2(2分)
(2分) (2)<(1分),(Ⅱ)(1分) (3)3∶2(2分)
(4)研究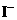 、
、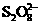 浓度对反应速率的影响(1分);22(1分);反应速率与反应物浓度乘
浓度对反应速率的影响(1分);22(1分);反应速率与反应物浓度乘
积成正比(2分)。
21.(10分)
(1)A-+H+=HA(2分);HA+OH-=H2O+A-(2分)
(2)①>(2分) 因为c(Na+)+c(H+)=c(CN-)+c(OH-),溶液显碱性,则c(H+)<c(OH-),所以c(Na+)>c(CN-)(2分)
②c(CH3COO-)>c(Na+)>c(H+)>c(OH-)或CH3COO-、Na+、H+、OH-(2分)
20.(8分)
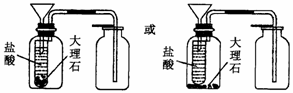
(1)铁屑(1分) (2)打开(1分) H2(1分)
(3)关闭活塞E,使FeSO4溶液被压入B瓶中进行反应(2分)
(4)4Fe(OH)2+O2+2H2O=4Fe(OH)3(3分)
19.(6分)(1)
|
仪器编号 |
|
b |
|
d |
|
|
名称 |
|
|
|
|
|
|
改正的名称 |
|
容量瓶 |
|
酸式滴定管 |
|
(每空1分,共2分。多写或写错一处扣1分,扣完为止)
(2)①往细口容器中加液体;②组成过滤装置(只要答对两个即可,其它合理答案亦可)(每种情况1分)
 (3)(2分)
(3)(2分)
(只需画对试管的位置即可得分)
3.化学方程式、离子方程式未配平的,都不给分。
第Ⅰ卷(选择题,共46分)
(每小题2分,共16分)
(每小题3分,共30分)
第Ⅱ卷(非选择题,共54分)
2.化学专用名词中出现错别字、元素符号有错误,都要参照评分标准扣分。
24.(8分)臭氧(O3)能与KI溶液反应,生成O2等。在反应后的溶液中滴入酚酞变为红色,若滴入淀粉则变为蓝色。为测定某环境空气中的臭氧含量,将0℃、1.01×105Pa的空气33.6m3通过KI溶液,使之完全反应,所得溶液用0.0100mol·L-1的Na2S2O3溶液60.0mL恰好滴定达终点。反应方程式为:2Na2S2O3+I2=Na2S4O6+2NaI。
(1)臭氧通入KI溶液中的化学方程式: ;
(2)滴定过程中选择的指示剂是 ,达到滴定终点时的现象为 ;
(3)计算该空气中臭氧的体积分数。
高 三 年 级 考 试
 化学试题(A)参考答案及评分标准
化学试题(A)参考答案及评分标准
说明:1.每小题若有其它正确答案,可参照评分标准给分。
23.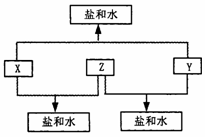 (12分)已知:A、B、C、D四种短周期元素,A与D的原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且存在如下转化关系,试推断回答下列问题。
(12分)已知:A、B、C、D四种短周期元素,A与D的原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且存在如下转化关系,试推断回答下列问题。
(1)D元素原子的结构示意图为 ;
(2)A、B、C三种元素的原子半径由小到大的顺序为
(用元素符号表示);
(3)Y与C元素的最高价氧化物可以发生反应,该反应的离子方程式为 ;
(4)A与D两元素的气态氢化物之间可以反应生成一种盐,该盐的水溶液呈 (填“酸”、“碱”或“中”)性,该水溶液中各离子浓度由小到大的顺序为 (用具体离子符号表示);
(5)实验室中,应将X的浓溶液保存在棕色试剂瓶中,其原因是
(用化学方程式表示)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com