
题目列表(包括答案和解析)
21.(8分)Z、W为含有相同电子数的分子或离子,均由原子序数小于10的元素组成,X有5个原子核。通常状况下,W为无色液体。 已知:X+Y Z+W
Z+W
(1)Y的电子式是_________________________。
(2)液态Z和W的电离相似,都可电离出电子数相同的两种离子,液态Z的电离方程式是_____________________。
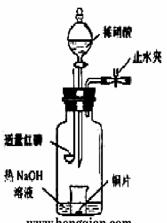
(3)用图示装置制备NO并验证其还原性。有下列主要操作:
a.向广口瓶内注入足量热NaOH溶液,将盛有铜片的小烧杯放入瓶中。
b.关闭止水夹,点燃红磷,伸入瓶中,塞好胶塞。
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中滴入少量稀硝酸。
①步骤c后还缺少的一步主要操作是_________________ ______________。
②红磷充分燃烧的产物与NaOH溶液反应的离子方程式是____________________。
③步骤c滴入稀硝酸后烧杯中的现象是_________________________ ____________ 反应的离子方程式是________________________________________。
20.今有两种正盐的稀溶液,分别是a mol/LNaX溶液和b mol/LNaY溶液,下列说法不正确的是
A.若a=b,pH(NaX) >pH(NaY),则相同浓度时,酸性HX<HY
B.若a=b,并测得c(X-)=c(Y-)+c(HY) ,则相同浓度时,酸性HX>HY
C.若a>b,测得c(X-)=c(Y-),则可推出溶液中c(HX)>c(HY),且相同浓度时,酸性HX<HY
 D.若两溶液等体积混合,测得c(X-)+c(Y-)+c(HX)+c(HY)=0.1mol/L,则可推出a=b=0.1 mol/L
D.若两溶液等体积混合,测得c(X-)+c(Y-)+c(HX)+c(HY)=0.1mol/L,则可推出a=b=0.1 mol/L
19.2.8gFe全部溶于一定浓度、100mL的HNO3溶液中,得到标准状况下的气体1.12L,测得反应后溶液的pH为1。若反应前后溶液体积变化忽略不计,则下列有关判断不正确的是
A.反应前HNO3溶液的浓度为2.0mol·L-1 B.1.12L的气体全部为NO
C.反应后溶液中c(NO3-)=1.6mol·L-1 D.反应后的溶液最多还能溶解1.61gFe
18.化合物A、B、C、D各由两种元素组成,甲、乙、丙是三种单质。这些常见的化合物与单质之间存在如下关系(已知化合物C是一种有机物),
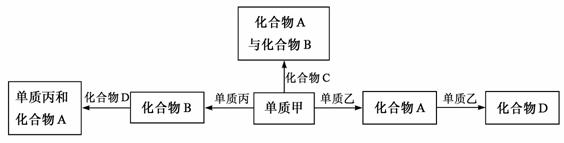
以下结论不正确的是
A.甲、乙、丙三种单质全是非金属
B.上述转化关系所涉及的化合物中有一种是电解质
C.上图所示的五个转化关系中,有三个是化合反应
D.上图所示的五个转化关系中,均为放热反应
17.下列物质中既能跟H2S反应,又能使溴水褪色的是 ①K2S溶液 ②SO2 ③CuSO4溶液 ④AgNO3溶液 ⑤氯化亚铁溶液 ⑥烧碱溶液
A.①②③ B.①②④⑥ C.③④⑤⑥ D.②④⑥
16.将KCl和CrCl3两种固体混合物共熔发生化合反应制得化合物X。将1.892gX中Cr元素全部氧化成Cr2O72-, Cr2O72-可与过量的KI发生氧化还原反应氧化出2.667g I2,反应的离子方程式是:Cr2O72-+6I-+14H+=2Cr3++3 I2+7H2O,如果取溶有1.892g X的溶液,加入过量的AgNO3,可得4.52gAgCl沉淀,则表示X组成的化学式为
A.K3Cr2Cl7 B.K3Cr2Cl5 C.K3Cr2Cl9 D.K2CrCl4
15、化学反应N2+3H2 = 2NH3的能量变化如题13图所示,该反应的热化学方程式是
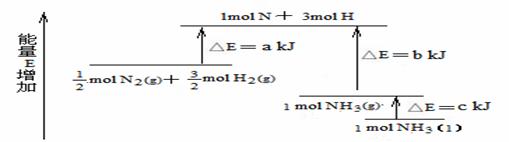
A、N2(g)+3H2(g) = 2NH3(l); ⊿H = 2(a-b-c)kJ/mol
B、N2(g)+3H2(g) = 2NH3(g) ; ⊿H = 2(b-a)kJ/mol
C、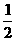 N2(g)+
N2(g)+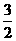 H2(g) = NH3(l) ; ⊿H = (b+c-a)kJ/mol
H2(g) = NH3(l) ; ⊿H = (b+c-a)kJ/mol
D、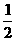 N2(g)+
N2(g)+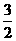 H2(g) =NH3(g) ; ⊿H = (a+b)kJ/mol
H2(g) =NH3(g) ; ⊿H = (a+b)kJ/mol
14.固体氧化物燃料电池(SOFC)以固体氧化物作为电解质。下列关于固体燃料电池的有关说法正确的是
A.通O2的电极为电池负极,电极反应式为O2+4e-=4O2-
B.固体氧化物的作用是让电子在电池内通过
C.若H2作为燃料气,则接触面上发生的反应为H2+2OH--4e-=2H++H2O
D.若C2H4作为燃料气,则接触面上发生的反应为C2H4+6O2--12e-=2CO2+2H2O
13.一定温度下可逆反应:A(s)+2B(g) 2C(g)+D(g);△H<0。现将1mol A和2molB加入甲容器中,将4
molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )
2C(g)+D(g);△H<0。现将1mol A和2molB加入甲容器中,将4
molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是( )
A.保持温度和活塞位置不变,在甲中再加入1molA和2molB,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍
B.保持活塞位置不变,升高温度,达到新的平衡后,甲中B的体积分数均增大,乙则减小
C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍
D.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略)

12.除去下列物质中少量杂质的方法正确的是 ( )
A.除去CO2中混有的HCl:用饱和碳酸钠溶液洗气
B.除去NO2中混有的NO:用水洗气
C.除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤
D.除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com