
题目列表(包括答案和解析)
29.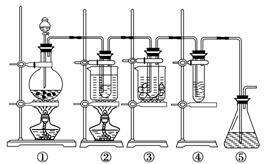 (A)实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
(A)实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过 (填写仪器名称)向烧瓶中加入适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有 (填写下列编号字母)的净化装置。
A.碱石灰 B.饱和食盐水 C.浓硫酸 D.饱和碳酸氢钠溶液
 (2) 比较制取氯酸钾和次氯酸钠的条件,二者的差异是:
(2) 比较制取氯酸钾和次氯酸钠的条件,二者的差异是:
反应完毕经冷却后,②的试管中有大量晶体析出。
右图中符合该晶体溶解度曲线的是
(填写编号字母);冷却后从②的试管中分离出该晶体的方法是 (填写实验操作名称)。
(3)本实验中制取次氯酸钠的离子方程式是 ,实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
|
实验现象 |
原因 |
|
溶液最初从紫色逐渐变为 色 |
氯气与水反应生成的H+使石蕊变色 |
|
随后溶液逐渐变为无色 |
|
|
然后溶液从无色逐渐变为 色 |
|
28.某化学实验兴趣小组为探究实验室制备Cl2 的过程中有水蒸气和HCl挥发来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略):
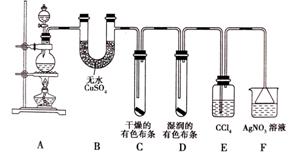
试回答下列问题:
(1) 下列方法中,可制得氯气的是________________。
① MnO2和浓盐酸混合共热 ② MnO2、NaCl和浓硫酸混合共热
③ 次氯酸钠和浓盐酸混合 ④ KClO3和浓盐酸混合共热
⑤ KMnO4和浓盐酸混合
(2) 若用含有0.2mol HCl 的浓盐酸与足量MnO2反应制取Cl2,制得的Cl2在标准状况下的体积总是小于1.12L的原因是___________________________________。
(3) ①装置B的作用是__________,现象是______________________________。
②装置C和D出现的不同现象说明的问题是___________________________________。
③装置E 的作用应该是___________________________________________。
④写出装置F中发生反应的离子方程式_______________________________。
(4)乙同学认为甲同学的实验有缺陷,不能确认最终通入AgNO3溶液中的气体只有一种,为了保证实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在______之间(填装置字母序号),装置中应加入_______________________。
27.海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
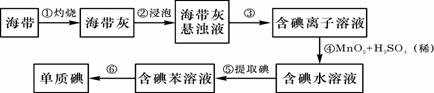
(1) 从上述步骤中可知,海带中含有的碘元素的主要存在形式是 。
(2) 步骤①灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是 。
(3) 步骤④中的转化还可以Cl2或双氧水,请分别写出反应的离子方程式:
、 。
(4) 步骤⑥是从含碘苯溶液中分离出单质碘和回收苯,还需经过蒸馏,指出
 下列实验装置中的错误之处。
下列实验装置中的错误之处。
①
②
进行上述蒸馏操作时,使用水浴的
原因是 、
______________________________,
最后晶态碘在 里聚集。
26.现有m g某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1。若阿伏加德罗常数用NA表示,则该气体的物质的量为 mol,该气体所含原子总数为 个,在标准状况下该气体的体积为 L。若该气体不与水反应,将其溶于1L水中,所得溶液中溶质的质量分数为 ,该气体溶于水后形成VL溶液,其溶液的物质的量浓度为 mol/L。
25.1811年法国化学家库特瓦用硫酸处理海藻灰时发现了碘。碘单质通常状况下为_______色固体,其制剂可用来消毒和治疗甲状腺肿。碘缺乏病是目前已知的导致人类智力障碍的主要原因,因此碘元素称作“智慧元素”。碘的单质有两种特性,一是物理特性:_____________________;二是化学特性:____________________________。
1824年法国化学家巴拉尔用氯气处理提取食盐后的盐水母液时发现了溴。溴元素的99%存在于海洋,称作“海洋元素”,其化合物可用作镇静剂。溴的原子序数为35,其原子结构简图为________________;溴化钠中存在的化学键是____________,在物理性质上表现出_______________________。氯化钠的电子式为_________,溴化钠的电离方程式为_________________ 。检验某固体试样中是否有Br-的方法为____________
_______________________________________________________。
24.(1)用滴管将新制的饱和氯水逐滴滴入含酚酞的氢氧化钠的稀溶液中,当滴到最后一滴时,红色突然褪去。产生该现象的原因可能有两个:
①是由于__________________________________________________;
②是由于__________________________________________________。
用实验证明红色褪去的原因是①或者是②,其方法是:______________________
_______________________________________。
(2)在一定条件下氯气可与氯化铵发生反应:xCl2+yNH4Cl→yNCln+(x+y)HCl
当消耗6.72 L标准状况下的氯气时,生成0.10 mol氮的氯化物,则此氮的氯化物的化学式为________。
23.某元素M的原子核内质子数与中子数相等,它形成气态氢化物在标准状况下的密度是1.518g/L,该氢化物0.5mol充分燃烧,生成9g水,则M的元素符号为 ,原子序数是 ,原子结构示意图为 ,M的阴离子电子层结构与____________等微粒相同。
22.20℃时有a g硫酸铜溶液V mL,将溶液蒸发掉b g水后恢复到20℃,恰好全部生成硫酸铜晶体(CuSO4·5H2O),则下列关系式错误的是( )
A.原硫酸铜溶液的密度为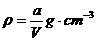
B.生成硫酸铜晶体的物质的量为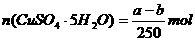
C.原硫酸铜溶液的物质的量浓度为
D.原硫酸铜溶液的质量分数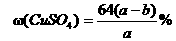
21.元素X与Y组成A、B两种化合物,A中X的质量占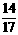 ,B中X的质量占
,B中X的质量占 ,则化合物A和B的分子式分别是 ( )
,则化合物A和B的分子式分别是 ( )
A.XY和XY2 B.X2Y和X2Y3 C.XY2和X2Y D.XY3和X2Y4
20.氯的原子序数为17,35Cl是氯的一种同位素,下列说法正确的是( )
A.35Cl原子所含质子数为18
B.1 mol的1H35Cl分子所含中子数约为19×6.02×1023
C.3.5 g的35Cl2气体的体积为2.24 L
D.35Cl2气体的摩尔质量为70 g·mol-1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com