
题目列表(包括答案和解析)
7.2010年诺贝尔化学奖授予美日科学家,他们由于研究“有机物合成过程中钯催化交叉偶联”而获奖。钯的化合物氯化钯可用来检测有毒气体CO,发生反应的化学方程式为:
CO+PdCl2
+H2O CO2
+Pd↓ +2HC1。下列说法正确的是 ( )
A.题述反应条件下还原性:CO> Pd
B.题述反应中PdCl2被氧化
C.生成22.4 L CO2时,转移的电子为2 mo1
D.CO气体只有在高温下才能表现还原性
6.化学在生产和日常生活中有着重要的应用。下列说法不正确的是 ( )
A.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
B.高温电解Al2O3可制得金属铝
C.MgO的熔点很高,可用于制作耐高温材料
D.根据冷的浓硫酸可以用铝质容器储存的事实,说明常温下铝不会与浓硫酸发生反应
5.某化学兴趣小组对某奖牌中金属的成分提出猜想:甲认为该金属是由纯金制成;乙认为该金属是由金银合金制成;丙认为该金属是由黄铜(铜锌合金)制成。为证明甲、乙、丙猜想的正误,可取少量制造该奖牌的材质粉末,加入一种试剂,该试剂应是( )
A.硫酸铜溶液 B.硝酸银溶液
C.盐酸 D.稀硝酸
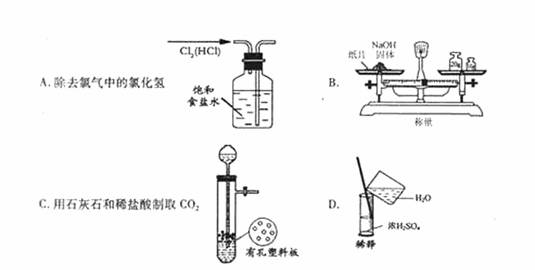
4.实验是研究化学的基础,下图中所示的实验方法、装置或操作完全正确的是 ( )
3.用你所学有机化学知识判断下列表述,其中正确的是 ( )
A.甲烷、乙烯、乙醇和乙酸都能发生加成反应
B.欲将蛋白质从溶液中析出而又不改变它的性质,可如入CuSO4溶液
C.乙烯气体既能使酸性高锰酸钾溶液褪色,也能使溴的四氯化碳溶液褪色
D.淀粉与蔗糖均不能被氧化
2. 2010年诺贝尔物理学奖用于表彰首次剥离出单层石墨的科学家。单层石墨称为石墨烯,这种“只有一层碳原子厚的碳薄片”的石墨烯,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,应用前景十分
2010年诺贝尔物理学奖用于表彰首次剥离出单层石墨的科学家。单层石墨称为石墨烯,这种“只有一层碳原子厚的碳薄片”的石墨烯,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,应用前景十分
广阔!下列关于石墨烯的叙述正确的是( )
A.石墨烯是碳单质
B.石墨烯是一种有机物
C.石墨烯中碳原子的化合价为+3
D.石墨烯可导电,说明它是电解质
1.分类是重要的科学研究方法,下列物质归类不正确的是 ( )
A.电解质:明矾、氯气、冰醋酸、硫酸钡
B.化合物:干冰、烧碱、冰水混合物、胆矾
C.混合物:铝热剂、矿泉水、水玻璃、漂白粉
D.同索异形体:C60、C70、金刚石
30.(B)生态溶液涉及农家肥料的综合利用,某种肥料经发酵得到一种含有甲烷、二氧化碳、氮气的混合气体。2.016L标准状况下的该气体通过盛有红色CuO粉末的硬质玻璃管,发生的反应为:CH4+4CuO CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管中物质的质量减轻4.8g。将反应后产生的气体通过过量的澄清石灰水,充分吸收,生成沉淀8.5g。
CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管中物质的质量减轻4.8g。将反应后产生的气体通过过量的澄清石灰水,充分吸收,生成沉淀8.5g。
(1) 试计算原混合气体中甲烷的物质的量。
(2) 原混合气体中氮气的体积分数为多少?
黄浦区2010学年度第一学期高三化学期终测试题
30.(A)使一定量的磷化氢和氢气的混合气体,依次通过两支加热的硬质玻璃管,第1支玻璃管中装有铜屑,第2支玻璃管中装有氧化铜,第1支玻璃管中由于发生如下反应:2PH3+Cu Cu3P2(s)+3H2,玻璃管中物质的质量增加4.96 g,第2支玻璃管中物质的质量减少了5.76 g。
Cu3P2(s)+3H2,玻璃管中物质的质量增加4.96 g,第2支玻璃管中物质的质量减少了5.76 g。
(1)计算原混合气体中磷化氢和氢气的体积比。
(2)在标准状况下,原混合气体的密度是多少?
29.(B)海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
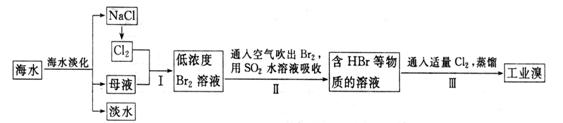
(1)请列举海水淡化的一种方法: 。
(2)将NaCl溶液电解,在电解槽中可直接得到的产品H2、 、 ,或H2、 。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为 _________。
(4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为 ,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是 。
(5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,了解到如下装置:

请你参与分析讨论:
① 图中仪器B的名称: 。
② 整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是__________________
。
③ 实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件:
。
④ C中液体产生颜色为 。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com