
题目列表(包括答案和解析)
17.(15分)V、W、X、Y、Z是原子序数依次递减的五种常见元素。X元素是地壳中含量最多的元素,Y、Z组成气态化合物M的水溶液呈碱性,W的单质在X2中燃烧的产物可使品红溶液褪色,V是一种历史悠久,应用广泛的金属元素。请回答:
(1)Y元素在周期表中的位置是 ;写出X、Z两种元素组成的化合物一种用途: 。
(2)由以上五种元素两两组合所形成的化合物中,有一种物质能与水反应生成气体且属于氧化还原反应,请写出该反应的化学方程式 。
(3)X、Y、Z三种元素可组成一种强酸U,M在适当条件下被U吸收生成一种盐。该盐的水溶液的pH 7(填“大于”、“小于”或“等于”)。
(4)若将V金属投入到盐酸溶液中,生成了浅绿色溶液N。N的酸性溶液与双氧水反应的离子方程式: 。
(5)有人设想寻求合适的催化剂和电极材料,以Y2、Z2为电极反应物,以HCl一4NHCl溶液为电解质溶液制造新型燃料电池,试写出该电池的正极反应式 ;放电时溶液中H+移向 (填“正”或“负”)极。
(6)W(a)+O2(g) WO2(g);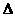 H1 W(g)+O2(g)
H1 W(g)+O2(g) WO2(g);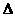 H2
H2
则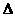 Hl
(填“>”或“(”或“=”)
Hl
(填“>”或“(”或“=”)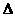 H2。
H2。
16.实验室常用硫酸铜溶液吸收气体中的硫化氢:
CuSO4+H2S CuS↓+H2SO4,该反应可以推测 ( )
A.CuS易水解
B.CuS可溶于盐酸
C.相同温度下氢硫酸饱和溶液中硫离子(S2-)浓度比CuS饱和溶液中大
D.强酸可以制取弱酸
第Ⅱ卷(非选择题52分)
15.从海水中提取镁的工艺流程如下图所示:
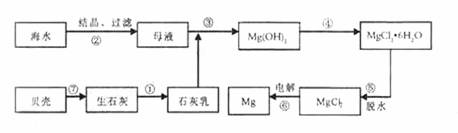
下列说法错误的是 ( )
A.用此法提取镁的优点之一是原料来源丰富
B.步骤⑥电解MgCl2时阴极产生氯气
C.步骤⑤可将晶体置于HCI气体氛围中脱水
D.上述工艺流程中涉及化合、分解和复分解反应
14.有关常温下pH均为3的醋酸溶液和盐酸的说法正确的是 ( )
A.两种溶液中,由水电离出的氢离子浓度均为l×10“1 mal.L-1
B.分别加水稀释100倍后,两种溶液的pH仍相等
C.中和同体积的这两种酸溶液所需要NaOH物质的量也相等
D.分别加入足量锌片,两种溶液生成H2的体积相等
13.能够使反应Cu+2H2O
Cu(OH)2+ H2↑发生的是 ( )
A.用铜片作阴、阳极,电解氯化铜溶液
B.用铜片作阴、阳极,电解硫酸钾溶液
C.铜锌合金在潮湿空气中发生电化学腐蚀
D.铜片和碳棒用导线相连后同时插入一烧杯内的氯化钠溶液中
12.下列离子组一定能大量共存的是 ( )
A.甲基橙呈红色的溶液中:I-、Cl一、NO3-、Na+
B.石蕊呈蓝色的溶液中:Na+、A1O2-、NO3-、HCO3-
C.含大量OH -的溶液中:CO32-、Cl-、F-、K+
D.含大量Al3+的溶液中:K+、Na+、NO3-、C1O-
11.下列化学实验相应的离子方程式正确的是 ( )
A.向Ba( OH)2溶液中滴加稀盐酸:2H++2C1- +Ba2+ +2OH-=2H2O+BaCl2
B.往FeCl3溶液中加入Fe粉:2Fe3+ +Fe 3Fe2+
C.往澄清石灰水中通入过量二氧化碳:Ca2+ +2OH -
+CO2 CaCO3↓+H2O
D.往FeCl3溶液中加入Cu粉:Fe3+
+Cu Fe2++Cu2+
10.NA表示阿佛加德罗常数。下列说法中正确的是 ( )
A.200mLlmol·L-lFe2(SO4),溶液中,Fe3+和SO42-离子数的总和是NA
B.O2和O3的混合物共4.8 g,其中所含氧分子数为0.3 NA
C.一定条件下,0.1mo1 Fe与0.2 molCl2充分反应,转移的电子数为0.3NA
D.标准状况下,22.4 L NO和11.2 L O2混合后气体的分子总数为1.5 NA
9.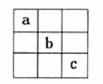 短周期的三种元素a、b、c在周期表中的位置关系如图所示,下列有关这三种元素的叙述中,正确的是 ( )
短周期的三种元素a、b、c在周期表中的位置关系如图所示,下列有关这三种元素的叙述中,正确的是 ( )
A.a是一种活泼金属元素
B.c的最高价氧化物的水化物是强酸
C.'b的氢氧化物是强碱
D.c的最高价氧化物的水化物是两性氢氧化物
8.某短周期元素X,其原子的电子层数为n,最外层电子效为2n +1。下列有关元素X的说法错误的是 ( )
A.元素X不可能是金属元素
B.元素X的气态氢化物易溶于水
C.元素x-定能形成化学式为KXO3的盐
D.工业上制取X的单质时一定采用氧化还原反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com