
题目列表(包括答案和解析)
23.已知I-、Fe2+、SO2、Cl-、H2O2在酸性溶液中的还原性强弱顺序为:
SO2 > I-> H2O2> Fe2+> Cl-,则下列反应不可能发生的是:
A、H2O2+ H2SO4= SO2+ O2+ 2H2O
B、2I- + 2Fe3+= I2 + 2Fe2+
C、2Fe2++SO42-+ 4H+=2Fe3+ + SO2 + 2H2O
D、SO2 +2H2O+ I2= H2SO4+2HI
22.下列反应的离子方程式书写正确的是
A.氯化铝溶液中加入过量氨水:Al3++3NH3·H2O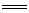 Al(OH)3↓+3NH4+
Al(OH)3↓+3NH4+
B.澄清石灰水与过量小苏打溶液混合:Ca2++OH-+HCO3-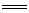 CaCO3↓+H2O
CaCO3↓+H2O
C.碳酸钙溶于醋酸:CaCO3+2H+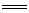 Ca2++CO2↑+H2O
Ca2++CO2↑+H2O
D.氯化亚铁溶液中通入氯气:2Fe2++Cl2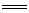 2Fe3++2Cl-
2Fe3++2Cl-
12.氮化铝(AIN)广泛用于电子工业、陶瓷工业等领域。可通过如下反应制取: Al2O3+N2+3C 2AlN+3CO
下列叙述正确的是
A.该反应中,Al2O3是氧化剂 B.该反应中,N2是还原剂
2AlN+3CO
下列叙述正确的是
A.该反应中,Al2O3是氧化剂 B.该反应中,N2是还原剂
C.该反应中,C是还原剂
D.该反应中每生成2molAlN,N2得到3mole-
10. 下列离子在溶液中能大量共存的是 A.NH4+、SO42-、NO3-、H+ B.I-、NO3-、H+、K+ C.NH4+、Cl-、OH-、NO3- D.Na+、Ca2+、SO32-、SO42- 11.下列各组离子在指定环境下能大量共存的是
A.pH=1的溶液中:Na+、S2-、K+、MnO4-
B.pH=7的溶液中:Al3+、Cl-、SO42-、HCO3-
C.pH>7的溶液中:Na+、AlO2-、SO42-、K+
D.pH=0的溶液中:Na+、K+、Fe2+、ClO-
9. 300 mL Al2(SO4)3溶液中,含Al3+为1.62 g,在该溶液中加入0.1 mol/L Ba(OH)2溶液300 mL,反应后溶液中SO的物质的量浓度为
A.0.4 mol/L B.0.3 mol/L
C.0.2 mol/L D.0.1 mol/L
8.设 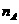 为阿伏加德罗常数的数值,下列说法正确的是
为阿伏加德罗常数的数值,下列说法正确的是
A.16g 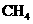 中含有4
中含有4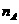 个C-H键
个C-H键
B.1mol·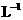
 溶液含有
溶液含有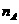 个
个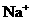
C..将0.1 mol 氯化铁溶于1 L水中,所得溶液含有0.1 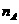 个Fe3+
个Fe3+
D.常温常压下,22.4L 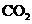 中含有
中含有 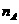 个
个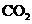 分子
分子
(化学部分可能用到的相对原子质量:C-12, O-16, H-1, Al-27, Na-23, Ba-137, Cl-35.5)
7.某合作学习小组讨论辨析以下说法:①粗盐和酸雨都是混合物;②沼气和水煤气都是可再生能源;③冰和干冰既是纯净物又是化合物;④不锈钢和目前流通的硬币都是合金;⑤盐酸和食醋既是化合物又是酸;⑥纯碱和熟石灰都是碱;⑦豆浆和雾都是胶体。上述说法正确的是
A. ①②③④ B.①②⑤⑥ C.③⑤⑥⑦ D.①③④⑦
4.
常温下,向含白色沉淀M的浊液中加入氯化钠固体,M的溶解度 将_____ (填“增大"、“减小"或“不变”),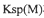 将_______________ (填“增大"、“减小"或“不变”)。
将_______________ (填“增大"、“减小"或“不变”)。
3. 在一定温度下,向容积不变(容积为10L)的密闭容器中加入2mol乙气体、8mol甲气体及固体催化剂。10分钟后反应达到平衡状态,容器内气体压强变为起始的80%,用乙气体表示的反应速率为:__________,反应达平衡犹态时甲气体的转化率为_______________,若想提高A的产率,根据化学平衡移动原理,请提出合理的建议:______________________________(任意写一条);
在上述平衡中,若再加入2 molA气体、2 mol乙气体,则此时化学平衡将_______________移动。(填“向正方向”、“向逆方向”或“不”)。
2.
各物质之间存在如下图所示的转化关系
 请回答下列问题:
请回答下列问题:
(1) C溶液显__________性(填“酸”、“碱”或“中”),若A溶液的物质的量浓度是B溶液的物质的量浓度的2倍,且等体积混合后溶液中各离子浓度由大到小的顺序为____________________ (用离子符号表示)。
(2)一定条件下,乙气体与甲气体充分反应生成6.8g A气体,可放出18.44 KJ热量,则该反应的热化学方程式为_______________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com