
题目列表(包括答案和解析)
13.Li~SO2电池具有输出功率高且低温性能好特点,其电解质为LiBr,溶剂是碳酸丙烯酯和 乙腈,Li+可在其中移动。电池总反应式为:2Li+2SO2 Li2S2O4下列有关电池的说法正确的是 ( )
Li2S2O4下列有关电池的说法正确的是 ( )
A.该电池总反应为可逆反应 B.充电时阴极反应式为:Li++e-===Li
C.放电时Li+向负极移动 D.该电池电解质溶液可换成LiBr水溶液
12.下列各组物质:①C+O2,②NH3·H2O+SO2,③Cu+HNO3,④Cl2+FeBr2,⑤Fe+HCl,⑥Zn+H2SO4,⑦NaHCO3+HCl,⑧Fe+Cl2,在不同条件下(浓度,温度,或用量)反应,能得到不同产物的是 ( )
A.①②③④⑥ B.①②③④⑤⑥⑦⑧
C.②④⑥⑧ D.①③⑤⑦
11.下表中评价合理的是 ( )

10.I2在KI溶液中存在下列平衡:
 I2(aq) +I- (aq)
I2(aq) +I- (aq) I-3(aq)
I-3(aq)
某I2、KI混合溶液中,I-3的物质的量浓度与温度T的
关系如右图所示(曲线上任何一点均表示平衡状态),
下列说法正确的是: ( )
A.状态A与状态B相比,状态A的c(I2)大于状态
B的c(I2)
B.若温度T1,T2的平衡常数分别为K1,K2,则K1> K2
C.反应:I2(aq)+I-(aq) I-3(aq);△H>0
I-3(aq);△H>0
D.反应进行到状态D时,一定有V正< V逆
9.短周期金属元素甲~戊在元素周期表中的相对位置如右表所示,下面判断正确的是( )
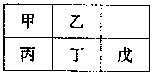 A.氢氧化物碱性:丙>丁>戊
A.氢氧化物碱性:丙>丁>戊
B.金属性:甲>丙
C.原子半径:丙<丁<戊
D.最外层电子数:甲>乙
8.在常温下发生下列反应:
(1)16H+ +10Z-+ 2XO-4 ===2X2++ 5Z2+ 8H2O
(2)2A2十+B2==2A3++ 2B-
(3)2B- +Z2==B2+2Z-
根据上述反应,判断下列结论中错误的是 ( )
A.溶液中可能发生:Z2+2A2+==2A3++2Z-
B.Z2在①、③反应中为还原剂
C.氧化性强弱顺序为:XO-4>Z2>B2>A3+
D.X2+是XO-4的还原产物
7.在中性含有Na+的溶液中,还可能存在NH4+,Fe2+,Br-,CO2-3,I一,SO2-3六种离子中的一种或几种,进行如下实验:
(1)原溶液滴加足量氯水后,有气泡生成,溶液呈橙黄色;
(2)向橙黄色溶液中加BaCI2溶液无沉淀生成
(3)橙黄色溶液不能使淀粉变蓝
由此推断原溶液中一定不存在的离子是: ( )
A.NH4+,Br-,CO2-3 B.NH+4,I-,SO2-3
C.Fe2+,I一,CO2-3 D.Fe2+,I-,SO2-3
6.下列叙述正确的是 ( )
A.Li在氧气中燃烧主要生成Li2O2
B.将SO2通入BaCl2溶液中可生成BaSO3沉淀
C.将CO2通人次氯酸钙溶液中可生成次氯酸
D.将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu
5.25℃时,弱酸的电离平衡常数如右表,下列说法正确的是 ( )
 A.等物质的量浓度溶液pH关系:
A.等物质的量浓度溶液pH关系:
pH(NaCN)> pH(Na2CO3)>
pH(CH3COONa)
B.amol/L HCN与bmol/L NaOH溶液等体积
混合后所得溶液中c(Na+)>c(CN-),则a一定小于b
C.往冰醋酸中逐滴加水,溶液导电能力先增大,后减小
D.NaHCO3和Na2CO3的混合液中:c(Na+)+c(H+)==c(OH-)+c(HCO-3)+c(CO2-3)
4.NA表示阿佛加德罗常数,下列说法正确的是 ( )
A.关于反应:C2H2(g)+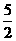 O2(g)==2CO2(g)+H2O(1);△H=-1300kJ/mol,若CO2中有4NA个共用电子对生成,则放出热量为1300kJ
O2(g)==2CO2(g)+H2O(1);△H=-1300kJ/mol,若CO2中有4NA个共用电子对生成,则放出热量为1300kJ
B.16g甲基正离子(13CH3+)所含中子数为9NA
C.200mL,0.lmol/L的Fe2(SO4)3溶液中阴离子和阳离子总数为0.1NA
D.0.1molFe与0.1molCl2充分反应转移电子数为0.2NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com