
题目列表(包括答案和解析)
3. 下列溶液中,不需避光保存的是
A.硝酸银溶液 B.浓硝酸 C.浓盐酸 D.氨水
2.下列各分子中,所有原子都满足最外层8 电子结构的是
A.CH4 B.BF3 C.CO2 D. PCl5
1.化学与生活、社会密切相关。下列说法不正确的是
A.燃煤中加人适量石灰石,可减少废气中SO2的量
B.高纯度的硅单质广泛用于制作光导纤维
C.为防止电池中的重金属污染土壤和水体,应积极开发废旧电池的综合利用技术
D.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
23. (10 分)
乙基香兰素的键线式结构如右图,它是当今世界上最重要的合成香料之一。 (1)以下推测正确的是_________ (填字母)。
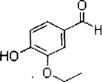
a.
从成键方式看,所含碳氧双键中有一个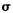 键和一个
键和一个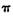 键
键
b. 该物质的一个分子内含有一个碳氧双键、三个碳碳双键
C 1 mol该物质最多能与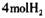 发生加成反应
发生加成反应
D 该物质能使酸性高锰酸钾溶液褪色,也能与碳酸钠溶液反应产生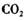 气体
(2)已知R物质是乙基香兰素的同分异构体,其性质如下:
气体
(2)已知R物质是乙基香兰素的同分异构体,其性质如下:
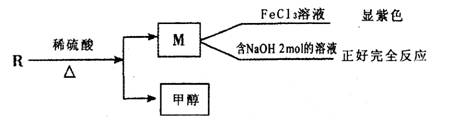
R符合上述条件,且lmol R与溴水发生取代反应时,消耗1mol溴,试写出符合要求的Fl的结构简式__________、___________、_________________;
(3)X也是乙基香兰素的同兮异构体,其结构简式为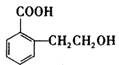 可以通过不同的反应制得下列物质。
可以通过不同的反应制得下列物质。
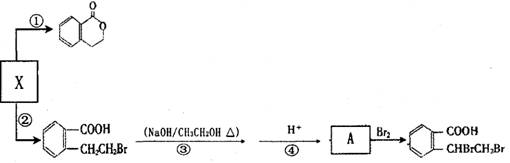
请回答下列问题:
A 反应③的反应类 型_______;
B 反应①的化学方程式____________
合肥市2011年高三第一次教学质量检测
21. (12分)
2006年世界锂离子电池总产量超过25亿只,锂电池消耗量巨大,对不可再生的金属资源的消耗是相当大的。因此锂离子电池回收具有重要意义,其中需要重点回收的是正极材料,其主要成分为钴酸锂(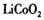 )、导电乙炔黑(一种炭黑)、铝箔以及有机粘接剂。某回收工艺流程如下:
)、导电乙炔黑(一种炭黑)、铝箔以及有机粘接剂。某回收工艺流程如下:
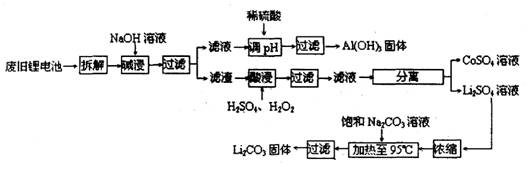
(1)上述工艺回收到的产物有______________________________________________
(2)废旧电池可能由于放电不完全而残留有原子态的锂,为了安全对拆解环境的要求是_________________________________________________
(3)碱浸时主要反应的离子方程式为_____________________________ 。
(4)酸浸时反应的化学方程式为___________________________________ 。最后一步过滤应__________
(5)如何洗涤过滤后的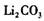 固体________________________________________________
固体________________________________________________
22(10 分)
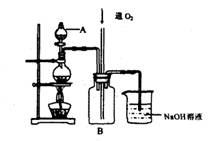
硫酸铜是一种用途广泛的化工原料。将适量稀硝酸分多次加人到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶,得到硫酸铜晶体(装置如图所示)。
(1)图中烧瓶内发生的离子反应方程式为:_____
(2)反应时B瓶内的现象是 _____________________
(3)为符合绿色化学的要求,某研究性学习小组进行如下设计:
第一组:以空气为氧化剂法
把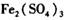 作催化剂加人到铜粉与稀硫酸的混合物中,并通人空气或氧气,即发生反应。反应完全后向其中加人物质甲调节
作催化剂加人到铜粉与稀硫酸的混合物中,并通人空气或氧气,即发生反应。反应完全后向其中加人物质甲调节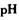 ,产生
,产生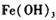 沉淀,过滤、蒸发、结晶,得到硫酸铜晶体,滤渣作催化剂循环使用。
经查阅资料得知,在溶液中通过调节溶液的酸碱性而使
沉淀,过滤、蒸发、结晶,得到硫酸铜晶体,滤渣作催化剂循环使用。
经查阅资料得知,在溶液中通过调节溶液的酸碱性而使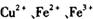 分别生成沉淀的pH如下:
分别生成沉淀的pH如下:
 请回答下列问题:
请回答下列问题:
①物质甲 是_____ (填字母序号)。
a. 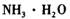 b.
b.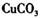 c.
c.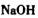 d.
d.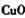
②该方案中调节PH的范围是_______ 。
第二组:过氧化氢氧化法
|
物质 |
开始沉淀时的PH |
完全沉淀时的PH |
|
Fe(OH)3 |
1.9 |
3. 2 |
|
Cu(OH)2 |
4. 7 |
6. 7 |
|
Fe(OH)2 |
6. 3 |
9. 7 |
将铜丝放到稀硫酸中,加入10%的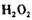 ,微热。充分反应后,经过滤、蒸发结晶、抽滤等操作,用少量95%的酒精淋洗后晾干,得到硫酸铜晶体。
请回答下列问题:
,微热。充分反应后,经过滤、蒸发结晶、抽滤等操作,用少量95%的酒精淋洗后晾干,得到硫酸铜晶体。
请回答下列问题:
③加热时温度不宜过高的原因是 _____,晶体采用酒精淋洗的优点是_____ 。
20. (12分)
二甲醚是一种重要的清洁燃料,可替代氟利昂作制冷剂,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。请回答下列问题:
(1)利用水煤气合成二甲醚的总反应为:
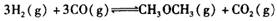
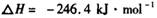
它可以分为两步,反应分别如下:
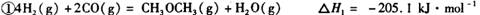
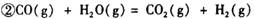
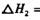 :__________________ ______________
:__________________ ______________
(2)在一定条件下的密闭容器中,该总反应达到平衡,只改变一个条件能同时提高反应速和CO的转化率的是_______(填字母代号)。
a.降低温度 b.加人催化剂 c.缩小容器体积
d.增加H2的浓度 e.增加CO的浓度
(3)在一体积可变的密闭容器中充入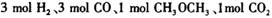 ,在一定温度和压强下发生反应:
,在一定温度和压强下发生反应: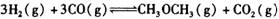 ,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。问:①反应开始时正、逆反应速率的大小:V(正)____V(逆)(填“ >”、“ < ”或"="),理由是:________________________________
,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。问:①反应开始时正、逆反应速率的大小:V(正)____V(逆)(填“ >”、“ < ”或"="),理由是:________________________________
②平衡时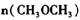 =__________________ ,平衡时CO的转化率= ______________ 。
=__________________ ,平衡时CO的转化率= ______________ 。
18. 多硫化钠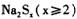 在
在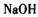 溶液中可被
溶液中可被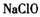 氧化成
氧化成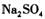 ,而
,而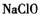 被还原成
被还原成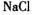 ,反应中
,反应中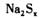 与
与 的物质的量之比为1:16。
的物质的量之比为1:16。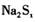 在结构上与
在结构上与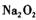 相似。则下列有关说法正确的是
相似。则下列有关说法正确的是
A.
该反应中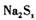 是氧化剂,
是氧化剂, 是还原剂
是还原剂
B.
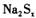 含有离子键和极性共价键
含有离子键和极性共价键
C.
 参加反应,有32mol电子转移
参加反应,有32mol电子转移
D.
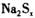 中的X数值为2
中的X数值为2
第II卷非选择题(56分)
|
19.
(12 分) 有关元素X、Y、Z、W的信息如下:
|
请回答下列问题:
(1) Y的单质在空气中充分燃烧所得氧化物的电子式_________________
(2) X、Y、W的简单离子的半径由大到小的是________________ (写离子符号)
(3) 向淀粉碘化钾溶液中滴加几滴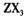 的浓溶液,现象为_______________ ,
的浓溶液,现象为_______________ ,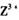 基态离子的电子排布式为
基态离子的电子排布式为
(4) 以 溶液为原料制取无水
溶液为原料制取无水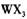 ,主要操作包括加热浓缩、冷却结晶、过滤,先制得
,主要操作包括加热浓缩、冷却结晶、过滤,先制得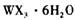 晶体,然后在 条件下加热
晶体,然后在 条件下加热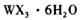 晶体,能进一步制取无水
晶体,能进一步制取无水 .其原因是(结合离子方程式简要说明) _____________________________________________
.其原因是(结合离子方程式简要说明) _____________________________________________
17. 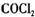 俗名¥作光气,是有毒气体。在一定条件下,可发生的化学反应为:
俗名¥作光气,是有毒气体。在一定条件下,可发生的化学反应为:
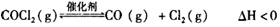 下列有关说法正确的是
下列有关说法正确的是
A. 在一定条件下,使用催化剂能加快反应速率并提高反应物的平转化率
B. 当反应达平衡时,恒温恒压条件下通人Ar,能提高COCl2的转化率
C.
单位时间内生成CO和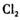 的物质的量比为1:1时,反应达到平衡状态
的物质的量比为1:1时,反应达到平衡状态
D. 平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
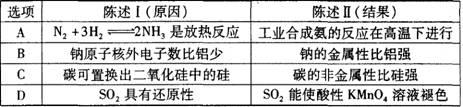
16. 下表列举的各组事实中存在因果关系的是
15. 下列关于电解质溶液的叙述正确的是
A.
常温下,在 的醋酸钠和醋酸混合溶液中:
的醋酸钠和醋酸混合溶液中: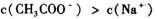
B. 稀释醋酸溶液,溶液中所有离子的浓度均降低
C.
在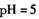 的氯化钠和稀硝酸的混合溶液中,
的氯化钠和稀硝酸的混合溶液中,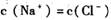
D.
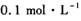 的硫化钠溶液中,•
的硫化钠溶液中,•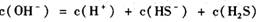
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com