
题目列表(包括答案和解析)
6.2010年4月,湖北又报道某水域爆发蓝藻。保护环境,保护水资源刻不容缓。蓝藻的形成是由于含N、P等元素的废水排入水域,引发蓝藻的疯狂生长。通过定量实验,分析得知某蓝藻的组成为(质量分数):C-35.80%,O-49.50%,P-0.87%,H-7.37%,N-6.31%。则该蓝藻的化学式为 ( )
A.C106H263O110N16P B.C106H263O111N15P
C.C106H262O111N17P D.C105H262O110N14P
5.蝇类昆虫的雌性信息素可用芥酸(来自白芥)与羧酸X在浓NaOH溶液中进行阳极氧化得到。电解总反应式为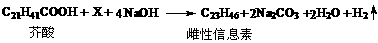
则下列说法正确的是 ( )
A.X为C2H5COOHww.k@s@5@ 高#考#资#源#网
B.电解的阳极反应式为: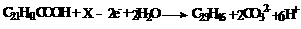
C.电解过程中,每转移2 mol电子,则生成2 mol 雌性信息素
D.阴极的还原产物为H2和OH-
[解析]此题为原创题。电解池电极反应判断,电极反应中关于物质的量的计算
4.醋酸和盐酸是高中化学中常见的两种酸,下列说法正确的是( )
A.物质的量浓度相同的盐酸和醋酸溶液中的H+浓度也相同
B.相同浓度的醋酸和醋酸钠溶液混合,得到溶液中c(CH3COO-)> c(Na+)> c(H+)> c(OH-)
C.pH=2的两溶液稀释100倍后,pH都为4
D.两溶液中都加入钾盐,H+浓度都减小
[解析]此题为原创题。主要考察物质水解离子浓度的比较
3.2011年3月9日,美国“发现”号航天飞机结束它的最后一次飞行使命,于佛罗里达肯尼迪航天中心着陆,未来的航天科技又将翻开新的篇章,胶状液氢(主要成分是H2和CH4)有望用于未来的运载火箭和空间运输系统。实验测得:101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ的热量;1 mol CH4完全燃烧生成液态水和CO2,放出890.3 kJ的热量。下列说法或热化学方程式书写正确的是( )
A.胶状液氢的标准燃烧热比甲烷要高
B.CH4(g)+2O2(g) ====CO2(g)+2H2O(l);ΔH=-890.3 kJ·mol-1
C.一般H2加压后以液态形式保存,且液氢燃烧效果比氢气要好,释放热量更多
D.2H2(g)+O2(g) ====2H2O(l);ΔH=-285.8 kJ
ww.k@s@5@ 高#考#资#源#网
[解析]此题为改编题。考察化学反应热方程的应用
2.化学是建立在实验基础上的学科。关于下列各实验装置的叙述中,不正确的是 ( )

A.装置①可用于实验室制取少量NH3或O2
B.可用从a处加水的方法检验装置②的气密性ww.k@s@5@ 高#考#资#源#网
C.实验室可用装置③收集H2、NH3
D.利用装置④制硫酸和氢氧化钠,其中b为阳离子交换膜、c为阴离子交换膜
[解析]此题为原创题。对新教材《实验化学》的强调,实验装置的熟悉度;电解池装置中离子交换膜的知识点
1.“砒霜”是我国古代一味重要的中药,其中含有一定量的砷元素,但同时它也具有剧毒。下列关于砷的说法不正确的是 ( )
A.水体的砷污染,会使水生生物体内砷含量超标,对人体造成危害
B.砷化氢的稳定性比溴化氢的弱,Mg3As2可以发生水解反应生成白色沉淀物质
C.砒霜可以用于癌症治疗,但服用过多可使人致命
D.砷、汞等都属重金属元素,对环境会造成污染。
[解析]此题为原创题。考察学生生活知识面是否丰富以及对元素周期律的应用
11. (改编自高三化学易错专题训练1)(14分)化合物A(C4H10O)是一种有机溶剂,A可以发生以下变化:

(1)1A分子中的官能团名称是__________________。
2A只有一种一氯代物B。写出由A转化为B的化学方程式__________________。
3A的同分异构体F也可以有框图内A的各种变化,且F的一氯取代物有三种。F的结构简式是_____________________。
(2)化合物“HQ”(C6H6O2)可用作显影剂,“HQ”可以与氯化铁溶液发生显色反应。“HQ”还能发生的反应是(选填序号)___________。
1加成反应 2氧化反应 3加聚反应 4水解反应
“HQ”的一硝基取代物只有一种。“HQ”的结构简式是_________________。
(3)A与“HQ”在一定条件下相互作用形成水与一种食品抗氧化剂“TBHQ”,“TBHQ”与氢氧化钠溶液作用得到化学式为C10H12O2Na2的化合物。“TBHQ”的结构简式为___________________。
ww.k@s@5@ 高#考#资#源#网
10、(原创)(15分)某化学实验小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置。按要求回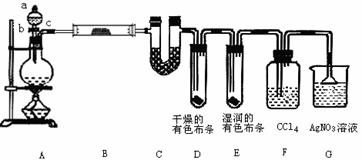 答问题。ww.k@s@5@
高#考#资#源#网
答问题。ww.k@s@5@
高#考#资#源#网
(1)如何检查装置A气密性?
写出装置A中反应的离子方程式____________________
(2)①装置B中盛放的试剂为 ,装置C中的盛放的试剂为
装置C的作用是
②装置D和E中出现的不同现象说明的问题是
③装置F的作用是 。
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在 与 之间(填装置字母序号),装置中应放入 (填写试剂或用品名称)
9.(改编自浙江省杭二中2011届高考理综化学部分7+4)(13分)A、B、C、D、E、F六种物质的相互转化关系如右图所示(反应条件未标出),其中反应①是置换反应。
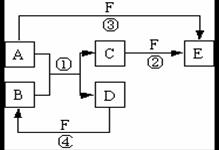
(1)若A是常见的金属单质,D、F是气态单质,反应①在水溶液中进行,反应后溶液呈浅绿色。则A在元素周期表中的位置是 ,反应②(在水溶液中进行)的离子方程式是 ;已知1 g D与F反应生成B时放出92.3 kJ热量,写出该反应的热化学方程式 。
(2)若A、D为短周期元素单质,且所含元素的原子序数A是D的2倍,所含元素的原子核外最外层电子数D是A的2倍,③和④两个反应中都有红棕色气体生成,反应①的化学方程式是 ,反应④的化学方程式是 。
(3)若A、D、F都是非金属单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式是 。晶体D的晶体类型为 ,A在生活中的常见用途 (写出一种)。
8.(改编自百度文库)(16分)A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。试回答:

(1)若A是乙醇,则C的结构简式是 ,反应①的化学方程式 ;2001年5月,中国宣布将推广“车用乙醇汽油”,所谓乙醇汽油就是在无铅汽油里加入适量乙醇混合而成的一种燃料。下列叙述中一定错误的是 。
A.乙醇汽油是一种新型的化合物
B.汽车使用乙醇汽油能减少有害气体的排放ww.k@s@5@ 高#考#资#源#网
C.工业常用裂化的方法提高汽油的产量
D.用玉米、高粱发酵可以制得乙醇
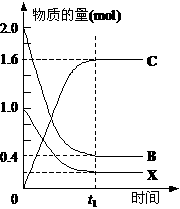
(2)若A是一种工业制硫酸的含金属元素矿物质主要成分,则A的化学式为 ,反应②的化学方程式 。某温度T时,在一定条件的2 L密闭容器中,反应②从起始到平衡后的关系如下左图所示。请据图回答下列问题:
①物质B的转化率 。
②求该温度下反应②的平衡常数 。
③在上述相同条件下,向相同的容器中投入2 mol C,t2时刻达到平衡。请在右下图中画出从反应开始至平衡后各物质物质的量与时间的关系图。ww.k@s@5@ 高#考#资#源#网

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com