
题目列表(包括答案和解析)
7. 下列各组离子在碱性条件下能大量共存,且在强酸性条件下能发生氧化还原反应的是
A. Ca2+、Al3+、SO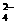 、Cl- B.
K+、Na+、SO
、Cl- B.
K+、Na+、SO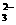 、NO
、NO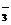
C. Na+、K+、NO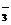 、SO
、SO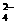 D.
NH
D.
NH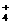 、Na+、Cl-、CO
、Na+、Cl-、CO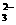
22.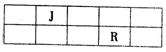 (7分)J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素。
(7分)J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素。
(1)元素T在周期表中位于第____族。
(2)M和T形成的化台物在潮湿的空气中形成酸雾,
反应的化学方程式为 。
(3)L的最简单气态氢化物甲的水溶液显碱性。在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为 。
21.(8分)X、Y、Z、W均为短周期元素组成的物质,它们之间有如图所示转化关系:
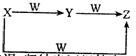
请从你所学的知述要求的X、Y、Z、W的组合。
|
|
X |
Y |
Z |
W |
备注 |
|
(1) |
|
|
|
|
W为单质 |
|
(2) |
|
|
|
|
W为酸 |
|
(3) |
|
|
|
|
W为碱 |
|
(4) |
|
|
|
|
W为氧化物 |
20.(9分)为减少和消除CO2对环境的影响,有科学家提出“绿色自由”的构想。既先把空气吹入碳酸钾溶液,然后再把CO2从溶液中提取出来,并使之变为可再生燃料甲醇。“绿色自由”构想技术流程如下:
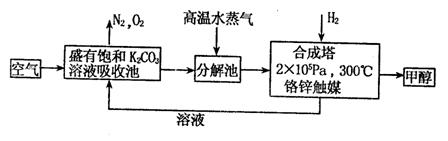
(1)写出分解池中反应方程式:
(2)在合成塔中,当有4.4kgCO2与足量H2完全反应,可放出热量4947kJ,写出合成塔中反应的热化学方程式:____
(3)写出以氢氧化钾为电解质的甲醇燃料电池的负极反应式:
19.(12分)海水中不仅含有丰富的非金属元素资源,(如CI,Br,I等),还含有丰富的金属元素资源(如Na,Mg,Fe,Cr等),
(1)海水晒盐的原理是: ;写出氯化钠的电子式: ;
与Na,Cl同周期,且简单离子半径最小的离子结构示意图:
(2)晒出的粗盐常混有MgSO4,CaSO4等杂质,为了得到精制盐,则提纯过程操作步骤和加入试剂的顺序是:①溶解,② ,③加过量Na2CO3溶液,④ 。
⑤过滤除去杂质,⑥ ,⑦蒸发结晶;
(3)晒盐得到的母液(盐卤)中含有丰富的镁元素,但其中常混有Fe2+,Cr3+等,为富集镁使其转化力MgCl2晶体。
有关资料:
|
M(OH)n |
pH |
|
|
开始沉淀 |
沉淀完全 |
|
|
Fe(OH)2 |
7.6 |
9.6 |
|
Fe(OH)3 |
2.7 |
3.7 |
|
Mg(OH)2 |
9.5 |
11.0 |
|
Cr(OH)3 |
4.3 |
5.0 |
为了有效除去杂质离子,又不引入新的杂质离子,且能满足“绿色化学理念”,则最佳试剂选择和操作是:
①先加 ;目的是 ;
②再加 ;目的是 ____,
③过滤后,为能得到纯净MgCl2晶体,采用的操作方法是: 。
18.(7分)随着环保意识的增强,清洁能源越来越受人们关注,
(1)甲烷是一种洁净能源,已知:
CH4(g)+ 2O2(g)===CO2(g)+ 2H2O(g);△H=-830kJ/mol
H2O(1)=H2O(g);△H=+44kJ/mol,则4.8g甲烷气体燃烧生成液态水放出热量为: ;
(2)利用甲烷与水反应制备氢气,因原料价廉产氢率高,具有实用推广价值,该反应:
CH4(g)+H20(g) CO(g)+3H2(g)△H=+206.1kJ/mol
CO(g)+3H2(g)△H=+206.1kJ/mol
①若800℃时,反应的平衡常数K1=1.0,某时刻测得该温度下,密闭容器中各物质的物质的量浓度分别为:c(CH4)=3.0mol/L;c(H2O)=8.5mol,/L;c(CO)= 2.0mol/L;c(H2):2.0mol/L,则此时正逆反应的速率关系是: (填序号)
A.V正>V逆 B.V正<V逆
C.V正=V逆 D.无法判断
②若将温度降至600℃时,此时平衡常数为K2,则K1 K2;(填“>”,“<”或“=”)
(3)利用MnFe2O4作催化剂,通过二步反应可将水分解制得H2,第一步反应为:
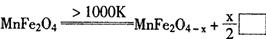
则框内的物质为: ;
第二步反应方程式为: 。
17.(9分)(1)化学实验设计和操作中必须十分重视安全问题和环境保护问题。下列实验阅题处理方法不正确的是 ( )
①配制稀硫酸时,可先在烧杯中加一定体积的水,再边搅拌边加入浓硫酸
②在气体发生装置上直接点燃一氧化碳气体时,必需要先检验一氧化碳气体的纯度。最 简单的方法是用排空气的方法先收集一试管气体,点燃气体,听爆呜声。
③实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室
④给试管中的液体加热时不时移动试管,以免暴沸伤人
⑤不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛
A.②③ B.②⑤ C.③④ D.①③
(2)下列实验操作完全正确的是 ( )
|
编号 |
实验 |
操作 |
|
A |
钠与水反应 |
用镊子从煤油中取出金属钠,切下绿豆大小的钠,小心放入装满水的烧杯中 |
|
B |
配制一定浓度的氯化钾溶液1000mL |
准确称取氯化钾固体,放入到1000mL的容量瓶中,加水溶液,振荡摇匀,定容 |
|
C |
排除碱式滴定管尖嘴部分的气泡 |
将胶管弯曲使玻璃尖嘴斜向上,用两指捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出 |
|
D |
取出分液漏斗中所需的上层液体 |
下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
①量筒的刻度由下向上增大,无零刻度 ②在250mL容量瓶上,除刻度外,还刻有250mL 和20℃③滴定管的刻度是由上向下增大,零刻度在上④温度计的刻度由下向上增大, 零刻度偏下⑤用托盘天平称量样品质量时,指针应在标尺的中央
A.②③正确 B.①②⑤正确 C.都正确 D.②③④⑤正确
16.向一定量的Fe,FeO,Fe2O3,Fe3O4的混合溶液中,加入150mL 4mol/L的稀硝酸,恰好使混合物完全溶解,并放出标准状况下NO气体2.24L,往所得溶液中加KSCN溶液,无红色出现。若用足量的氢气在加热条件下还原相同质量的该混合物,所得铁的物质的量可能为: ( )
A.无法计算确定 B.0.6mol C.0.5mol D.0.25mol
第Ⅱ卷非选择题(共52分)
15.工业以CaO和硝酸反应制Ca(NO3)2·4H2O晶体,为
确保制备过程既不补充水分,又无水剩余,则应选用的
硝酸反量分数为 ( )
A.无法计算 B.30% C.63% D.70%
14.下列各组物质中,满足下图物质一步转化关系的选项是 ( )
|
|
X |
Y |
 Z Z |
|
A |
Na |
NaOH |
NaHCO3 |
|
B |
Cu |
CuSO4 |
Cu(OH)2 |
|
C |
C |
CO |
CO2 |
|
D |
Si |
SiO2 |
H2SiO3 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com