
题目列表(包括答案和解析)
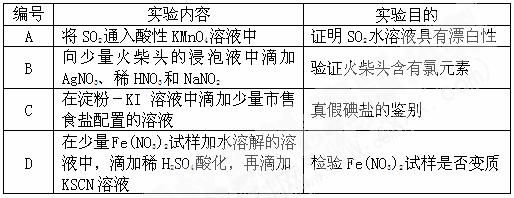
9.下述实验能达到预期目的的是
8.下列离子方程式书写正确的是( )
A.小苏打中加入过量的石灰水
Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O
B.氧化铁可溶于氢碘酸Fe2O3+6H+=2Fe3++3H2O
C.氯化镁溶液与氨水反应: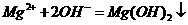
D.明矾溶液加入Ba(OH)2溶液至沉淀质量最多
Al3++2SO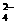 +2Ba2++4OH
+2Ba2++4OH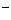 =Al(OH)4-+2BaSO4↓
=Al(OH)4-+2BaSO4↓
7.对于反应H- + NH3=H2 + NH2-的不正确的说法是
A.属于置换反应 B.H-是还原剂[
C.H2既是氧化产物又是还原产物
D.氧化产物与还原产物的化学计量数之比为1:1
6.同周期ⅠA和ⅢA族两种元素原子的核外电子数的差值不可能为
A.2 B.12 C.18 D.26
4.下列叙述正确的是
A.ⅠA族元素的金属性比ⅡA元素的金属性强
B.ⅦA族元素的氢化物中,稳定性最好的物质其沸点也最高
C.在零族元素的单质晶体中,既有共价键又有分子间作用力
D.同周期非金属氧化物对应的水化物的酸性从左到右依次增强
5 . 下列反应中生成物总能量高于反应物总能量的是 ( )
. 下列反应中生成物总能量高于反应物总能量的是 ( )
A.碳酸钙受热分解 B.乙醇燃烧
C.铝粉与氧化铁粉末反应 D.氧化钙溶于水
3.设NA为阿伏加德罗常数的值,下列叙述中正确的是
A.常温常压下,22 g 氧气和26 g 臭氧所含氧原子总数为3 NA
B.1L1 mol·L-1FeCl3完全水解生成NA个胶体粒子
C.1 mol SiO2中含有2 mol Si–O单键
D.常温常压下,1mol氦气分子含有的核外电子数为4NA
2.下列说法正确的是
A.把100mL10mol·L-1的H2SO4跟100mLH2O混合,硫酸的物质的量浓度改变为5mol·L-1
 B.把100g20%的NaCl溶液跟
B.把100g20%的NaCl溶液跟 100gH2O混合,NaCl溶液的质量分数是10%
100gH2O混合,NaCl溶液的质量分数是10%
C.把200mL3mol·L-1的BaCl2溶液跟100mL3mol·L-1的KCl溶液混合后,溶液中的C(Cl-)仍然是3mol·L-1
D.在浓度为1 mol/L的某酸溶液中,c(H+)≤1 mol/L
1. 下列化学用语
下列化学用语 使用正确的是
A. NH4Cl的电子式:
B.次氯酸的结构式:
H-Cl-O
使用正确的是
A. NH4Cl的电子式:
B.次氯酸的结构式:
H-Cl-O
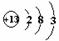
C.铝离子的结构示意图
D. 10个中子的氧原子:
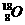
28. (14分)芳香族化合物A只有两个对位取代基,在一定条件下有如下图所示转化关系。其中,1 mol C与Na完全反应生成1
mol H2,若1 mol C与NaHCO3完全反应,也产生1 mol气体,E可以使溴的四氯化碳溶液褪色。 www.k@s@5@
高#考#资#源#网
(14分)芳香族化合物A只有两个对位取代基,在一定条件下有如下图所示转化关系。其中,1 mol C与Na完全反应生成1
mol H2,若1 mol C与NaHCO3完全反应,也产生1 mol气体,E可以使溴的四氯化碳溶液褪色。 www.k@s@5@
高#考#资#源#网
(1)D分子中的含氧官能团名称是 ,A的结构简式是 。
(2)反应④的基本类型是 反应,反应⑤的化学方程式是 。
(3)与C取代基位置相同,既能与FeCl3溶液显色、又能发生水解反应的同分异构体结构简式为: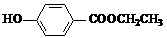 、
、 、 。
、 。
(4)现有C和E的混合物n mol,在空气中完全燃烧消耗O2 L(标准状况),若生成CO2 a L(标准状况)、H2O b g,则C、E混合物中含E的物质的量的计算式为: 。
26.(14分)在一定条件下,科学家利用从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇,其过程如下图所示,试回答下列问题:
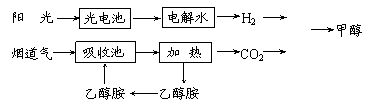
⑴ 该合成路线对于环境保护的价值在于 。
⑵ 15-20%的乙醇胺(HOCH2CH2NH2)水溶液具有弱碱性,上述合成线路中用作CO2吸收剂。用离子方程式表示乙醇胺水溶液呈弱碱性的原因: 。
 ⑶ CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式:
。
⑶ CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol,写出工业上以CO2、H2合成CH3OH的热化学方程式:
。
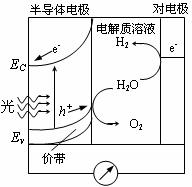
⑷ 科学家发明了一种基于右图所示原理的廉价光电化学电池装置,写出光照时半导体电极表面发生的电极反应式 。目前应用最多的半导体材料是Si,甚至有人提出硅是“21世纪的能源”,硅可作为新能源的原因可能的是 。
a.在自然界中存在大量的单质硅
b.硅可以通过化学方法“再生”
c.硅具有较强的亲氧性,燃烧放出的热量多
d.硅的化学性质不活泼,便于安全运输、贮存
27(16分)21世纪是钛的世纪。下面是利用钛白粉(TiO2)生产海绵钛(Ti)的一种工艺流程:
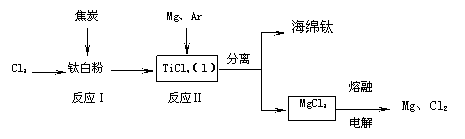
已知:① Mg(s)+Cl2 (g)=MgCl2 (s) △H=-641 kJ·mol-1
② Cl2(g)+1/2Ti (s)=1/2TiCl4 (l) △H=-385 kJ·mol-1
(1) 钛白粉是利用TiO2+发生水解生成钛酸(H2TiO3)沉淀,再煅烧沉淀制得的。
TiO2+发生水解的离子方程式为 。
(2)反应I在800-900℃下进行,还生成一种可燃性无色气体,该反应的化学方程式
 为
;反应II的热化学方程式为
。
为
;反应II的热化学方程式为
。
(3)该工艺流程中,可以循环使用的物质有 。
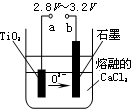
(4)在800℃-1000℃时电解TiO2也可制得海绵钛,装置如右图所示。图中b是电源的 极,阴极的电极反应式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com