
题目列表(包括答案和解析)
4.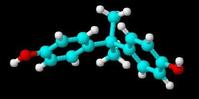 (原创)2010年年底,欧盟通过一项禁令,2011年3月1日开始,含有双酚A的塑料被禁止用于儿童奶瓶的生产。双酚A广泛应用于塑料生产,但直到20世纪90年代,科学家们才发现双酚A的另一面--作为一种环境激素,它的结构类似雌性激素,可能影响内分泌和生殖系统。双酚A结构如图,下列说法不正确的是
A.可以与Br2发生取代反应
B.1 mol该化合物可以与2 mol NaOH反应ww.k@s@5@
高#考#资#源#网
C.既可以催化加氢,又可以使酸性KMnO4溶液褪色
D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
(原创)2010年年底,欧盟通过一项禁令,2011年3月1日开始,含有双酚A的塑料被禁止用于儿童奶瓶的生产。双酚A广泛应用于塑料生产,但直到20世纪90年代,科学家们才发现双酚A的另一面--作为一种环境激素,它的结构类似雌性激素,可能影响内分泌和生殖系统。双酚A结构如图,下列说法不正确的是
A.可以与Br2发生取代反应
B.1 mol该化合物可以与2 mol NaOH反应ww.k@s@5@
高#考#资#源#网
C.既可以催化加氢,又可以使酸性KMnO4溶液褪色
D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
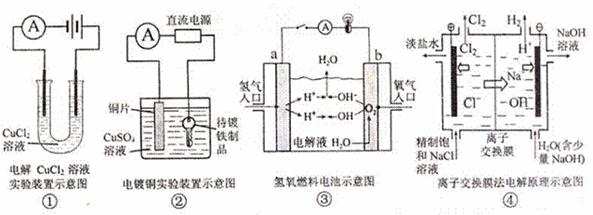
3、(根据2009云南统测6改编)观察下列几个装置示意图,有关叙述正确的是 A.装置①中阴极产物能使淀粉KI试纸变蓝 B.装置②的待镀铁制品应与电源正极相连 C.装置③中闭合电键后外电路电子由a极流向b极 D.装置④的离子交换膜允许阳离子、阴离子、水分子自由通过
2. (根据2010江苏卷13改编)已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料。下列说法正确的是
A.元素A、B组成的化合物常温下一定呈气态
B.一定条件下,元素C、D的最高价氧化物对应的水化物之间不能发生反应
C.化合物AE与CE古有相同类型的化学键ww.k@s@5@ 高#考#资#源#网
D.工业上常用电解法制备元素C、D、E的单质
1.(原创)下列有关说法正确的是
A、用红外光谱仪可以确定物质中是否存在某些有机原子团
B. 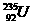 是一种常用的核燃料,与
是一种常用的核燃料,与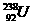 核外电子排布方式不同
核外电子排布方式不同
C. 可用米汤检验含碘盐中的碘酸钾(KIO3) D.绿色化学的核心是应用化学原理对环境污染进行治理
11.(常州一中2011届高三化学 改编)(12分)固定和利用CO2能有效地利用资源,并减少空气中的温室气体。CO2与化合物Ⅰ反应生成化合物Ⅱ,与化合物Ⅲ反应生成化合物Ⅳ,如反应①和②所示(其他试剂、产物及反应条件均省略)。
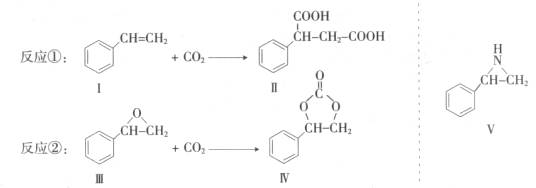
(1)化合物Ⅰ的分子式为__▲____,该物质至少有 ▲ 个碳原子共平面。ww.k@s@5@ 高#考#资#源#网
(2)由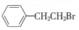 通过消去反应制备Ⅰ的化学方程式为___▲_____(注明反应条件)。
通过消去反应制备Ⅰ的化学方程式为___▲_____(注明反应条件)。
(3)Ⅱ与过量C2H5OH在酸催化下发生酯化反应,生成的有机物的结构简式为___▲_____。
(4)在一定条件下,化合物V能与CO2发生类似反应②的反应,生成两种化合物(互为同分
异构体),请写出其中任意一种化合物的结构简式:____▲____。
(5)与CO2类似,CO也能被固定和利用。在一定条件下,CO、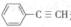 和H2三者发生反
和H2三者发生反
应(苯环不参与反应),生成化合物Ⅵ和Ⅶ,其分子式均为C9H8O,且都能发生银镜反应.下
列关于Ⅵ和Ⅶ的说法正确的有_____▲___(双选,填字母)。
A.都属于芳香烃衍生物 B.都能使溴的四氯化碳溶液褪色
C.都能与Na反应放出H2 D. 1 molⅥ或Ⅶ最多能与4 mol H2发生加成反应
10.(2010山东卷 改编)(16分)对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:

①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是__▲____(用离子方程式表示)。为将碱洗槽液中铝以沉淀形式回收,最好向槽液中加入下列试剂中的_▲_____.。
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4 溶液中电解,铝材表面形成氧化膜,阳极电极反应为__▲__。取少量废电解液,加入NaHCO3,溶液后产生气泡和白色沉淀,产生沉淀的原因是_▲____。
 (2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是__▲____。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是__▲____。
在铜的电解精炼中,应用粗铜作▲ ,精铜作 ▲ ,CuSO4溶液为电解质溶液。
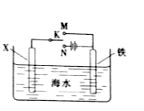
(3)利用右图装置,可以模拟铁的电化学防护。
若X为碳棒,为减缓铁的腐蚀,开关K应置于__▲____处。
若X为锌,开关K置于M处,该电化学防护法称为_____▲__。
9.(江苏省前黄高级中学2011届高三模拟考试 改编)(14分)ww.k@s@5@ 高#考#资#源#网
柴达木盆地以青藏高原“聚宝盆”之誉蜚声海内外,它有富足得令人惊讶的盐矿资源。液体矿床以钾矿为主,伴生着镁、溴等多种矿产。某研究性学习小组拟取盐湖苦卤的浓缩液(富含K+、Mg2+、Br-、SO42-、Cl-等),来制取较纯净的氯化钾晶体及液溴(Br2),他们设计了如下流程:
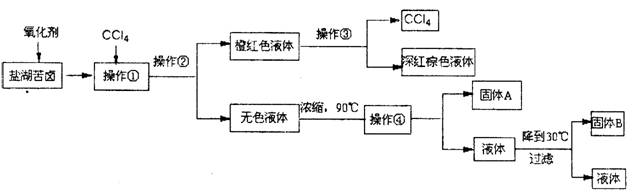
请根据以上流程,回答相关问题:
(1)操作①的名称是:_____▲_______;
操作④需要的玻璃仪器有:_______▲______。
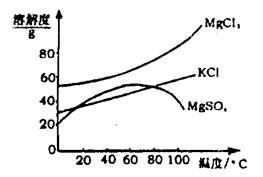
(2)参照右图溶解度曲线,固体B的主要成分 ▲
(3)同学甲提出一些新的方案,对上述操作②后
无色溶液进行除杂提纯,其方案如下:
[有关资料]
|
化学式 |
BaCO3 |
BaSO4 |
Ca(OH)2 |
MgCO3 |
Mg(OH)2 |
|
Ksp |
8.1×10一9 |
1.08×10一10 |
1.0×10一4 |
3.5×10一5 |
1.6×10一11 |
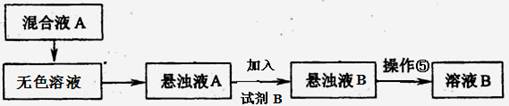 [设计除杂过程]
[设计除杂过程]
(i)若在操作⑤结束后发现溶液B略有浑浊,应采取的措施是▲ ,
(ii)混合液A的主要成分是 ▲ 试剂B的化学式是▲ (填化学式)。
[检验除杂效果]
(ⅲ)为检验Mg2+、SO42-是否除尽,通常分别取悬浊液A上层清液于两试管中。进行如下实验:
步骤一:检验Mg2+是否除尽。向其中一支试管中加入某溶液 ,如果没有沉淀生成,则表明Mg2+已除尽。效果最好的是 ▲ (填字母)。
A.K2 CO3 B.KOH C.CaCl2
步骤二:检验SO42-是否除尽。向另一支试管中加入BaCl2溶液,如果无有沉淀生成,则SO42-已除尽,ww.k@s@5@ 高#考#资#源#网
[获取纯净氯化钾]
(ⅳ)对溶液B加热并不断滴加l mol· L一1的盐酸溶液,同时用pH试纸检测溶液,直至pH=5时停止加盐酸,得到溶液C。
(ⅴ)将溶液C倒入 ▲ (填仪器名称)中,加热蒸发并用玻璃棒不断搅拌,直到 ▲ ,停止加热。
[问题讨论]
(ⅵ)进行操作⑤前,需先加热,使沉淀颗粒增大,便于过滤;该操作中控制溶液pH=12可确保Mg2+除尽,根据提供的数据计算,此时溶液B中Mg2+物质的量浓度 ▲ 。
8.( 2011年三月浙江金华、丽水、衢州十二校联考 改编)(16分)I、物质A-G有下图所示转化关系(部分反应物、生成物没有列出)其中A为某金属矿的主要成分,经过一系列反应可得到B和C。单质C可与E的浓溶液发生反应,G为砖红色沉淀。ww.k@s@5@ 高#考#资#源#网
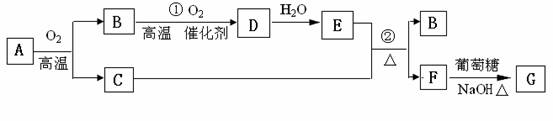
请回答下列问题
(1)写出下列物质的化学式:B ▲ E ▲ G ▲
(2)工业上B制备D在 ▲ 设备中进行.
(3)反应②的化学方程式是 ▲ 。
(4)将0.23molB和0.11mol氧气放入容积为1L的密闭容器中,发生反应①,在一定温度下,反应达到平衡,得到0.12molD,则反应的平衡常数K= ▲ L·mol-1,若温度不变,再加入0.50 mol氧气后重新达到平衡,平衡 ▲ (填“向左”、“不变”、“向右”)移动,氧气的转化率 ▲ ,(填“升高”“不变”或“降低”),D的体积分数
▲ (填“增大”“不变”或“减小”)
II、“蓝瓶子”实验中使用的亚甲基蓝(C16H18ClN3S·3H2O)是一种氧化还原型指示剂,其氧化型呈蓝色,还原型呈无色:
氧化型(蓝色)+ne- 还原型(无色)
还原型(无色)
将葡萄糖的碱性溶液放在锥形瓶中,滴加亚甲基蓝指示剂(蓝色),塞上瓶塞,溶液呈蓝色;静置一段时间,溶液褪色;振荡后,溶液又呈蓝色;再静置,又变无色;再振荡,又变蓝色……
⑴上述溶液由蓝色变无色的过程中,亚甲基蓝被 ▲ (填“氧化”或“还原”,下同),其中 ▲ 剂是 ▲ (填物质名称)。
⑵上述溶液由无色变蓝色的过程中,亚甲基蓝被 ▲ (填“氧化”或“还原”,下同),其中氧化剂是 ▲ (填物质名称)。
7.迷迭香酸是从蜂花属植物中提取到的酸性物质,其结构
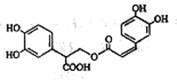 如下图所示。下列叙述正确的是
( )
如下图所示。下列叙述正确的是
( )
A.迷迭香酸的分子式为C18H15O8
B.该物质能使溴水或高锰酸钾溶液褪色,但不能与FeCl3溶液 发生显色反应
C.1mol迷迭香酸跟H2反应,最多消耗6molH2
D.1mol迷迭香酸与足量NaOH溶液反应,最多消耗6mol NaOH
6.(原创)下述实验能达到预期目的的是
|
编号 |
实验内容 |
实验目的 |
|
A |
在滴有酚酞的Na2CO3溶液中, 加入CaC12溶液后红色褪去 |
验证Na2CO3溶液中存在水解平衡 |
|
B |
将SO2通入中KMnO4溶液中 |
验证SO2具有漂白性 |
|
C |
淀粉溶液和稀H2SO4混合加热,后加新制的Cu(OH)2悬浊液加热至沸腾 |
检验淀粉水解产物有还原性 |
|
D |
将乙醇与浓硫酸共热制得的气体通入酸性KMnO4溶液中 |
检验气体中含有乙烯 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com