
题目列表(包括答案和解析)
7、下列有关电池的说法不正确的是( )
A.手机上用的锂离子电池属于一次电池
B.铜锌原电池工作时,电子沿外电路从锌电极流向铜电极
C.甲醇燃料电池可把化学能转化为电能
D.锌锰干电池中,锌电极是负极
(改编自09广东理科基础 34)
ww.k@s@5@ 高#考#资#源#网
第Ⅱ卷
6、人体血液内的血红蛋白(Hb)易与O2结合生成HbO2,因此具有输氧能力,CO吸入肺中发生反应: ,37 ℃时,该反应的平衡常数K=220 。
,37 ℃时,该反应的平衡常数K=220 。 的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是( )
的浓度达到HbO2浓度的0.02倍,会使人智力受损。据此,下列结论错误的是( )
A.CO与 反应的平衡常数
反应的平衡常数
B.人体吸入的CO越多,与血红蛋白结合的O2越少
C.当吸入的CO与O2浓度之比大于或等于0.02时,人的智力才会受损
D.把CO中毒的病人放入高压氧仓中解毒,其原理是使上述平衡向左移动
(09天津理综)
5、X、Y、Z是3种短周期元素,原子序数依次增大。其中X、Y位于同一周期,Y、Z位于同一主族。Y原子的最外层电子数是其电子层数的3倍。X、Y原子序数相差2。下列叙述不正确的是( )
A、XY2是直线型分子
B、Z元素最高价氧化物对应水化物的化学式可表示为H2ZO4 ww.k@s@5@ 高#考#资#源#网
C、3种元素的氢化物中,Y的氢化物最稳定
D、原子半径由大到小的顺序为Z>Y>X
(改编高中化学网题库)
4、下列化学实验事实及其解释都正确的是( )
A、向碘水中滴加CCl4,振荡静置后分层,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘
B、向SO2水溶液中滴加盐酸酸化的BaCl2溶液,有白色沉淀生成,说明BaSO3难溶于盐酸
C、向0.1mol/LFeSO4溶液中滴加少量酸性KMnO4溶液,KMnO4溶液褪色,说明Fe2+具有氧化性D、 向2.0mL浓度均为0.1mol/L的KCl、KI混合溶液中滴加1~2滴0.01 mol/L AgNO3 溶液,振荡,沉淀呈黄色,说明AgCl的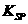 比AgI的
比AgI的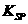 小
小
(改编自09年江苏化学9题)
3、北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开。S-诱抗素的分子结构如图,下列关于该分子说法正确的是 ( )
A、含有碳碳双键、羟基、碳基,羧基

B、1mol该物质可消耗2 molNaOH
C、分子式为C14H20O4
D、1mol该物质可与4molH2加成
(原创)
2、下列离子方程式正确的是 ( )
A、过量的NaHSO4与Ba(OH)2溶液反应:Ba2+十OH-十H+十SO42-=BaSO4↓ 十2H2O
B、苯酚钠溶液中通入少量CO2 C6H5O-+CO2+H2O= C6H5OH+HCO3-
C、氯化铵溶液中加入稀氢氧化钠溶液 NH4++OH-=NH3↑+H2O
D、用惰性电极电解饱和食盐水 2Cl- + 2H+=H2↑+ Cl2↑
(原创)
1、燃油税从2009年1月1日起开始征收,燃油税“燃”来好处之一是节能减排,抑制燃油的不合理消费。下列说法错误的是 ( )
A.石油的裂解是工业生产乙烯的主要方法
B.裂化汽油,不能使溴水褪色
C.石油是不可再生资源
D.辛烷有一种同分异构体的命名为3,3一二甲基己烷
(原创)ww.k@s@5@ 高#考#资#源#网
11.(14分)(成都树德中学2010高考模拟28题改编)某天然芳香族有机物A仅含C、H、O元素,与A相关的反应框图如下(图中每一步反应都进行完全),其中M分子式为CxHyO2Cl,能与NaHCO3溶液反应。A分子由22个原子构成,1molA完全燃烧生成的CO2比生成的H2O多4mol。K与银氨溶液不反应,P的最小环为四元环。
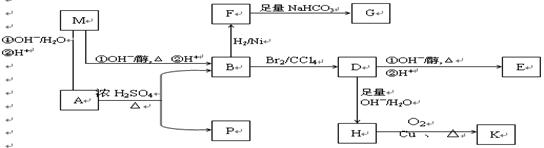
(1)写出下列反应的反应类型:
A→P ▲ ;D→E第①步反应 ▲ 。
(2)A的分子式为 ▲ ,B中所含的官能团名称是 ▲ 。
(3)写出A、D、E、S的结构简式:
G ▲ ,E ▲ ,P ▲ 。
(4)H到K的反应方程式为:
▲
(5)含有一个五元环结构,在一定条件下能发生水解反应,且由水解得到的两个侧链处于苯环的邻位,满足以上条件的B的芳香族同分异构体有 ▲ 种。写出其中一种同分异构体与足量NaOH溶液反应的化学方程式 ▲ 。
ww.k@s@5@ 高#考#资#源#网
ww.k@s@5@ 高#考#资#源#网
10. (15分)(重庆八中2011年第一次月考29题改编)纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。制备纳米TiO2的方法之一是TiCl4水解生成TiO2·xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2 。用氧化还原滴定法测定TiO2的质量分数操作如下:首先在一定条件下,把TiO2溶解并转化为Ti3+ ,再用NH4Fe(SO4)2标准溶液滴定Ti3+至全部转化成Ti4+。
请回答下列问题:
⑴ TiCl4水解生成TiO2·xH2O的化学方程式为___________▲ _________________。
⑵检验TiO2·xH2O中Cl-是否被除净的方法是__________▲ __________________。
(3)配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的目的是_______▲ ____;配制溶液使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要下图中的__▲ __(填字母代号)。
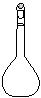
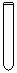
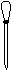
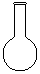
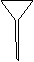
a b c d eww.k@s@5@ 高#考#资#源#网
(4)该滴定操作所用到的指示剂是 ▲ ,滴定终点的现象是 ▲
(5)滴定分析时,称取TiO2(摩尔质量为M g·mol-1)试样w g,消耗c mol·L-1NH4Fe(SO4)2标准溶液V mL,则TiO2质量分数为________▲ ______________。
9. (15分) (2011年苏、锡、常、镇四市高三教学情况调查17题改编)二甲基亚砜有消炎止痛、镇静等作用。甲醇和硫化氢在γ-Al2O3催化剂作用下
(2011年苏、锡、常、镇四市高三教学情况调查17题改编)二甲基亚砜有消炎止痛、镇静等作用。甲醇和硫化氢在γ-Al2O3催化剂作用下
生成甲硫醚(CH3-S-CH3),甲硫醚再与NO2反应制取二甲基亚砜 ( ),
有关反应如下:
反应① 2CH3OH(l)+H2S(g)=(CH3)2S(l) +2H2O(l) △H=―akJ·mol-1
反应②(CH3)2S(l)+NO2(g)=(CH3)2SO(l)+NO(g) △H=-bkJ··mol-1
反应③ 2NO(g)+O2(g)=2NO2(g) △H=-ckJ·mol-1
(1)写出用甲硫醚直接和氧气反应制取二甲基亚砜的热化学反应方程式
▲ ,
 (2)能说明反应2CH3OH(l)+H2S(g) (CH3)2S(l) +2H2O(l)达平衡状态的是 ▲ 。
(2)能说明反应2CH3OH(l)+H2S(g) (CH3)2S(l) +2H2O(l)达平衡状态的是 ▲ 。
A. v(CH3OH) = 2v(H2S)
B. 恒容容器中,体系的压强不再改变
C. 恒容容器中,体系中气体的密度不再改变
D. 恒容容器中,气体的摩尔质量不再改变
(3)反应③在一定条件下可达到平衡,则此条件下该反应平衡常数表达式K= ▲ 。
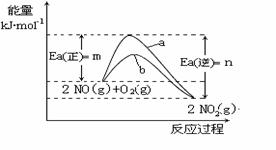
(4)上图是反应③在一定条件下发生反应,反应物和生成物能量与活化能的关系。在图中曲线_▲_(填“a”或“b”)表示加入催化剂的能量变化曲线,催化剂能加快反应速率的原理是___________________▲___________________________;
(5)N2O5是一种新型绿色硝化剂,其制备方法有以下两种。
方法一:4NO2(g)+O2(g) =2N2O5(g) ; △H=-56.76 KJ·mol-1 ww.k@s@5@ 高#考#资#源#网
常温下,该反应能逆向自发进行,则逆向反应的△S ▲ 0(填“>、<”或“=”)
方法二:用硼氢化钠燃料电池作电源,采用电解法制备得到N2O5。工作原理如下图:
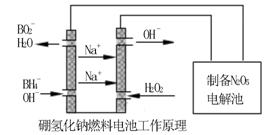
硼氢化钠燃料电池的正极反应式 ▲ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com